To describe the impact of the introduction of the viral tetra vaccine in the National Immunization Program in 2013 for 15‐month‐old children in mortality rates and hospitalization associated with varicella in Brazil.
MethodsMortality rates and hospitalizations rates associated with varicella were evaluated between 2010 and 2016 and described according to Brazilian macro regions and age. The population was stratified into age groups: < 1 year, 1‐4 years, and 5‐14 years. Data were collected from the Informatics Department of the Unified Health System. A percentage difference was calculated between rates of hospitalizations and mortality in the pre (2010‐2012) and post‐vaccination periods (2014‐2016) to estimate the approximate effectiveness of the vaccine.
Data synthesisAt the national level, vaccination significantly reduced the mortality rates and hospitalizations rates in all age groups analyzed. Among those under 5 years of age, mortality rates and hospitalizations rates decreased 57‐49% and 40‐47%, respectively. There was a national decrease of up to 57% in the mortality rates due to the disease, with smaller decreases seen in the North and Northeast regions and the largest in the South and Southeast regions. The hospitalizations rates for varicella reached a maximum national decline of 47%. In children aged 1–4 years, with higher vaccination coverage, the highest reduction was observed in both mortality rates and hospitalizations rates, which decreased from 2.6 to 0.4/100,000/year.
ConclusionsThe tetra vaccine proved to be effective in reducing both mortality and hospitalizations of children and adolescents up to 15 years of age in the 2014‐2016 triennium.
Descrever o impacto da introdução da vacina tetra viral no Programa Nacional de Imunização em 2013 para crianças de 15 meses nas taxas de mortalidade e de internação hospitalar associadas à varicela no Brasil.
MétodosAs taxas de mortalidade e de internação hospitalar associadas à varicela foram avaliadas entre 2010 e 2016 e descritas conforme macrorregiões brasileiras e idade. A população foi estratificada em grupos etários: < 1 ano; 1‐4 e 5‐14 anos. Os dados foram coletados do Departamento de Informática do Sistema Unificado de Saúde. Foi realizado um cálculo de diferença percentual entre taxas de internações e mortalidade nos períodos pré (2010‐2012) e pós‐vacinal (2014‐2016) para estimativa de impacto da vacina.
ResultadosNo nível nacional, a vacinação reduziu significativamente as taxas de mortalidade e de internação hospitalar em todas faixas etárias analisadas. Entre os menores de 5 anos, a taxas de mortalidade e de internação hospitalar diminuíram 57‐49% e 40‐47%, respectivamente. Houve uma queda nacional de até 57% nos índices de mortalidade pela doença, com menores quedas vistas nas regiões Norte e Nordeste e as maiores nas regiões Sul e Sudeste. As taxas de internação hospitalar por varicela atingiram queda nacional máxima de 47%. Em crianças de 1–4 anos, com maior cobertura vacinal, foi observada a maior redução tanto na taxa de internação hospitalar como na taxa de mortalidade, a qual passou de 2,6 para 0,4/100.000/ano.
ConclusõesA vacinação se mostrou efetiva em reduzir tanto mortalidade quanto hospitalizações das crianças e adolescentes de até 15 anos no triênio 2014‐2016.
O Programa Nacional de Imunizações (PNI) brasileiro é uma referência internacional de política pública de saúde. O país já erradicou, por meio da vacinação, doenças de alcance mundial como a varíola e a poliomielite. Uma das novidades no calendário foi a introdução da vacina contra o vírus varicela zoster (VVZ), que ocorreu em setembro de 2013, sob a forma de vacina tetravalente viral – sarampo, caxumba, rubéola e varicela (SCRV) – para lactentes aos 15 meses e mais recentemente, em 2018, a introdução de uma segunda dose de vacina contra varicela para crianças entre 4‐6 anos.1 Estimativas de 2014 calculam que a varicela gere aproximadamente 4 milhões de internações por complicações inerentes a doença e 4.000 mortes mundialmente todos os anos.2 No Brasil, dados do Sistema Único de Saúde apontam a varicela como causa de 1.800 mortes entre 2003‐2013, mais de 36% delas entre crianças de 1‐4 anos.3
Causada por um DNA vírus pertencente à ordem Herpervirales, família Herpesviridae, subfamília Alphaherpesvirinae, gênero Varicellovirus e espécie alphaherpesvirus humano 3, a varicela é marcada por sua alta transmissibilidade e por lesões exantemáticas pruriginosas características. Mesmo tendo uma evolução majoritariamente autolimitada, dura em torno de uma semana e evolui com cura espontânea, ela apresenta riscos inerentes à disseminação viral e às complicações por infecções secundárias em pele e tecidos moles, que podem se tornar fatais ao atingir articulações, ossos, pulmões e sistema neurológico.4
A vacina contra varicela foi desenvolvida no Japão na década de 1970, mas apenas na década de 1990 passou a ser usada na maioria dos países ocidentais.5 Ela induz imunidade através do vírus vivo atenuado e sua eficácia mostrou‐se alta: 70 a 90% na prevenção contra qualquer forma de varicela e de 95 a 100% na prevenção de doença grave.6
A efetividade da introdução da vacina já tem sido demonstrada em vários países ao redor do mundo, como, por exemplo, Austrália e Estados Unidos da América.7 Hoje, 5 anos após a introdução da vacina no Brasil e um ano após a introdução da segunda dose, é de interesse da saúde pública verificar o cenário da doença ao redor do país com o objetivo de avaliar suas mudanças epidemiológicas e fazer ajustes nos programas vacinais, caso necessário. Este estudo pretende comparar, em nível nacional e macrorregional, a frequência de internações e óbitos relacionados à doença antes e depois do advento da vacinação.
MétodosOs dados de mortalidade e internações relacionadas ao VVZ foram coletados do Departamento de Informática do Sistema Único de Saúde (Data SUS), por meio do website http://www2.datasus.gov.br/DATASUS/index.php?area=02. Na página de Informações de Saúde, foram acessadas a seção Mortalidade em Estatísticas Vitais para avaliar os óbitos relacionados à varicela, a seção Morbidade Hospitalar em Informações Epidemiológicas e Morbidade para avaliar internações relacionadas ao VVZ e a seção Imunizações em Assistência à Saúde para obtenção dos dados de cobertura vacinal. Os óbitos relacionados à varicela foram verificados de acordo com a Classificação Internacional de Doenças, 10ª Revisão [CID‐10]. Apenas os óbitos por Varicela Zoster (B01) foram considerados no cálculo de mortalidade, em virtude da baixa prevalência de Herpes Zoster na faixa etária estudada.
Focalizou‐se a atenção em três faixas etárias (< 1, 1‐4, 5‐14 anos) de maior interesse para a avaliação do impacto da vacina em curto prazo. A taxa de mortalidade (TM) por varicela foi calculada com a divisão do número de óbitos por varicela com a população de cada faixa etária e multiplicação por 100.000. O mesmo cálculo foi aplicado para determinar a taxa de internação hospitalar (TIH), calculada com a divisão do número de internações hospitalares por varicela com a população de cada faixa etária e multiplicação por 10.000. O tamanho da população usado nos denominadores foi obtido do Instituto Brasileiro de Geografia e Estatística (IBGE) com base no censo de 2010 e nas estimativas populacionais de 2011 a 2016. Houve perda inconstante de dados de mortalidade por falta de notificação estadual em todos os anos estudados, os estados de Rondônia (RO), Roraima (RR), Sergipe (SE), Tocantins (TO), Acre (AC) e Mato Grosso do Sul (MS) foram s mais afetados.
A evolução das taxas anuais por faixa etária e por macrorregiões brasileiras foi apresentada graficamente. O impacto da vacinação foi calculado como a diferença percentual das taxas no período pré versus pós‐vacinal. Análise estatística incluiu os números absolutos e as taxas por região e faixa etária. Para o cálculo das taxas e seus intervalos de confiança de 95% assumiu‐se a distribuição de Poisson dos desfechos (óbitos e hospitalizações). Foi usada a regressão de Poisson hierárquica que levou em conta os possíveis efeitos randômicos do impacto da vacinação entre os estados da mesma macrorregião e a correlação (“intraclasse”) entre as taxas anuais sucessivas de cada estado. Todas análises foram feitas no programa estatístico Stata, versão 12.0
Como este estudo usou uma fonte de dados secundária, de domínio público, e não envolveu sujeitos humanos, não foi necessária a obtenção de uma aprovação do comitê de ética.
ResultadosEm 2012, ano anterior à introdução da vacina, foram registradas 967 internações por varicela em menores de um ano no país. No mesmo ano, as complicações referentes à varicela foram relatadas como a causa da morte de 26 pacientes. Já em 2016, último ano analisado, foram registradas 597 internações e 8 óbitos.
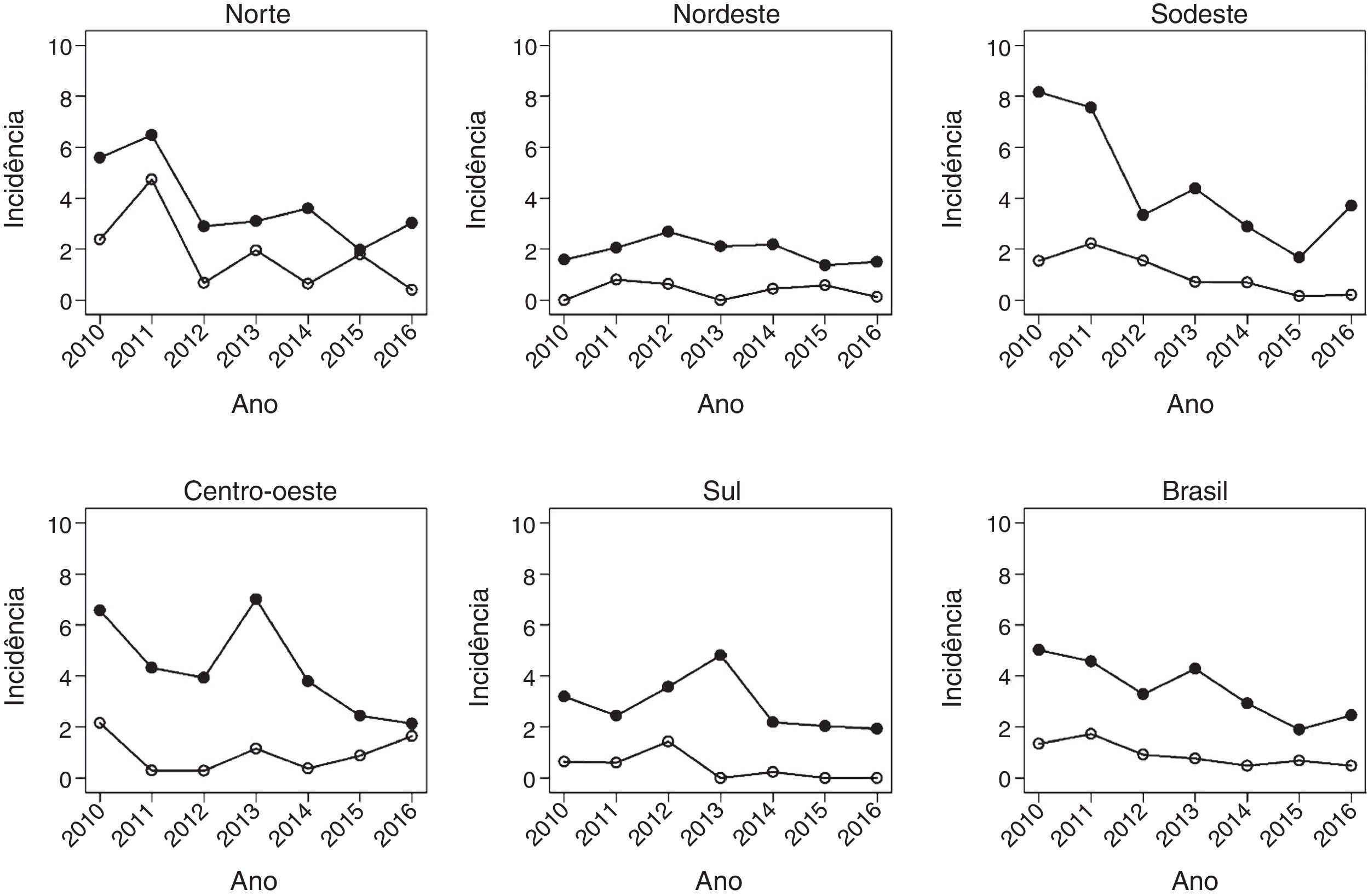
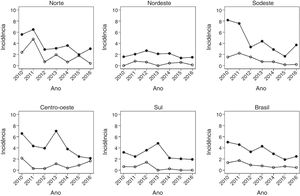
A fig. 1 mostra a evolução das taxas em menores de um ano entre 2010 e 2016. Houve uma diminuição da TIH em todas as regiões do país. No Brasil, a TIH diminui de 3,6 em 2012 para 2,5 em 2016. Houve ainda redução significativa de mortalidade pela doença na mesma faixa etária. A queda mais expressiva ocorreu na região Norte, seguida pelo Sudeste.
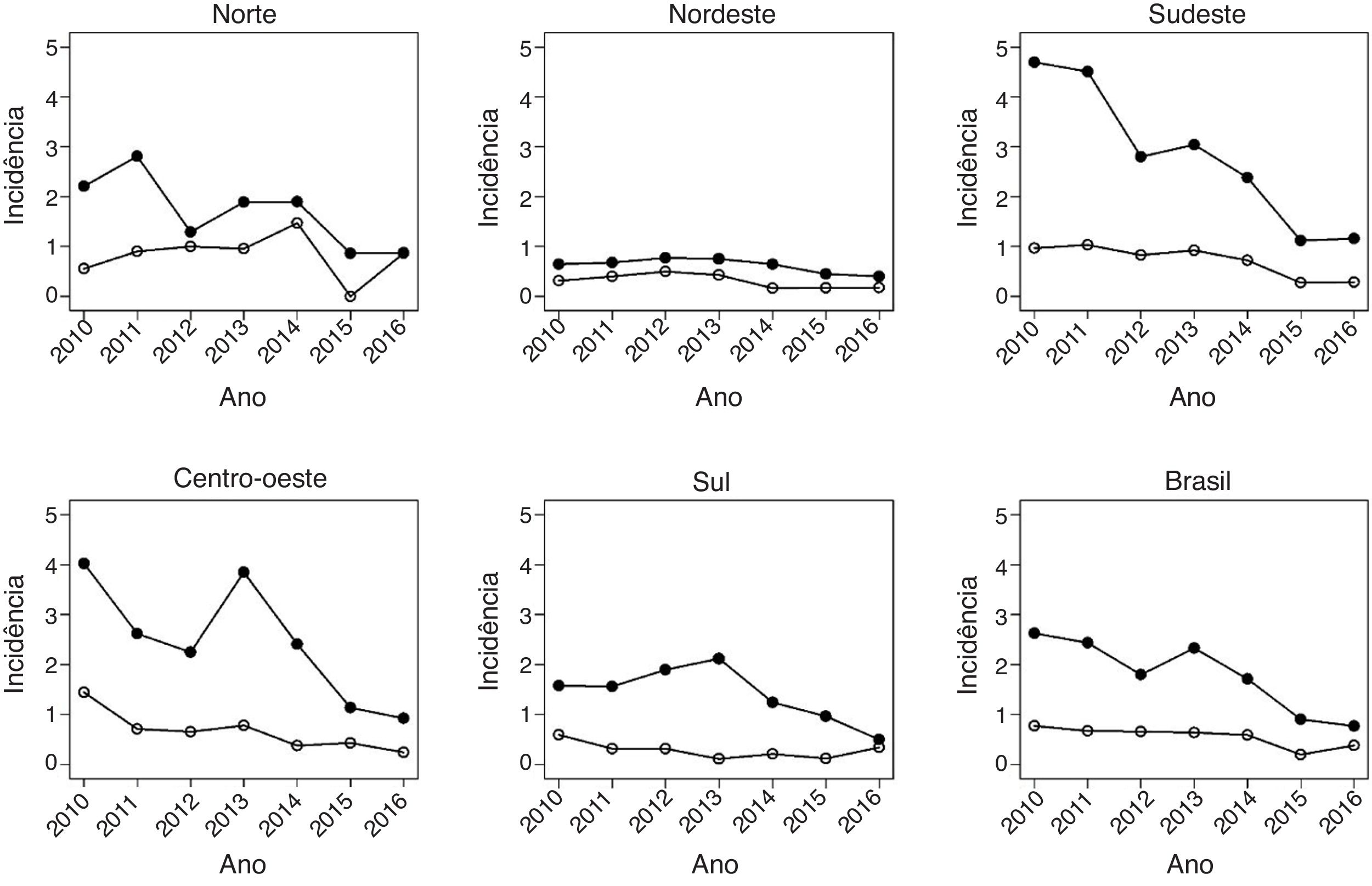
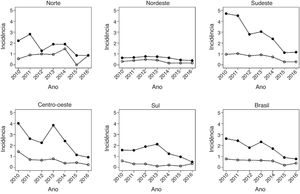
A fig. 2 traz a mesma análise temporal para a faixa etária de um a 4 anos, grupo de maior abrangência vacinal, a qual evidencia uma maior diminuição nas taxas de hospitalização nas regiões Sudeste, de 2,8 em 2012 para 1,4 em 2016, e Centro‐Oeste, de 2,3 para 1,2, Com relação aos óbitos nessa faixa etária, também se observou uma queda da mortalidade no cenário nacional, passou‐se de 0,9 óbito em 2010 para 0,4 a cada 100.000 crianças em 2016.
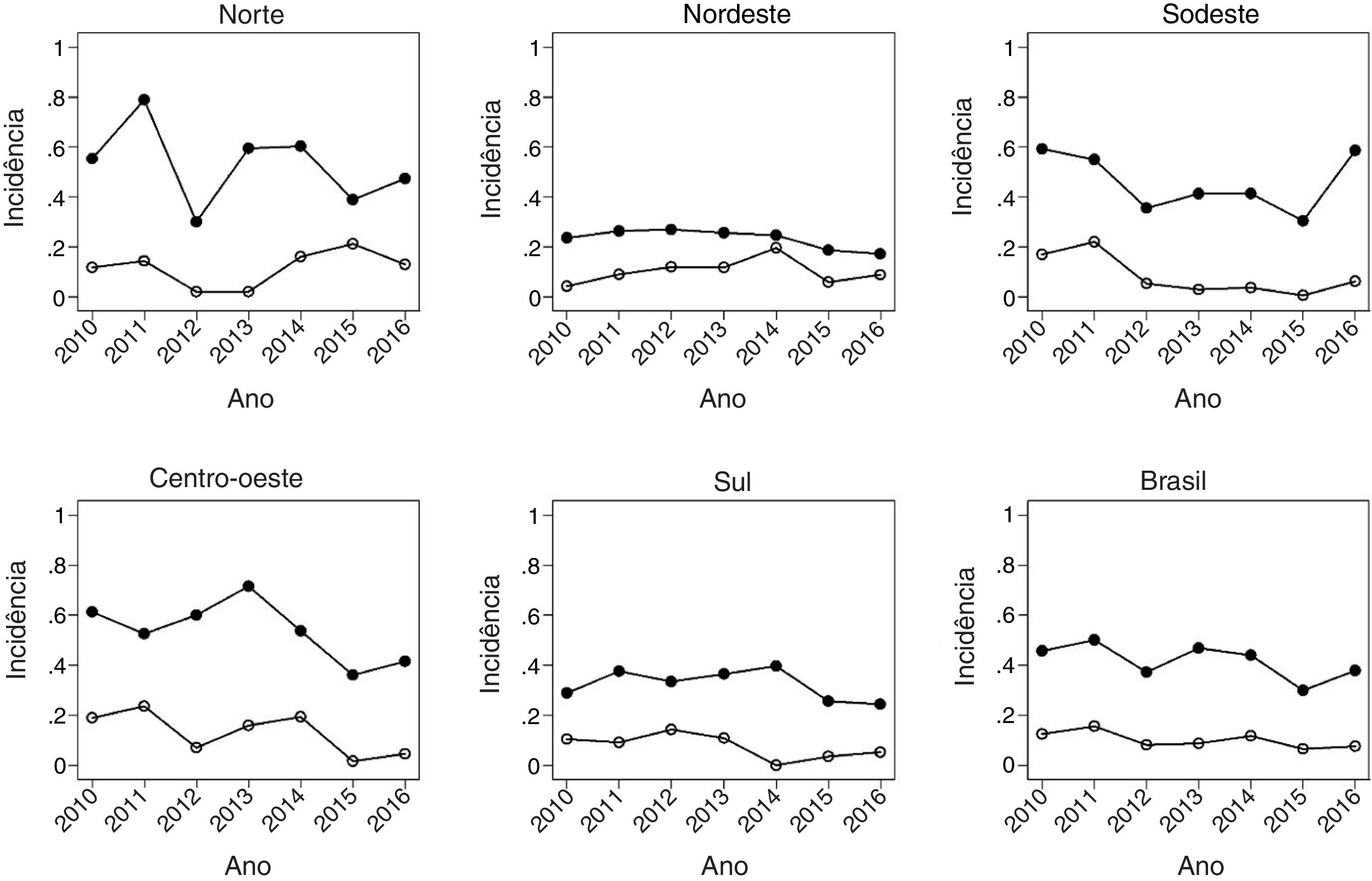
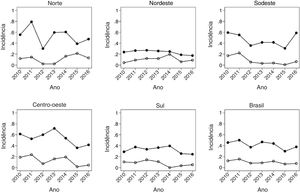
A fig. 3 abrange a maior faixa etária do estudo, 5‐14 anos, e demonstra maior variação das incidências no decorrer dos anos estudados. A região Sudeste manteve a mesma TM nos anos 2010 e 2016, após um súbito aumento entre 2015 e 2016 com relação aos anos prévios pós‐vacinais. A mortalidade apresentou uma queda em todas as regiões, foi mais pronunciada na região Centro Oeste.
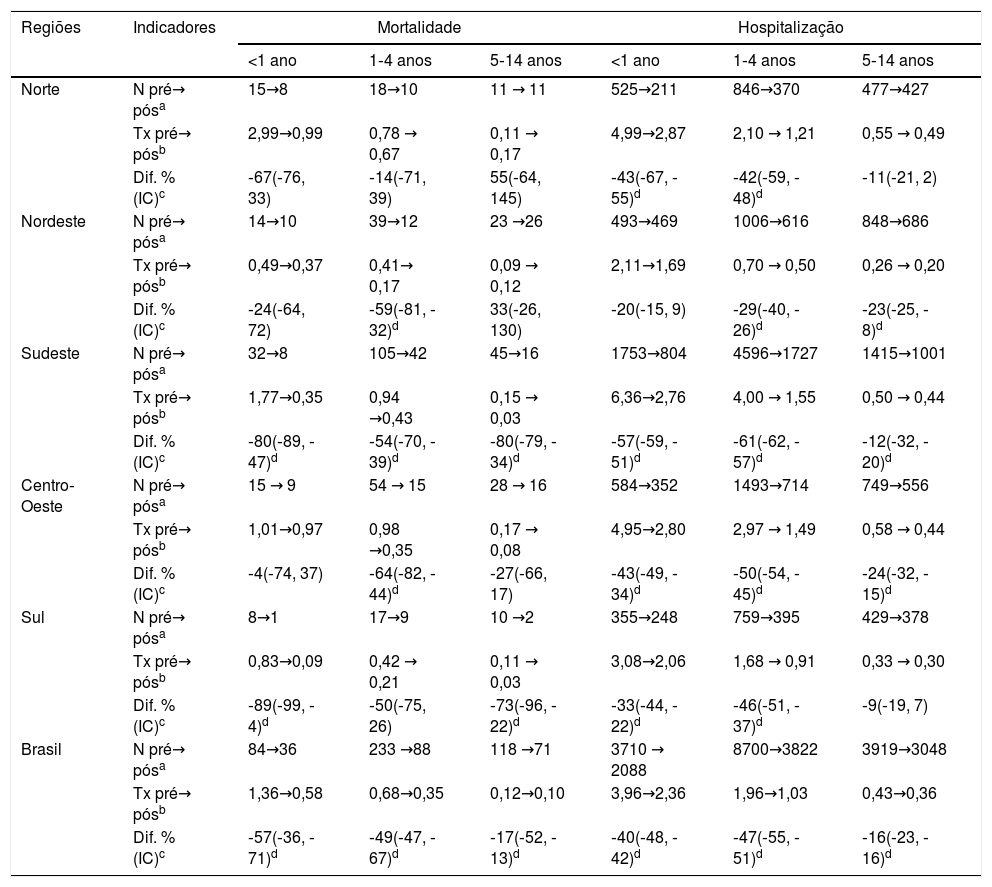
A tabela 1 mostra que, em nível nacional, a vacinação contra varicela reduziu significativamente as taxas de mortalidade e de hospitalização em todas as faixas etárias analisadas, embora esse efeito tenha sido menor na faixa de 5 a 14 anos (TM ‐ 17% e TIH ‐ 16%). Entre os menores de 5 anos, houve queda na TM de 57% em lactantes e 49% em crianças de 1‐4 anos. Já em internações, a queda foi de 40% e 47% respectivamente.
Diferença percentual das taxas de mortalidade e de hospitalização no período de três anos após (2014‐2016) vs. três anos antes (2010‐2012) da introdução da vacinação contra varicela, por faixa etária
| Regiões | Indicadores | Mortalidade | Hospitalização | ||||
|---|---|---|---|---|---|---|---|
| <1 ano | 1‐4 anos | 5‐14 anos | <1 ano | 1‐4 anos | 5‐14 anos | ||
| Norte | N pré→ pósa | 15→8 | 18→10 | 11 → 11 | 525→211 | 846→370 | 477→427 |
| Tx pré→ pósb | 2,99→0,99 | 0,78 → 0,67 | 0,11 → 0,17 | 4,99→2,87 | 2,10 → 1,21 | 0,55 → 0,49 | |
| Dif. % (IC)c | ‐67(‐76, 33) | ‐14(‐71, 39) | 55(‐64, 145) | ‐43(‐67, ‐55)d | ‐42(‐59, ‐48)d | ‐11(‐21, 2) | |
| Nordeste | N pré→ pósa | 14→10 | 39→12 | 23 →26 | 493→469 | 1006→616 | 848→686 |
| Tx pré→ pósb | 0,49→0,37 | 0,41→ 0,17 | 0,09 → 0,12 | 2,11→1,69 | 0,70 → 0,50 | 0,26 → 0,20 | |
| Dif. % (IC)c | ‐24(‐64, 72) | ‐59(‐81, ‐32)d | 33(‐26, 130) | ‐20(‐15, 9) | ‐29(‐40, ‐26)d | ‐23(‐25, ‐8)d | |
| Sudeste | N pré→ pósa | 32→8 | 105→42 | 45→16 | 1753→804 | 4596→1727 | 1415→1001 |
| Tx pré→ pósb | 1,77→0,35 | 0,94 →0,43 | 0,15 → 0,03 | 6,36→2,76 | 4,00 → 1,55 | 0,50 → 0,44 | |
| Dif. % (IC)c | ‐80(‐89, ‐47)d | ‐54(‐70, ‐39)d | ‐80(‐79, ‐34)d | ‐57(‐59, ‐51)d | ‐61(‐62, ‐57)d | ‐12(‐32, ‐20)d | |
| Centro‐Oeste | N pré→ pósa | 15 → 9 | 54 → 15 | 28 → 16 | 584→352 | 1493→714 | 749→556 |
| Tx pré→ pósb | 1,01→0,97 | 0,98 →0,35 | 0,17 → 0,08 | 4,95→2,80 | 2,97 → 1,49 | 0,58 → 0,44 | |
| Dif. % (IC)c | ‐4(‐74, 37) | ‐64(‐82, ‐44)d | ‐27(‐66, 17) | ‐43(‐49, ‐34)d | ‐50(‐54, ‐45)d | ‐24(‐32, ‐15)d | |
| Sul | N pré→ pósa | 8→1 | 17→9 | 10 →2 | 355→248 | 759→395 | 429→378 |
| Tx pré→ pósb | 0,83→0,09 | 0,42 → 0,21 | 0,11 → 0,03 | 3,08→2,06 | 1,68 → 0,91 | 0,33 → 0,30 | |
| Dif. % (IC)c | ‐89(‐99, ‐4)d | ‐50(‐75, 26) | ‐73(‐96, ‐22)d | ‐33(‐44, ‐22)d | ‐46(‐51, ‐37)d | ‐9(‐19, 7) | |
| Brasil | N pré→ pósa | 84→36 | 233 →88 | 118 →71 | 3710 → 2088 | 8700→3822 | 3919→3048 |
| Tx pré→ pósb | 1,36→0,58 | 0,68→0,35 | 0,12→0,10 | 3,96→2,36 | 1,96→1,03 | 0,43→0,36 | |
| Dif. % (IC)c | ‐57(‐36, ‐71)d | ‐49(‐47, ‐67)d | ‐17(‐52, ‐13)d | ‐40(‐48, ‐42)d | ‐47(‐55, ‐51)d | ‐16(‐23, ‐16)d | |
O impacto da vacinação foi heterogêneo entre as macrorregiões do país. Com relação à mortalidade, a queda significantemente estatística entre menores de um ano foi de 80% na região Sudeste e 89% na região Sul. Já para crianças de 1‐4 anos a queda foi de 54% na região Sudeste, 59% no Nordeste e 64% no Centro Oeste, com coberturas vacinais de 87%, 79%, 86%, respectivamente. Na faixa de 5 a 14 anos, houve queda com significância estatística apenas nas regiões Sul (73%) e Sudeste (80%).
A redução da TIH teve amplitude de 33% no Sul a 57% no Sudeste entre menores de um ano. Entre 1‐4 anos foi observada redução significativa em todas as regiões, variou de 29% no Nordeste a 61% no Sudeste, com coberturas vacinais médias de 78% e 87%, respectivamente. No Nordeste observou‐se uma redução de 23% na TIH entre 5‐14 anos, já no Sudeste a diminuição foi de 12% nessa faixa etária. A região Sudeste mostrou a maior consistência e magnitude da redução de mortalidade e hospitalização sobre as faixas etárias analisadas. A região Sul teve o menor número de óbitos e das hospitalizações, provavelmente associado a uma cobertura vacinal de quase 86%. Ao mesmo tempo, o baixo número de eventos contribuiu para aumento da variação das estimativas para essa região por razões estatísticas.
No nível nacional, nenhuma das faixas etárias apresentou o valor de zero no intervalo de confiança de (IC) de 95%. Portanto, houve uma redução significativa da diferença percentual após a vacinação comparada ao período pré‐vacinal para TM e TIH.
DiscussãoEste estudo demonstrou significativa redução da morbimortalidade por varicela no Brasil após a introdução da vacina tetra viral no PNI. Vale ressaltar que, de modo geral, foi observada uma queda mais expressiva da TM comparada com a TIH por varicela. Isso pode ocorrer por fatores como melhoria do manejo hospitalar das complicações da infecção por VVZ e redução da infecção em grupos de maior risco de óbito, como lactentes, imunodeficientes e adolescentes.
Embora a SCRV tenha sido fornecida apenas para crianças aos 15 meses, viu‐se uma redução das taxas de internação e óbitos em todas as faixas etárias estudadas. A redução mais expressiva da hospitalização ocorreu, de forma geral, na faixa de 1‐4 anos, o que condiz com o esperado, por ser a população alvo da vacinação.8 O curto período pós‐vacinal estudado pode ter subestimado a efeito indireto proporcionado pela vacinação em longo prazo. Entretanto, persistem dúvidas se uma dose única da vacina pode ser suficiente para gerar imunidade de grupo.9
Os dados também mostram a manutenção de um maior número absoluto de ocorrência de casos graves em lactentes < 1 ano quando comparados às outras faixas etárias, oriundo, provavelmente, da baixa concentração de anticorpos maternos contra o VVZ e de um sistema imunitário em amadurecimento.10,11 Contudo, percebe‐se uma importante redução da mortalidade e internações hospitalares no referido grupo, reflexo provável de proteção coletiva indireta. Entretanto, é vital ressaltar que a coorte de crianças imunizadas tende a aumentar progressivamente ao longo dos anos, o que acarretará uma menor circulação do vírus e potencializará o efeito de imunização coletiva.12
Na faixa entre 5‐14 anos, houve uma queda menos acentuada nos índices. Isso pode ser oriundo, em grande parte, do fato de não serem a população diretamente imunizada, pelo maior convívio em ambientes fechados (creches e escolas) e pela tendência de ocorrência de casos mais graves da doença de acordo com o aumento da idade.13,14
Dois estudos feitos nos Estados Unidos entre 2 e 4 anos após a introdução da vacina contra VVZ no país observaram resultados pouco expressivos na queda da incidência de internações. Os dados divulgados por Rhein et al., referentes aos dois primeiros anos pós‐vacinais, não demonstraram queda nas taxas de internações. Enquanto o segundo estudo, que analisou os 4 anos após a introdução vacinal, mostrou uma queda de 23,5% nas hospitalizações por varicela no país. A melhoria gradual foi atribuída ao aumento da cobertura vacinal do país de 43,2% para 59% entre os anos estudados. Contudo em 2004, Davis et al. ressaltaram erros metodológicos nos referidos estudos. Em uma nova análise, eles observaram queda de aproximadamente 74% na TIH em 9 anos estudados.15–17
Em um estudo de levantamento nacional australiano que comparou os três anos prévios com os cinco anos após a introdução nacional da vacina contra VVZ, foi observada uma queda de 57,3% da TIH relacionada à varicela na população geral, com queda mais acentuada (de 83,3 para 29,3/100.000/ano) em crianças entre 1‐4 anos, a cobertura vacinal variou entre de 82% e 90% no período estudado.18
Uma revisão sistemática, publicada em 2019, que incluiu estudos de países latino‐americanos e caribenhos, mostrou, dentre outros dados, expressiva redução na TIH após a introdução vacinal na Costa Rica, 87% em menores de 5 anos, no Uruguai, 81%, e em Porto Rico, 76%. Na Costa Rica foi observado ainda um aumento, de 23 para 24, no número absoluto de óbitos entre os períodos pré e pós‐vacinal.19
Após a introdução pioneira da vacinação contra a varicela em Florianópolis, em 2002, foi observada uma redução da incidência da doença em crianças entre 1‐4 anos, sem evidência de efeito indireto associado.20 O presente estudo mostra que, nos três primeiros anos da implantação da vacinação universal das crianças de 15 meses, ocorreu queda de 16% da TIH em crianças maiores de 5 anos e adolescentes brasileiros. Reflexo provável de efeito indireto da cobertura vacinal, que atingiu uma média de 82% no período estudado.21
Observou‐se ainda, nas faixas <1 ano e 5‐14 anos, um aumento da TIH entre 2015 e 2016. Essa maior incidência é decorrente da queda da cobertura vacinal em 2015, reflexo da falta de vacina em algumas regiões nacionais nos anos supracitados e, possivelmente, do crescente movimento antivacinal.22,23
O presente estudo mostra que o impacto da vacinação foi heterogêneo. Portanto, a média nacional, descrita por Scotta et al. em 2018, não é suficiente para elucidar a evolução da morbimortalidade no período analisado. As cinco regiões apresentaram padrões epidemiológicos de queda diferentes. Por exemplo: as regiões Sudeste e Sul apresentaram uma maior queda de mortalidade na população menor de um ano. Já a região Norte apresentou importante queda da TIH quando comparada inclusive com a região Sul. Isso poderia ser explicado pelas diferentes características socioeconômicas das regiões estudadas, tais como o índice de desenvolvimento humano, o acesso a serviços de saúde privados e a cobertura vacinal das regiões.24,25
Outra divergência importante encontrada entre o presente estudo e o estudo de 2018 é o período pré‐vacinal estudado. O período de 11 anos usado por Scotta et al. é longo o suficiente para refletir as causas da hospitalização não relacionadas a vacina, tais como melhoria no acesso ao sistema de saúde pública. O mesmo efeito é drasticamente reduzido com período pré‐vacinal de 3 anos usado no presente estudo. Além disso, o referido estudo incluiu 2013 na análise do período pós‐vacinal apesar de suas características atípicas, tais como a baixa cobertura vacinal (< 50%), que provavelmente foi insuficiente para produzir um efeito significativo.
Acrescenta‐se ainda que o estudo de Scotta et al. usou séries temporais com dados mensais de taxa de internação hospitalar por VVZ e a diferença entre as médias das taxas no período pré versus pós‐vacinal foi calculada por meio de teste t de Student para amostras independentes, embora essa suposição seja pouco crível, visto que a circulação do vírus nos meses anteriores foi o principal determinante do risco da infecção no período. O presente estudo usou a regressão hierárquica (multinível) de Poisson para levar em conta essa dependência temporal por meio da correlação intercalasse dentro das medidas repetidas na mesma unidade federativa a cada ano e dentro das unidades da mesma macrorregião do país. A regressão de Poisson permite fazer estimativas substanciais do erro‐padrão.
O presente estudo apresenta algumas limitações por ser do tipo ecológico retrospectivo, embasado nos dados secundários, é difícil avaliar a qualidade dos dados obtidos. Além disso, o diagnóstico da varicela é predominantemente clínico. Portanto, é possível que a doença seja subdiagnosticada e subnotificada, principalmente nas regiões do país nas quais o acesso aos serviços de saúde ainda é precário. Destaca‐se sobretudo que o curto período pós‐intervenção disponível para análise reduz o poder da análise estatística. Estudos posteriores, com maiores períodos pós‐vacinais, poderão mostrar com maior acurácia a efetividade da vacinação em reduzir hospitalizações e óbitos por varicela em médio e longo prazo.
É vital ressaltar que séries temporais de comparação antes e depois pressupõem homogeneidade entre os grupos confrontados nos dois períodos. É pouco provável que a redução das taxas aqui apresentadas resulte exclusivamente de um aumento ao acesso aos serviços de saúde e da melhoria do nível socioeconômico das populações estudadas.20 É importante ressaltar, por fim, que o tratamento efetivo da varicela não apresentou mudanças significativas após a introdução da vacina contra VVZ. Portanto, não explicaria a magnitude da redução de mortalidade e internações pela doença encontradas no presente estudo.4
Em conclusão, o presente estudo demonstrou uma significativa redução das taxas de mortalidade e da internação hospitalar em crianças e adolescentes de até 14 anos após a introdução da vacina contra varicela no PNI em 2013. Contudo, os valores ainda se mostram aquém dos observados em países com maior tempo de adesão vacinal e com programas vacinais que incluem uma segunda dose. Um acompanhamento epidemiológico dos avanços nos casos de varicela e da cobertura vacinal brasileira é essencial para avaliar a criação de políticas públicas de saúde que visem à manutenção de uma cobertura vacinal eficaz. Faz‐se necessária também uma nova avaliação da efetividade vacinal após a introdução da segunda dose da vacina contra varicela em 2018, a qual visa à correção de falha vacinal da primeira dose, prevenção de surtos em escolares e a um aumento da proteção por efeito rebanho.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Como citar este artigo: Ribeiro MZ, Kupek E, Ribeiro PV, Pinheiro CE. Impact of the tetra viral vaccine introduction on varicella morbidity and mortality in the Brazilian macro regions. J Pediatr (Rio J). 2020;96:702–9.