To compare the values of the markers for volumetric capnography and spirometry and their ability to classify children and adolescents with asthma, cystic fibrosis (CF), and healthy controls.
MethodsThis was a cross‐sectional study that included 103 patients with controlled persistent allergic asthma, 53 with CF and a healthy control group with 40 volunteers (aged 6–15 years), of both sexes. The individuals underwent volumetric capnography and spirometry.
ResultsPhase III slope (SIII), SIII standardized by exhaled tidal volume (SIII/TV) and capnographic index (SIII/SII)×100 (KPIv) were different among the three groups assessed, with highest values for CF. The relation between the forced expiratory volume in one second and the forced vital capacity (FEV1/FVC) was the only spirometric marker that presented difference on the three groups. On individuals with normal spirometry, KPIv and FEV1/FVC were different among the three groups. The ROC curve identified the individuals with asthma or CF from the control group, both through volumetric capnography (better to identify CF in relation to the control using KPIv) and through spirometry (better to identify asthma in relation to the control). KPIv was the best parameter to distinguish asthma from CF, even in individuals with normal spirometry.
ConclusionVolumetric capnography and spirometry identified different alterations in lung function on asthma, CF, and healthy controls, allowing the three groups to be distinguished.
Comparar os valores dos marcadores para capnografia volumétrica e espirometria e sua capacidade de classificar crianças e adolescentes com asma, fibrose cística (FC) e controles saudáveis.
MétodosFoi realizado um estudo transversal que incluiu 103 pacientes com asma alérgica persistente controlada, 53 com FC e um grupo controle saudável com 40 voluntários (6 a 15 anos), de ambos os sexos. Os indivíduos foram submetidos a capnografia volumétrica e espirometria.
ResultadosO slope da fase III (SIII), SIII padronizada pelo volume tidal exalado (SIII/VT) e o índice capnográfico (SIII/SII)×100 (KPIv) foram diferentes entre os três grupos avaliados, com maiores valores para o grupo FC. A relação entre o volume expiratório forçado no primeiro segundo e a capacidade vital forçada (VEF1/CVF) foi o único marcador de espirometria com diferenças nos três grupos. Nos indivíduos com espirometria normal, o KPIv e VEF1/CVF foram diferentes entre os três grupos. A curva ROC diferenciou os indivíduos com asma ou FC daqueles do grupo controle, ambos através da capnografia volumétrica (melhor para identificar a FC em relação aos controles pelo KPIv) e por meio da espirometria (melhor para identificar a asma em relação aos controles). O KPIv foi o melhor parâmetro para distinguir a asma da FC, mesmo em indivíduos com espirometria normal.
ConclusãoA capnografia volumétrica e a espirometria identificaram diferentes alterações de função pulmonar na asma, na FC e nos controles saudáveis, permitiram que os três grupos fossem diferenciados.
A asma está entre as doenças crônicas mais comuns em crianças e adolescentes; entretanto, a fibrose cística (FC) é pouco prevalente.1 Ambas as doenças pulmonares crônicas (FC e asma) apresentam obstrução das vias aéreas, mas cada uma delas com uma fisiopatologia diferente. Vários instrumentos têm sido estudados e propostos para avaliar os danos anatômicos e funcionais causados por ambas as doenças. A capnografia volumétrica (CapV) permite a análise gráfica do padrão de concentração de dióxido de carbono (CO2) no volume de ar exalado, representa a fonte anatômica de CO2. Três fases podem ser identificadas durante a CapV,2,3 inclusive o slope da fase III (SIII), que tem correlação direta com o grau de variação da ventilação/perfusão no modelo de lesão pulmonar e varia em um número elevado de doenças.4–7 Para recém‐nascidos, o SIII pôde possivelmente identificar prematuros com displasia broncopulmonar de outros sem doença pulmonar.8 O ângulo entre os slopes das fases II e III é conhecido como índice capnográfico (KPIv) e pode ser usado como um teste de triagem para a gravidade da doença pulmonar na FC.9 Quando comparado com outros testes de avaliação da função pulmonar, a CapV tem a vantagem de ser portátil, não invasiva, não usar gases caros e ser feita com respiração espontânea.10–12 Além disso, anteriormente, observamos que o SIII padronizado pelo volume tidal exalado (SIII/VT) é maior em crianças com asma, pode refletir na homogeneidade da ventilação, sugerir doenças respiratórias estruturais crônicas. Após o teste de provocação com metacolina, o SIII aumentou e subsequentemente diminuiu após a terapia inalatória com agentes broncodilatadores. Esse fato sugere o assincronismo no esvaziamento das unidades alveolares devido à ação constritiva da metacolina nas vias aéreas periféricas.10 Observamos também um aumento no valor do SIII em indivíduos com FC quando comparados com crianças e adolescentes saudáveis. Os valores do SIII foram maiores em pacientes com espirometria normal, sugeriram que a CapV pode identificar pacientes com alterações na homogeneidade da ventilação muito precocemente.13
Como hipótese, acreditamos que a CapV pode captar anormalidades da função pulmonar precocemente no contexto da espirometria normal. Além disso, enquanto a asma é primariamente uma doença das vias aéreas que pode ser descrita por anormalidades espirométricas, a FC é uma doença mista parenquimatosa/das pequenas vias aéreas que seria mais bem descrita pela CapV e no SIII da capnografia.
Portanto, o objetivo deste estudo foi comparar os marcadores para CapV e espirometria em crianças e adolescentes com asma, FC e controles saudáveis. Além disso, avaliamos a capacidade dos marcadores de identificar a que grupo cada indivíduo pertence.
MétodosFoi feito um estudo transversal, analítico, observacional e não randomizado, durante três anos no Laboratório de Fisiologia Pulmonar (Lafip) da Universidade de Campinas para completar o recrutamento. O projeto foi aprovado pelo Comitê de Ética em Pesquisa da Instituição (n° 419/2005 e n° 430/2008). Os responsáveis pelas crianças assinaram um termo de consentimento informado.
Foram incluídos três grupos de indivíduos: (i) 103 com asma alérgica persistente controlada (GAA); 53 com FC (GFC) – fora do período de exacerbações pulmonares; (iii) 40 voluntários como controles saudáveis (GCS). A idade de inclusão foi de seis a 15 anos, de ambos os sexos.
Os pacientes foram acompanhados no Ambulatório de Pneumologia Pediátrica do Hospital Universitário da instituição e recrutados durante a consulta de rotina. Todos os pacientes em acompanhamento no serviço foram convidados a participar do estudo e apenas os pacientes que aceitaram participar foram incluídos.
O diagnóstico e classificação da asma foram estabelecidos com os critérios da Global Initiative for Asthma (Gina).
Os pacientes com asma apresentavam dosagem sérica de imunoglobulina E superior a 180 UI/mL em pelo menos uma amostra de sangue, eosinófilos no sangue periférico> 4% e resposta positiva a pelo menos um antígeno testado em testes cutâneos de hipersensibilidade imediata. Os pacientes com asma usaram corticosteroide inalado (budesonida) em forma de pó seco com uma dose de 400 a 800 mcg/dia e formoterol 12 mcg duas vezes/dia, por pelo menos 30 dias como critério de inclusão, com o objetivo de obter‐se uma população mais homogênea. Nenhum paciente apresentou história de ataque de asma que necessitasse de internação em unidade de terapia intensiva no último ano, exacerbação ou pioria dos sintomas com necessidade de maior uso de broncodilatadores inalatórios ou corticosteroides sistêmicos por quatro semanas antes dos testes.
O diagnóstico de FC foi feito pelo teste do suor com estimulação da sudorese através da iontoforese pela pilocarpina (pelo menos duas doses de concentração de cloreto> 60 mEq/L) e/ou pela identificação de duas mutações do gene regulador da condutância transmembrana da fibrose cística (CFTR).
O GCS era composto por voluntários sadios, sem tabagismo ativo ou passivo, sem doença respiratória prévia ou atual, que não usavam medicação e não tinham comorbidades conhecidas. Os indivíduos incluídos não apresentaram grandes dificuldades para fazer a espirometria e a CapV.
As características clínicas dos participantes foram documentadas pela equipe médica durante as consultas para a espirometria e a CapV.
Capnografia volumétricaPara a CapV, foi usado o monitor de perfil respiratório CO2SMO Plus® modelo DX‐8100 (Novametrix, Wallingford, EUA) e o software Analysis Plus (Oasis Analysis Plus®, MS, EUA) para Windows para registro das medidas e curvas da CapV. Solicitamos aos participantes que se sentassem de costas para o monitor, usassem um clipe nasal e respirassem pelo bocal. Iniciamos com o registro dos marcadores da CapV por cinco minutos, após observarmos a normalização do padrão respiratório, e selecionamos uma sequência off‐line dos ciclos respiratórios dos pacientes após a coleta, excluímos os ciclos do primeiro minuto, os consideramos como um período de adaptação do indivíduo. Após esse procedimento, foram excluídos os ciclos respiratórios que apresentaram padrões irregulares da curva da CapV, como a ausência do platô devido ao vazamento de ar ou depressão do platô devido à tosse. Os ciclos em que a variação do VT foi maior ou menor do que 25% da média e nos quais o CO2 exalado foi maior ou menor do que 5% da média também foram excluídos.10,13,14
A média dos marcadores dos ciclos remanescentes foi calculada e considerada como o resultado final. Três fases podem ser identificadas durante a CapV: (fase I) corresponde ao espaço morto anatômico; (fase II) aumento rápido do CO2; (fase III) formação do platô de CO2 exalado correspondente ao volume de ar alveolar.2,3 Os marcadores analisados foram: SII e SIII. Usamos também o índice capnográfico [(SIII / SII) x 100] (KPIv).8,9,15 A normalização de SII e SIII pelo VT (SII/VT e SIII/VT) foi feita para compensar as variações no tamanho dos indivíduos.
EspirometriaPara a avaliação da espirometria, usamos o espirômetro modelo CPFS/D e o software BREEZE PF® versão 3.8B (MedGraphics, MN, EUA). A triagem foi feita de acordo com as recomendações da European Respiratory Society e American Thoracic Society.16 Os pacientes foram instruídos a não usar broncodilatadores de curta ou longa duração por 12 horas antes do exame. Os marcadores espirométricos foram ajustados ao escore‐z com o uso do software GLI2012 fornecido pela Global Lung Initiative (GLI) da European Respiratory Society.17 Foram usados os seguintes marcadores para o estudo: capacidade vital forçada (CVF), volume expiratório forçado no primeiro segundo da CVF (VEF1), índice de obstrução (VEF1/CVF) e fluxo expiratório forçado entre 25% e 75% da CVF. (FEF25‐75%) expressos como escore z e porcentagem do previsto.
Análise estatísticaComparações entre marcadores independentes sem distribuição normal foram feitas com o teste de Mann‐Whitney.
A curva ROC (Receiver Operating Characteristic) e a área sob a curva ROC (AUC) foram calculadas para avaliar o potencial dos marcadores de espirometria e CapV para diferenciar pacientes com asma de controles saudáveis, pacientes com FC de controles saudáveis e pacientes com FC daqueles com asma. Os marcadores da CapV que foram diferentes nos três grupos no estudo de associação foram usados para a análise da curva ROC.
A porcentagem do previsto foi usada devido ao seu extenso uso na prática clínica.18 Valores abaixo de 80% do previsto para os marcadores espirométricos foram considerados como abaixo do limite inferior do normal (LIN). Fizemos o escore‐z dos marcadores da CapV para o GCS. O LIN e o limite superior do normal (LSN) para os marcadores da CapV foram considerados<−2 e>+2 do escore z do GCS. Um subgrupo de indivíduos dos três grupos foi considerado como tendo espirometria “normal”, com o uso como critério de inclusão dos resultados de CVF, VEF1 e VEF1/CVF abaixo do LIN (80% do previsto para todos esses marcadores da espirometria).
Para comparar os grupos e analisar a curva ROC, usou‐se o software SPSS (SPSS Inc., Statistical Package for Social Sciences, versão 16.0, Chicago, IL, EUA). O valor de alfa adotado foi de 0,05.
Os gráficos para mediana e intervalo de confiança foram feitos com o MedCalc 16.4.3 (MedCalc Software bvba, Ostend, Bélgica; https://www.medcalc.org, 2016).
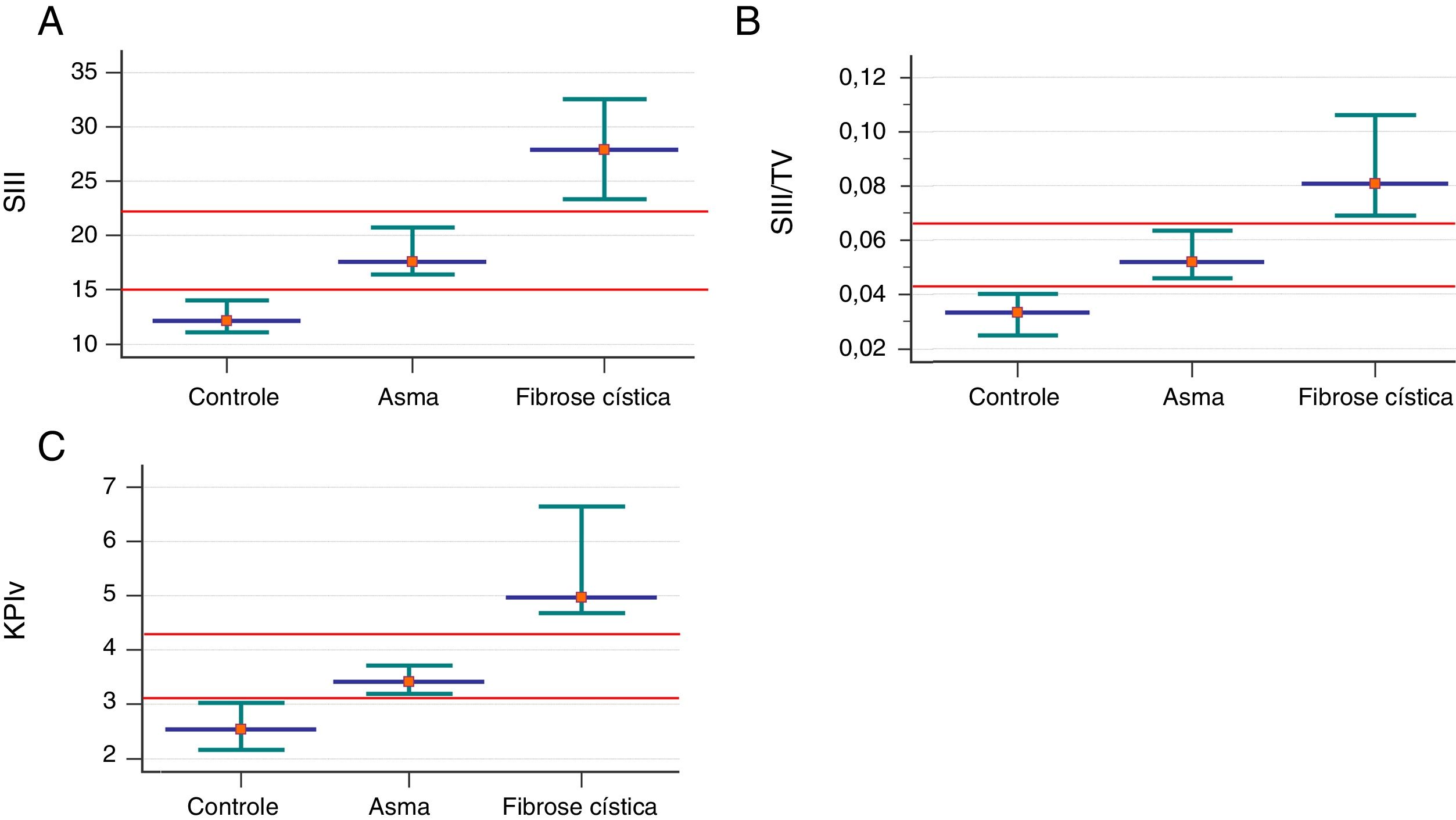
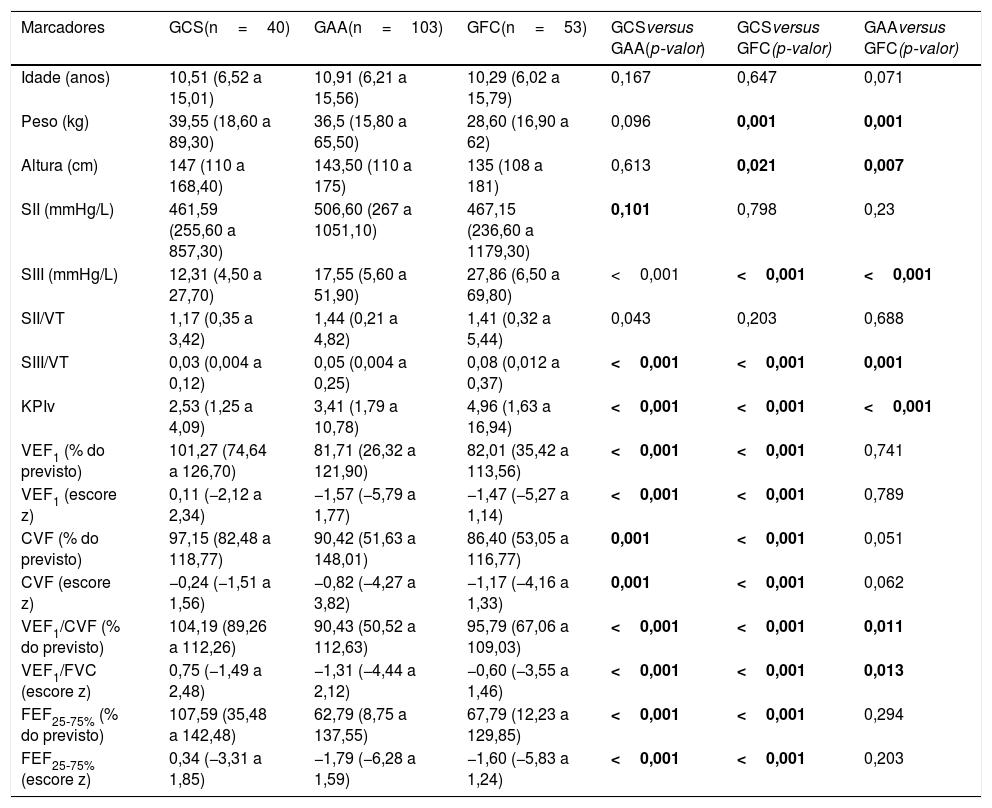
ResultadosA análise descritiva das variáveis antropométricas e os dados obtidos da CapV e da espirometria entre GAA, GFC e GCS são apresentados na tabela 1 e na figura 1. Os pacientes com FC apresentam menor estatura e peso em relação aos controles saudáveis e aos pacientes com asma. O SIII, SIII / VT e KPIv foram maiores nos grupos de doenças respiratórias em relação ao grupo controle, foram piores no GFC. Apenas a VEF1/CVF apresentou o mesmo grau de evidência (p‐valor<0,05), com os menores valores observados no GAA. Com exceção do SII, os demais marcadores da CapV e todos os marcadores da espirometria diferenciaram o GCS do GAA e o GFC (p<0,05).
Associação de variáveis antropométricas e dados obtidos através da capnografia volumétrica e da espirometria entre o grupo controle saudável (GCS) e pacientes com asma alérgica (GAA) ou fibrose cística (GFC)
| Marcadores | GCS(n=40) | GAA(n=103) | GFC(n=53) | GCSversus GAA(p‐valor) | GCSversus GFC(p‐valor) | GAAversus GFC(p‐valor) |
|---|---|---|---|---|---|---|
| Idade (anos) | 10,51 (6,52 a 15,01) | 10,91 (6,21 a 15,56) | 10,29 (6,02 a 15,79) | 0,167 | 0,647 | 0,071 |
| Peso (kg) | 39,55 (18,60 a 89,30) | 36,5 (15,80 a 65,50) | 28,60 (16,90 a 62) | 0,096 | 0,001 | 0,001 |
| Altura (cm) | 147 (110 a 168,40) | 143,50 (110 a 175) | 135 (108 a 181) | 0,613 | 0,021 | 0,007 |
| SII (mmHg/L) | 461,59 (255,60 a 857,30) | 506,60 (267 a 1051,10) | 467,15 (236,60 a 1179,30) | 0,101 | 0,798 | 0,23 |
| SIII (mmHg/L) | 12,31 (4,50 a 27,70) | 17,55 (5,60 a 51,90) | 27,86 (6,50 a 69,80) | <0,001 | <0,001 | <0,001 |
| SII/VT | 1,17 (0,35 a 3,42) | 1,44 (0,21 a 4,82) | 1,41 (0,32 a 5,44) | 0,043 | 0,203 | 0,688 |
| SIII/VT | 0,03 (0,004 a 0,12) | 0,05 (0,004 a 0,25) | 0,08 (0,012 a 0,37) | <0,001 | <0,001 | 0,001 |
| KPIv | 2,53 (1,25 a 4,09) | 3,41 (1,79 a 10,78) | 4,96 (1,63 a 16,94) | <0,001 | <0,001 | <0,001 |
| VEF1 (% do previsto) | 101,27 (74,64 a 126,70) | 81,71 (26,32 a 121,90) | 82,01 (35,42 a 113,56) | <0,001 | <0,001 | 0,741 |
| VEF1 (escore z) | 0,11 (−2,12 a 2,34) | −1,57 (−5,79 a 1,77) | −1,47 (−5,27 a 1,14) | <0,001 | <0,001 | 0,789 |
| CVF (% do previsto) | 97,15 (82,48 a 118,77) | 90,42 (51,63 a 148,01) | 86,40 (53,05 a 116,77) | 0,001 | <0,001 | 0,051 |
| CVF (escore z) | −0,24 (−1,51 a 1,56) | −0,82 (−4,27 a 3,82) | −1,17 (−4,16 a 1,33) | 0,001 | <0,001 | 0,062 |
| VEF1/CVF (% do previsto) | 104,19 (89,26 a 112,26) | 90,43 (50,52 a 112,63) | 95,79 (67,06 a 109,03) | <0,001 | <0,001 | 0,011 |
| VEF1/FVC (escore z) | 0,75 (−1,49 a 2,48) | −1,31 (−4,44 a 2,12) | −0,60 (−3,55 a 1,46) | <0,001 | <0,001 | 0,013 |
| FEF25‐75% (% do previsto) | 107,59 (35,48 a 142,48) | 62,79 (8,75 a 137,55) | 67,79 (12,23 a 129,85) | <0,001 | <0,001 | 0,294 |
| FEF25‐75% (escore z) | 0,34 (−3,31 a 1,85) | −1,79 (−6,28 a 1,59) | −1,60 (−5,83 a 1,24) | <0,001 | <0,001 | 0,203 |
| Indivíduos com valores normais na espirometria | ||||||
|---|---|---|---|---|---|---|
| Marcadores | GCS(n=39) | GAA(n=57) | GFC(n=28) | GCSversus GAA(p‐valor) | GCSversus GFC(p‐valor) | GAAversus GFC(p‐valor) |
| SIII (mmHg/L) | 12,31 (4,53 a 27,73) | 16,88 (6,78 a 37,85) | 21,77 (6,46 a 56,82) | <0,001 | <0,001 | 0,065 |
| SIII/TV | 0,03 (0,004 a 0,13) | 0,05 (0,01 a 0,18) | 0,08 (0,01 a 0,32) | <0,001 | 0,001 | 0,350 |
| KPIv | 2,55 (1,25 a 4,09) | 3,14 (1,79 a 10,78) | 4,47 (1,63 a 14,33) | 0,002 | <0,001 | 0,003 |
| VEF1 (% do previsto) | 101,41 (84,27 a 126,70) | 90,93 (80,23 a 121,90) | 92,78 (80,65 a 113,56) | <0,001 | 0,003 | 0,779 |
| FEV1 (escore z) | 0,13 (−1,30 a 2,34) | −0,75 (−1,67 a 1,77) | −0,61 (−1,67 a 1,14) | <0,001 | 0,003 | 0,793 |
| FVC (% do previsto) | 97,25 (82,48 a 118,77) | 95,79 (80,14 a 148,01) | 92,15 (81,70 a 112,46) | 0,389 | 0,069 | 0,266 |
| FVC (escore z) | −0,23 (−1,51 a 1,56) | −0,37 (−1,65 a 3,82) | −0,67 (−1,57 a 1) | 0,389 | 0,071 | 0,282 |
| FEV1/FVC (% do previsto) | 104,31 (90,67 a 112,26) | 95,23 (80,58 a 112,63) | 99,67 (90,30 a 109,03) | <0,001 | 0,005 | 0,006 |
| FEV1/FVC (escore z) | 0,77 (−1,27 a 2,48) | −0,69 (−2,32 a 2,12) | −0,06 (−1,37 a 1,46) | <0,001 | 0,005 | 0,007 |
| FEF25‐75% (% do previsto) | 108,20 (63,49 a 142,48) | 82,61 (63,28 a 135,56) | 90,56 (72,94 a 129,85) | <0,001 | 0,221 | 0,081 |
| FEF25‐75% (escore z) | 0,35 (−1,64 a 1,85) | −0,78 (−1,64 a 1,59) | −0,42 (−1,19 a 1,24) | <0,001 | 0,204 | 0,069 |
| Área sob a curva para capnografia volumétrica e espirometria entre grupo controle saudável (GCS) (n=40), grupo de pacientes com asma alérgica (GAA) (n=103) e grupo de pacientes com fibrose cística (GFC) (n=53). | ||||||
|---|---|---|---|---|---|---|
| Marcadores | GCS versus GAA | GCS versus GFC | GAA versus GFC | GCSversus GAA (p‐valor) | GCSversus GFC(p‐valor) | AAGversus GFC(p‐valor) |
| SIII (mmHg/L) | 0,782a | 0,899a | 0,722a | <0,001 | <0,001 | <0,001 |
| SIII/TV | 0,732a | 0,831a | 0,660a | <0,001 | <0,001 | 0,001 |
| KPIv | 0,737a | 0,927a | 0,763a | <0,001 | <0,001 | <0,001 |
| FEV1 (% do previsto) | 0,836b | 0,836b | 0,516b | <0,001 | <0,001 | 0,741 |
| FEV1 (escore z) | 0,839b | 0,838b | 0,513b | <0,001 | <0,001 | 0,789 |
| FVC (% do previsto) | 0,685b | 0,756b | 0,596b | 0,001 | <0,001 | 0,051 |
| FVC (escore z) | 0,686b | 0,754b | 0,591b | 0,001 | <0,001 | 0,062 |
| FEV1/FVC (% do previsto) | 0,863b | 0,799b | 0,624a | <0,001 | <0,001 | 0,011 |
| FEV1/FVC (escore z) | 0,864b | 0,800b | 0,622a | <0,001 | <0,001 | 0,013 |
| FEF25‐75% (% do previsto) | 0,839b | 0,778b | 0,551a | <0,001 | <0,001 | 0,294 |
| FEF25‐75% (escore z) | 0,843b | 0,780b | 0,562a | <0,001 | <0,001 | 0,203 |
| Pacientes com espirometria normal. GCS (n=39), GAA (n=57) e GFC (n=28). | ||||||
|---|---|---|---|---|---|---|
| Markers | GCS versus AAG | GCS versus GFC | AAG versus GFC | GCS versus AAG (p‐valor) | GCS versus GFC(p‐valor) | AAG versus GFC(p‐valor) |
| SIII (mmHg/L) | 0,768a | 0,822a | 0,623a | <0,001 | <0,001 | 0,065 |
| SIII/TV | 0,730a | 0,742a | 0,563a | <0,001 | 0,001 | 0,350 |
| KPIv | 0,686a | 0,866a | 0,702a | 0,002 | <0,001 | 0,003 |
| VEF1 (% do previsto) | 0,726b | 0,712b | 0,519b | <0,001 | 0,003 | 0,779 |
| VEF1 (escore z) | 0,732b | 0,717b | 0,518b | <0,001 | 0,003 | 0,793 |
| CVF (% do previsto) | 0,552b | 0,631b | 0,575b | 0,389 | 0,069 | 0,266 |
| CVF (escore z) | 0,552b | 0,630b | 0,572b | 0,389 | 0,071 | 0,282 |
| FEV1/FVC (% do previsto) | 0,814b | 0,702b | 0,683a | <0,001 | 0,005 | 0,006 |
| FEV1/FVC (escore z) | 0,815b | 0,701b | 0,681a | <0,001 | 0,005 | 0,007 |
| FEF25‐75% (% do previsto) | 0,740b | 0,596b | 0,634a | <0,001 | 0,221 | 0,081 |
| FEF25‐75% (escore z) | 0,745b | 0,600b | 0,640a | <0,001 | 0,204 | 0,069 |
Cm, centímetro; CVF, capacidade vital forçada; FEF25‐75%, fluxo expiratório forçado de 25% a 75% da CVF; Kg, quilograma; KPIv, razão entre o SII e o SIII multiplicado por 100; L, litros; mL, mililitros; mmHg, milímetros de mercúrio; SII, slope da fase II; SIII, slope da fase III; VEF1, volume expiratório forçado no primeiro segundo da CVF; VT, volume tidal exalado.
Os dados são apresentados pela mediana (mínimo a máximo). A análise estatística foi feita com o teste de Mann‐Whitney e comparamos dois grupos de cada vez. Alfa=0,05. Valores de p com associação positiva são apresentados em negrito. A área sob a curva foi medida pela curva ROC.
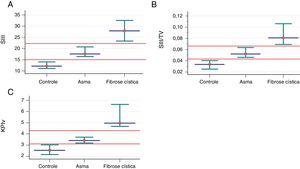
Associação dos parâmetros mensurados na capnografia volumétrica e espirometria entre indivíduos controles saudáveis (n=40) e pacientes com asma alérgica (n=103) e fibrose cística (n=53). Os dados são apresentados pela mediana (ponto vermelho) e intervalo de confiança de 95% (intersecção verde). A. SIII (controle saudável) 12,08; (asma) 17,55; (fibrose cística ‐ GFC) 27,86. B. SIII /VT: SIII: (controle saudável) 0,03; (asma) 0,05; (GFC) 0,08. C. KPIv: (controle saudável) 2,53; (asma) 3,41; (GFC) 4,96. Os dados são apresentados pela mediana. Alfa=0,05. Todos os dados apresentaram valor de p com associação positiva. O SII e SIII são apresentados em mmHg, milímetros de mercúrio. A análise estatística foi feita pelo teste de Mann‐Whitney e comparamos dois grupos de cada vez. mmHg, milímetros de mercúrio; L, litros; VT, volume tidal exalado; SII, slope da fase II; SIII, slope da fase III; KPIv, razão entre o SII e SIII multiplicada por 100.
A análise dos indivíduos com espirometria normal evidenciou que todos os marcadores, com exceção da CVF, eram diferentes entre o GCS e os pacientes (GAA e GFC). No entanto, apenas os valores do KPIv (maior no GFC) e razão VEF1/CVF (menor no GAA) foram diferentes entre o GAA e o GFC.
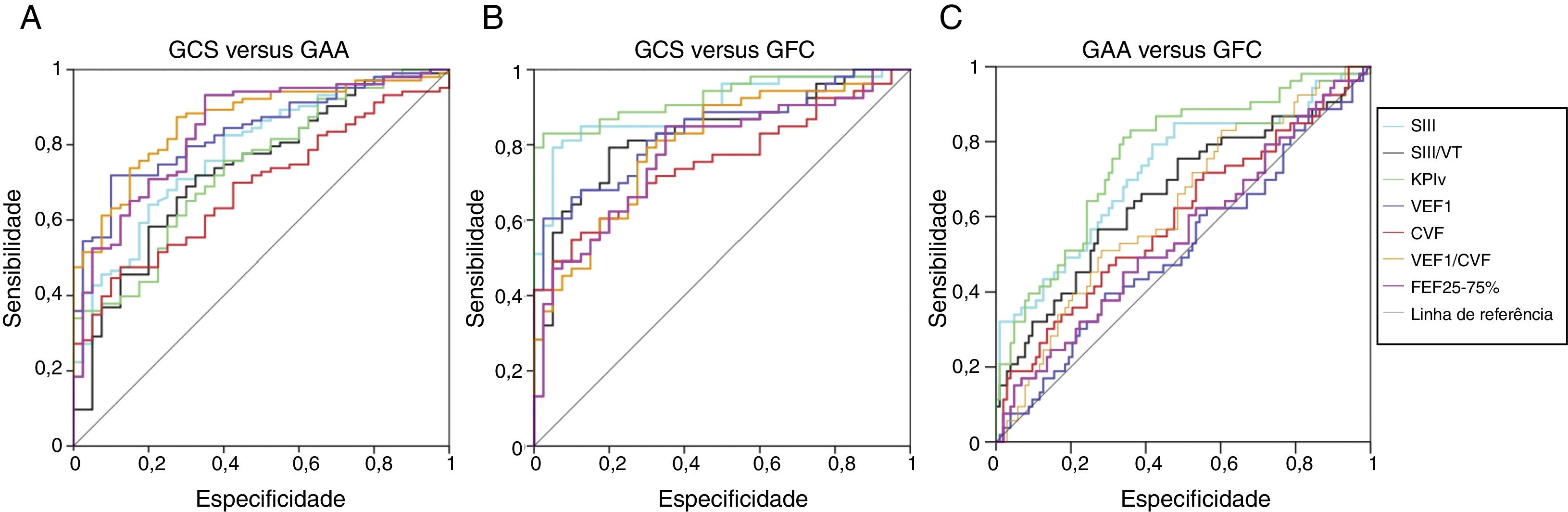
A AUC para a CapV e a espirometria entre o GCS e os pacientes (GAA e GFC), assim como entre o GAA e o GFC, são apresentadas na tabela 1 e na figura 2. Sobre a diferenciação do GCS do GAA, os marcadores foram diferentes (valor de p<0,05); entretanto, apenas o VEF1 e o VEF1/CVF apresentaram valores de AUC superiores a 0,800.
Área sob a curva para capnografia volumétrica e espirometria entre o grupo controle (GCS, n=40), o grupo de pacientes com asma alérgica (GAA, n=103) e grupo de pacientes com fibrose cística (GFC, n=53). VT, volume tidal exalado; SIII, slope da fase III; KPIv, razão entre o SII e SIII multiplicada por 100; VEF1, volume expiratório forçado no primeiro segundo da CVF; CVF, capacidade vital forçada; FEF 25‐75%, fluxo expiratório forçado de 25% a 75% da CVF.
Na discriminação entre os grupos GCS e o GFC, os marcadores apresentaram diferenças entre os grupos (p‐valor<0,05), com o maior valor de AUC para os marcadores VEF1/CVF e CapV, com o maior valor de AUC para KPIv (0,900). Da mesma forma, os marcadores CapV e VEF1/CVF diferenciaram entre o GAA e o GFC e o KPIv apresentou o maior valor de AUC (0,763).
Quando os indivíduos com espirometria normal foram avaliados, o CapV apresentou valores de AUC capazes de diferenciar o GCS do GAA (SIII=0,768, p‐valor<0,001; SIII / VT=0,730, p‐valor <0,001; KPIv=0,686, p‐valor=0,002); bem como o GCS do GFC (KPIv=0,866, p‐valor <0,001; SIII=0,822, p‐valor <0,001; SIII / VT=742, p‐valor=0,001). As AUCs que diferenciaram o GCS do GAA na espirometria foram: VEF1/CVF (% do previsto)=0,814 (p <0,001) e VEF1 (% do previsto)=0,726 (p‐valor <0,001). Entre o GCS e o GFC, os valores de VEF1 e VEF1 / CVF (% do previsto) foram diferentes (valor de p <0,05) (AUC=0,712 e 0,702, respectivamente).
A discriminação do GAA do GFC, em indivíduos com espirometria normal, foi feita pelo KPIv (AUC=0,702, p‐valor=0,003) e VEF1/CVF (%) (AUC=0,683, p‐valor=0,006).
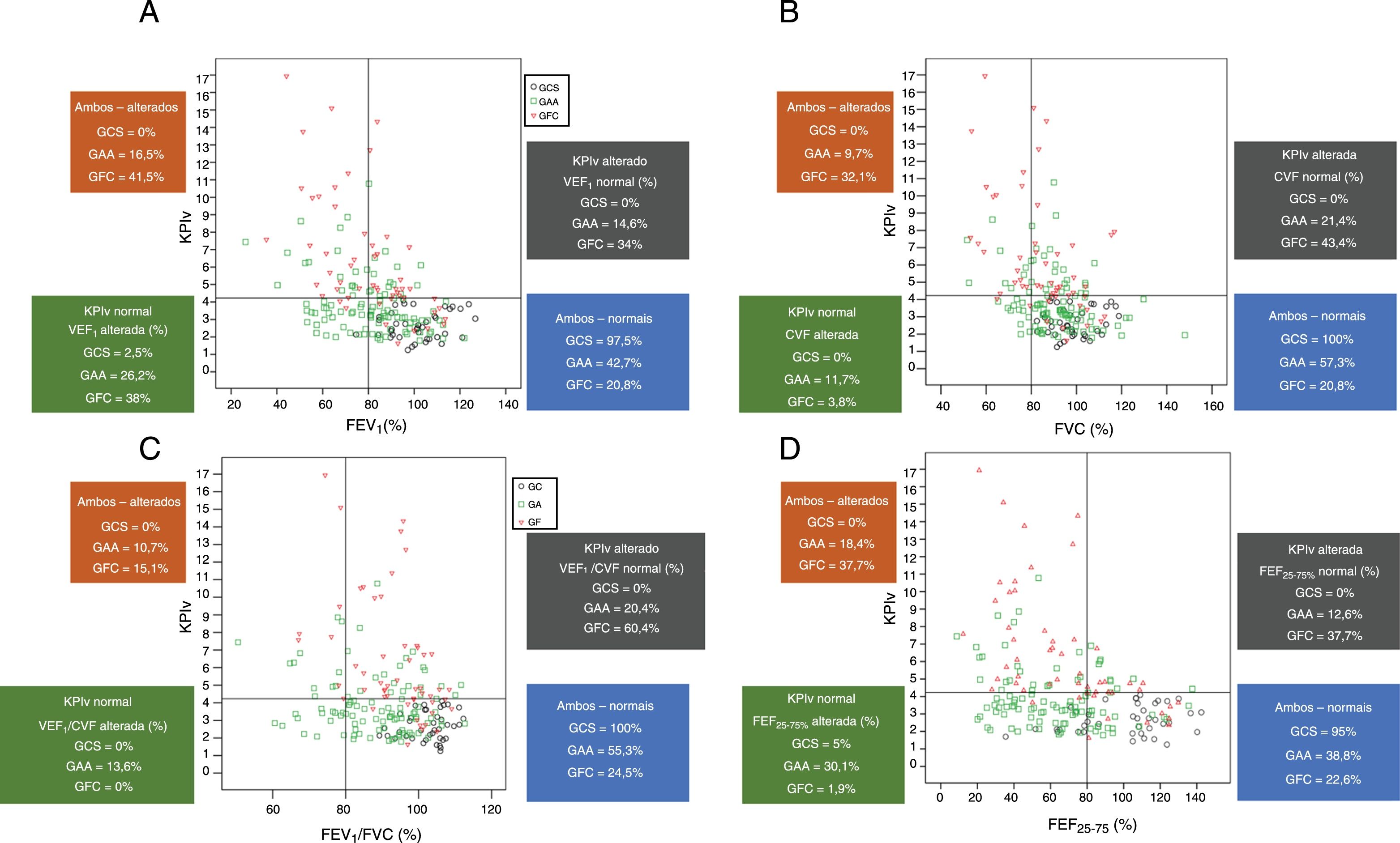
A figura 3 apresenta a relação entre os marcadores de espirometria e KPIv nos três grupos estudados.
Associação do KPIv na capnografia volumétrica com marcadores espirométricos entre indivíduos controles saudáveis (n=40) e pacientes com asma alérgica (n=103) ou fibrose cística (n=53), considerando a distinção entre marcadores espirométricos acima e abaixo do LIN (80%) e KPIv acima e abaixo do LSN (KPIv=4,23). A. KPIv versus VEF1 (% do previsto). B. KPIv versus CVF (% prevista). C. KPIv versus VEF1/CVF (% do previsto). D. KPIv versus FEF25‐75% (% do previsto). Cada gráfico é dividido em quatro quadrantes correspondentes às seguintes condições: KPIv e marcador de espirometria alterados; KPIv alterado e marcador de espirometria normal; KPIv normal e marcador de espirometria alterado; KPIv e marcador de espirometria normais. KPIv, razão entre o SII e SIII multiplicada por 100; VEF1, volume expiratório forçado no primeiro segundo da CVF; CVF, capacidade vital forçada; FEF 25‐75%, fluxo expiratório forçado entre 25% a 75% da CVF; LIN, Limite Inferior do Normal; LSN, Limite Superior do Normal. Círculo preto, indivíduos controles saudáveis; círculo verde, pacientes com asma; triângulo vermelho, pacientes com fibrose cística.
Os autores do presente estudo não conhecem outros que avaliem a capacidade dos marcadores da CapV de discriminar indivíduos com asma de indivíduos com FC e controles saudáveis, em comparação com os marcadores espirométricos. Além disso, um achado sem precedentes e substancial foi que SIII, SIII/VT e KPIv eram diferentes entre os três grupos avaliados, com maiores valores para FC. O VEF1/CVF foi o único marcador de espirometria a mostrar diferença nos três grupos. Além disso, em indivíduos com espirometria normal, o KPIv e VEF1/CVF foram diferentes entre os três grupos. Além disso, a curva ROC diferenciou os indivíduos com asma ou FC do grupo controle, tanto por meio da CapV (melhor para identificar FC em relação ao grupo controle com o uso do KPIv) quanto através da espirometria (melhor para diferenciar a asma do grupo controle). O KPIv foi o melhor parâmetro para distinguir a asma da FC, mesmo em indivíduos com espirometria normal.
A busca de métodos para avaliar a função pulmonar em crianças e adolescentes com doenças pulmonares crônicas e obstrução das vias aéreas é uma constante luta na comunidade científica. A espirometria é o instrumento mais usado para ensaios clínicos randomizados como desfecho primário.19–22 No entanto, o uso da espirometria sempre será criticado, apesar de sua importância, principalmente pela grande variabilidade intrapessoal e pela falta de equações para populações distintas. Portanto, comparar a espirometria com outros métodos é promissor.
Crianças apresentam várias doenças pulmonares crônicas com obstrução das vias aéreas e cada uma delas apresenta maior ou menor grau de inflamação e reatividade brônquica nas vias aéreas superiores e/ou inferiores.1
Cada instrumento de avaliação provavelmente terá maior ou menor eficácia, depende das doenças pulmonares crônicas, como mostra a figura 3 para a CapV e a espirometria. A busca pela caracterização da utilidade desses métodos tem como foco encontrar alterações anatômicas (tomografia computadorizada do tórax) e funcionais [espirometria, sistema de oscilometria de impulso, índice de clearance pulmonar (ICP), pletismografia, entre outros]. Em relação às doenças incluídas em nosso estudo, a asma difere da FC, considera‐se a predominância inicial de obstrução, manutenção e progressão da obstrução fixa das vias aéreas. A asma afeta as grandes vias aéreas e, se não for tratada, cresce nas pequenas vias aéreas.23 Por outro lado, o oposto acontece na FC: a doença começa nas pequenas vias aéreas e cresce nas grandes vias aéreas.24 Esses achados são ilustrados pelos nossos dados (fig. 3).
Os slopes da CapV avaliam a parte volumétrica das vias aéreas, onde ocorre o movimento dos gases por difusão. A espirometria, por outro lado, avalia melhor as alterações do fluxo nas vias aéreas condutoras – o movimento de gases nessa região é mais intenso devido à convecção. Portanto, era esperado que houvesse diferenças entre os resultados desses instrumentos na avaliação das várias doenças pulmonares crônicas com obstrução das vias aéreas em crianças, decorrentes de comprometimentos nas vias aéreas proximais ou distais.
Gustafsson et al. compararam asma e FC com o uso de ICP e espirometria; nossos resultados e os resultados do autor sugerem que as alterações das vias aéreas na FC afetam a periferia pulmonar de forma mais extensivamente do que na asma.25 Também, Fuchs et al. apresentaram associação entre o KPIv da CapV e ICP.9 De acordo com nossos dados, as diferenças entre a espirometria e a CapV no GCS, GAA e GFC ocorreram e observamos a presença de espirometria e KPIv concomitantemente alterados no GFC. Além disso, espirometria normal ocorreu no GFC e GAA (bem como no GCS). Vários pacientes com FC e espirometria normal apresentaram KPIv alterado, sugeriu‐se que as alterações avaliadas pela CapV podem ocorrer mais precocemente do que na espirometria e esse fato foi anteriormente documentado para outros marcadores de CapV e ICP.13,26 Um comportamento similar ocorreu entre o ICP e o VEF1 na FC.27 Por outro lado, pacientes com asma podem apresentar espirometria alterada com KPIv normal, sugeriu‐se que as alterações de fluxo são mais frequentes e afetam as vias aéreas proximais. Pacientes com asma que apresentam espirometria normal e KPIv alterado seriam mais difíceis de explicar. Esses indivíduos poderiam constituir fenótipos menos conhecidos e que merecem estudo com biomarcadores funcionais e inflamatórios para caracterizar o tipo de asma.
Para destacar a importância da CapV na avaliação das doenças pulmonares versus a espirometria, usamos a curva ROC para discriminar os diferentes grupos. De acordo com nossos dados, a CapV provou ser um instrumento útil para diferenciar pacientes com FC de controles saudáveis, tanto em adultos quanto em crianças6,13 e para diferenciar crianças, adolescentes e adultos com asma de indivíduos saudáveis.10,28
Os marcadores espirométricos (VEF1 e VEF1/CVF) foram melhores do que os marcadores da CapV para diferenciar o GAA e o GCS na curva ROC. Por outro lado, os marcadores da CapV apresentam uma maior AUC para distinguir entre o GFC e o GCS. O’Neal et al. encontraram uma maior AUC com ICP do que com a espirometria, para diferenciar a FC e os controles saudáveis.18 A espirometria e a CapV foram eficazes para diferenciar indivíduos saudáveis de pacientes com doença pulmonar. Na diferença entre GAA e GFC, apenas KPIv e VEF1 /CFC foram significativos, o KPIv foi maior (AUC <0,700).
Ao avaliar os indivíduos com espirometria normal, os marcadores CapV apresentaram maior comprometimento da homogeneidade da ventilação no GFC e no GAA em relação ao grupo controle. No entanto, a CapV foi melhor do que a espirometria para diferenciar o GCS do GFC. Nessa situação, a CapV também foi melhor do que a espirometria para discriminar entre a GFC e o GAA, considerou‐se uma AUC ≥ 0,700.
Nosso estudo apresentou algumas limitações: (i) o fato de não ser prospectivo e não ter medidas repetidas de CapV; (ii) a CapV é limitada para avaliar propriedades clinimétricas e isso não altera nossa percepção do potencial da CapV como instrumento clínico e científico no contexto de doenças pulmonares em pediatria; (iii) tamanho da amostra de conveniência; (iv) apenas um centro foi incluído para lidar com uma determinada população.
Em conclusão, nosso estudo mostrou que o SIII, SIII/VT e KPIv da VCap e o VEF1 e VEF1/CVF da espirometria foram bons marcadores para discriminar o GCS dos grupos GAA e GFC. Acreditamos que para cada doença pulmonar crônica com obstrução das vias aéreas, diferentes marcadores de deterioração da função pulmonar serão mais úteis. Finalmente, a CapV pode descrever mais precocemente e com maior precisão a fisiopatologia da FC do que a espirometria.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
FALM: Fundação de Amparo à Pesquisa do Estado de São Paulo (Fapesp) para apoio à pesquisa #2011/12939‐4, #2011/18845‐1, #2015/12183‐8 and #2015/12858‐5; Fundo de Apoio à Pesquisa, ao Ensino e à Extensão da Universidade Estadual de Campinas para apoio à pesquisa #0648/2015; JDR: Fapesp para o apoio #2011/18845‐1 # e #2015/12183‐8.
A Luciana Montes Rezende, Luciana Cardoso Bonadia, Maria de Fátima Corrêa Pimenta Servidoni, Carlos Emílio Levy, Adressa Oliveira Peixoto, Adyléia Aparecida Contrera Dalbo Toro, Renan Marrichi Mauch, Roberto José Negrão Nogueira, Eulália Sakano, Antônio Fernando Ribeiro, Carla Cristina de Souza Gomez, Elizete Aparecida Lomazi, Paloma Lopes Francisco Parazzi, Larissa Lazzarini Furlan, Emília da Silva Gonçalves, Aline Cristina Gonçalves, Milena Baptistella Grotta Silva e Alethea Guimarães Faria, que contribuem para estudos feitos em fibrose cística em nosso centro de referência.
Como citar este artigo: Almeida‐Junior A, Marson FA, Almeida CC, Ribeiro MÂ, Paschoal IA, Moreira MM, et al. Volumetric capnography versus spirometry for the evaluation of pulmonary function in cystic fibrosis and allergic asthma. J Pediatr (Rio J). 2020;96:255–63.
O estudo foi realizado no Laboratório de Fisiologia Pulmonar (Lafip), Centro de Investigação em Pediatria (Ciped), Faculdade de Ciências Médicas, Universidade Estadual de Campinas, Campinas, SP, Brasil.