To describe the dietary patterns and occurrence of metabolic disorders in children and adolescents with urolithiasis treatment at a referral hospital in southern Brazil in order to learn the features of urolithiasis in this population to better develop preventive actions.
MethodsDescriptive study conducted between 2016 and 2017 in a tertiary care referral hospital. Fourty patients aged 2–19 years old with urolithiasis proven by imaging were included. Clinical and dietary data were obtained through interviews and medical records. For statistical analyses, the chi‐squared test was performed.
Results40 individuals were analyzed. Mean age at diagnosis was 7.2±4 years. 25% were overweight or obese. 95% had metabolic disorders, hypocitraturia being the predominant type. Protein intake was adequate in all participants and carbohydrate intake, in 70% of them; 37.5% had lipid intake above recommended and 65% had low fiber intake. The mean daily sodium intake was 2.64g (±1.74), with 55% of participants ingesting more than the recommended amount. A total of 52.5% had low potassium intake, with a mean of 4.79g/day (±2.49). Calcium intake was adequate in 27.5%. No significant differences were identified in relation to mean daily consumption among participants with or without the various metabolic disorders.
ConclusionPediatric urolithiasis is often accompanied by metabolic disorders; therefore, metabolic evaluation should be part of the diagnostic process and subsequent analysis of these patients’ dietary patterns, helping to optimize treatment and prevent recurrences and complications.
Descrever o padrão alimentar e a ocorrência de distúrbios metabólicos em crianças e adolescentes portadoras de urolitíase acompanhadas em hospital de referências no sul do Brasil a fim de conhecer as particularidades da urolitíase nessa população para melhor desenvolver ações de prevenção.
MétodosEstudo observacional descritivo realizado entre 2016 e 2017 em centro de referência em atenção terciária. Foram selecionados 40 pacientes de dois a 19 anos com urolitíase comprovada por exame de imagem. Dados clínicos e alimentares foram obtidos através de prontuário e entrevista. Para análise estatística, utilizou-se o teste qui‐quadrado.
ResultadosForam analisados 40 indivíduos, 55% masculinos. Idade média ao diagnóstico 7,2 ± 4 anos; 25% tinham sobrepeso ou obesidade; 95% tinham distúrbios metabólicos, predominou a hipocitratúria. O consumo proteico e de carboidratos foi adequado em 100% e 70% dos participantes, respectivamente, 37,5% apresentaram ingestão de lipídeos acima do recomendado e 65% apresentaram ingestão de fibras alimentares abaixo do recomendado. O consumo diário médio de sódio foi de 2,64g (± 1,74), com 55% acima do recomendado; 52,5% apresentaram baixa ingestão de potássio com média de 4,79g/dia (± 2,49). O consumo de cálcio foi adequado em 27,5%. Não foram identificadas diferenças significativas em relação ao consumo médio diário dos nutrientes entre os participantes com ou sem os diversos distúrbios metabólicos.
ConclusõesA urolitíase pediátrica é frequentemente acompanhada de distúrbios metabólicos, o que confirma a necessidade de avaliação metabólica adequada ao diagnóstico e análise do padrão alimentar a fim de identificar erros alimentares, aprimorar o tratamento desses distúrbios e prevenir recorrências e complicações.
Ainda que menos frequente nas crianças, a incidência de urolitíase (UL) aumentou significativamente nessa população nas últimas décadas.1 Estudo recente mostrou que o risco de UL duplicou na faixa pediátrica entre 1997 e 2012.2 Atualmente o incremento anual na incidência está entre 5 a 10% para a população infantil.3
Diversos trabalhos têm buscado identificar causas para esse novo panorama epidemiológico. Além dos já clássicos fatores infecciosos e alterações anatômicas do trato urinário, estudos têm demonstrado o papel crucial dos distúrbios metabólicos (DMet) na gênese de aproximadamente 90% da UL pediátrica.1,3 Dentre os DMet mais estudados estão a hipercalciúria, hipocitratúria e hiperuricosúria.3
Existem evidências na literatura da relação entre o desenvolvimento de tais distúrbios e a alimentação, especialmente relacionadas à baixa ingestão de água, potássio e cálcio, bem como dietas ricas em proteína animal e sódio.1,4 Estudos recentes sugerem associação entre UL e obesidade em pacientes adultos.4 Entretanto, para a população infantil ainda não existem evidências dessa relação.4,5
Diante do panorama atual da UL pediátrica, o presente estudo teve como objetivo descrever o padrão alimentar em crianças com UL acompanhadas em um hospital de referência no sul do Brasil, buscou identificar possíveis alterações nutricionais relacionadas ao desenvolvimento dos DMet associados a fim de conhecer as particularidades da urolitíase nessa população para melhor desenvolver ações de prevenção.
MétodosEstudo observacional descritivo do qual participaram pacientes acompanhados no ambulatório de Nefrologia Pediátrica de centro de referência em atenção terciária em pediatria no Estado de Santa Catarina, entre setembro de 2016 e outubro de 2017.
O presente estudo foi aprovado pelo Comitê de Ética em Pesquisas do hospital em estudo (Protocolo 029/2016) e não obteve qualquer apoio financeiro.
Participantes foram selecionados através de amostragem não probabilística. Foram incluídos pacientes de dois a 19 anos completos (faixa etária definida em razão dos questionários de frequência alimentar – QFA)6–8 e que apresentaram diagnóstico de UL confirmado por exame de imagem (ultrassonografia ou tomografia computadorizada).
Os indivíduos, acompanhados de seus responsáveis legais, foram convidados a participar do estudo após consulta ambulatorial de rotina e todos assinaram um Termo de Consentimento Livre e Esclarecido. Foram coletados dados demográficos, clínicos, medidas antropométricas (peso e estatura) e aplicou‐se um QFA quantitativo, validado para a população brasileira, de acordo com a idade do participante.6–8 Diagnóstico de DMet e exames laboratoriais (urinários e séricos) feitos até seis meses antes do atendimento foram coletados do prontuário eletrônico.
Avaliou‐se o estado nutricional através do índice de massa corporal (IMC) e foram usados os gráficos de Padrão de Crescimento Infantil da Organização Mundial da Saúde para a devida classificação do participante.
Na avaliação alimentar foi calculada para cada alimento a quantidade ingerida pelo participante de: proteínas, lipídeos, carboidratos, fibra alimentar, cálcio, magnésio, ferro, sódio e potássio. Para isso, usou‐se a quantidade em medida caseira e a frequência de consumo referidas e foi usada como referência a Tabela Brasileira de Composição de Alimentos (TACO).9 Foram então somados todos os teores de cada nutriente, obteve‐se a ingestão habitual total. Com a finalidade de se conhecer a média diária de ingestão, o total foi então dividido por 30 dias. Esse valor foi classificado de acordo com as recomendações para idade e sexo da Dietary Reference Intakes (DRI).10 Foram tidos como limite inferior e superior de normalidade para ingestão de cada nutriente a Estimated Average Requirement (Necessidade Média Estimada) e o Tolerable Upper Intake Level (Limite Superior Tolerável de Ingestão), respectivamente. Os macronutrientes foram expressos em porcentagem em relação ao valor energético total (VET) diário e os demais nutrientes em grama ou miligrama por dia.10
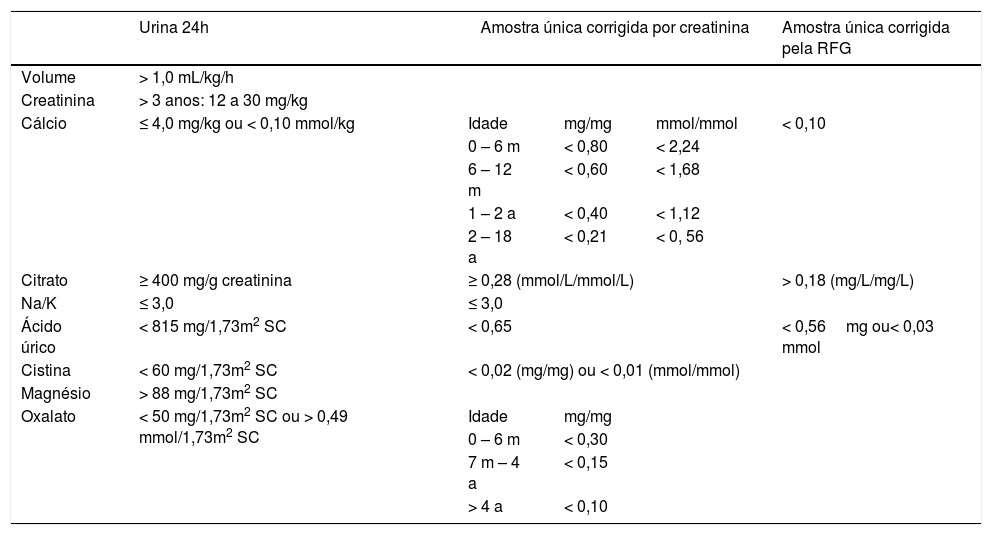
Os diagnósticos de DMet foram fundamentados em valores anormais de urina de 24 horas e/ou amostra urinária única segundo a tabela 1.11–14 Este estudo metabólico ocorreu pelo menos um mês após o diagnóstico de UL, durante período assintomático e padrões habituais de dieta e atividade física. Foram usados os ensaios bioquímicos padrão adotados no laboratório do hospital em estudo para análise das amostras urinárias.
Valores de referência para volume e excreção de solutos em urina de 24h e amostra urinária em crianças e adolescentes11–14
| Urina 24h | Amostra única corrigida por creatinina | Amostra única corrigida pela RFG | |||
|---|---|---|---|---|---|
| Volume | > 1,0 mL/kg/h | ||||
| Creatinina | > 3 anos: 12 a 30 mg/kg | ||||
| Cálcio | ≤ 4,0 mg/kg ou < 0,10 mmol/kg | Idade | mg/mg | mmol/mmol | < 0,10 |
| 0 – 6 m | < 0,80 | < 2,24 | |||
| 6 – 12 m | < 0,60 | < 1,68 | |||
| 1 – 2 a | < 0,40 | < 1,12 | |||
| 2 – 18 a | < 0,21 | < 0, 56 | |||
| Citrato | ≥ 400 mg/g creatinina | ≥ 0,28 (mmol/L/mmol/L) | > 0,18 (mg/L/mg/L) | ||
| Na/K | ≤ 3,0 | ≤ 3,0 | |||
| Ácido úrico | < 815 mg/1,73m2 SC | < 0,65 | < 0,56mg ou< 0,03 mmol | ||
| Cistina | < 60 mg/1,73m2 SC | < 0,02 (mg/mg) ou < 0,01 (mmol/mmol) | |||
| Magnésio | > 88 mg/1,73m2 SC | ||||
| Oxalato | < 50 mg/1,73m2 SC ou > 0,49 mmol/1,73m2 SC | Idade | mg/mg | ||
| 0 – 6 m | < 0,30 | ||||
| 7 m – 4 a | < 0,15 | ||||
| > 4 a | < 0,10 | ||||
RFG, ritmo de filtração glomerular; SC, superfície corporal.
Os dados coletados foram registrados em banco de dados no programa Excel® 2007. A análise estatística foi feita com o programa Epi Info versão 7.2. As variáveis nominais foram descritas em números absolutos e proporções, já as variáveis categóricas, em medidas de tendência central e de dispersão. Para comparação das variáveis qualitativas foi usado o teste qui‐quadrado, para o qual foi adotado o nível de significância de 95% (p < 0,05).
ResultadosDos 41 pacientes selecionados, um não concordou em participar, restaram 40.
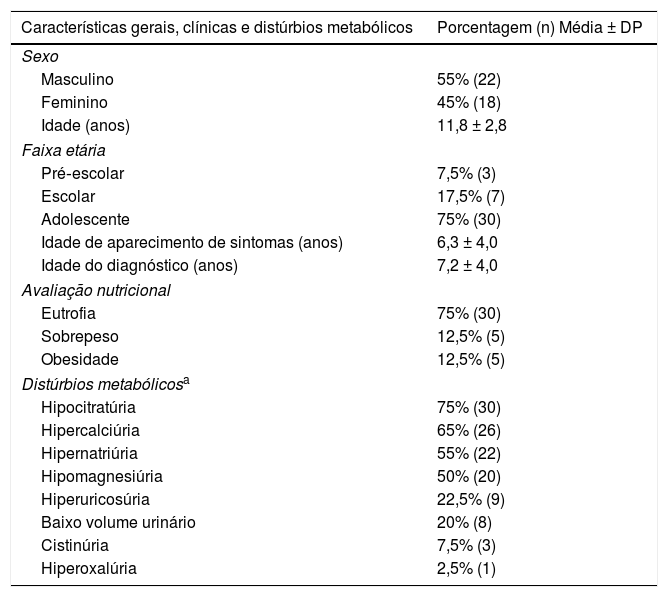
A tabela 2 apresenta as características gerais, os dados demográficos e clínicos dos participantes.
Características gerais, clínicas e distúrbios metabólicos das crianças e adolescentes com diagnóstico de urolitíase
| Características gerais, clínicas e distúrbios metabólicos | Porcentagem (n) Média ± DP |
|---|---|
| Sexo | |
| Masculino | 55% (22) |
| Feminino | 45% (18) |
| Idade (anos) | 11,8 ± 2,8 |
| Faixa etária | |
| Pré‐escolar | 7,5% (3) |
| Escolar | 17,5% (7) |
| Adolescente | 75% (30) |
| Idade de aparecimento de sintomas (anos) | 6,3 ± 4,0 |
| Idade do diagnóstico (anos) | 7,2 ± 4,0 |
| Avaliação nutricional | |
| Eutrofia | 75% (30) |
| Sobrepeso | 12,5% (5) |
| Obesidade | 12,5% (5) |
| Distúrbios metabólicosa | |
| Hipocitratúria | 75% (30) |
| Hipercalciúria | 65% (26) |
| Hipernatriúria | 55% (22) |
| Hipomagnesiúria | 50% (20) |
| Hiperuricosúria | 22,5% (9) |
| Baixo volume urinário | 20% (8) |
| Cistinúria | 7,5% (3) |
| Hiperoxalúria | 2,5% (1) |
DP, desvio‐padrão; n, número de participantes.
Dos 38 participantes (95%) que fizeram exames laboratoriais para avaliação de alteração metabólica, todos apresentavam pelo menos um DMet, tiveram exames séricos metabólicos dentro dos valores de normalidade do laboratório local. A frequência de ocorrência dos DMet é apresentada na tabela 2.
Na avaliação nutricional observou‐se que todos os pré‐escolares, seis escolares (85,7%) e 21 adolescentes (70%) eram eutróficos. Entre os participantes com sobrepeso, quatro eram adolescentes (80%). Dentre os obesos, todos eram adolescentes.
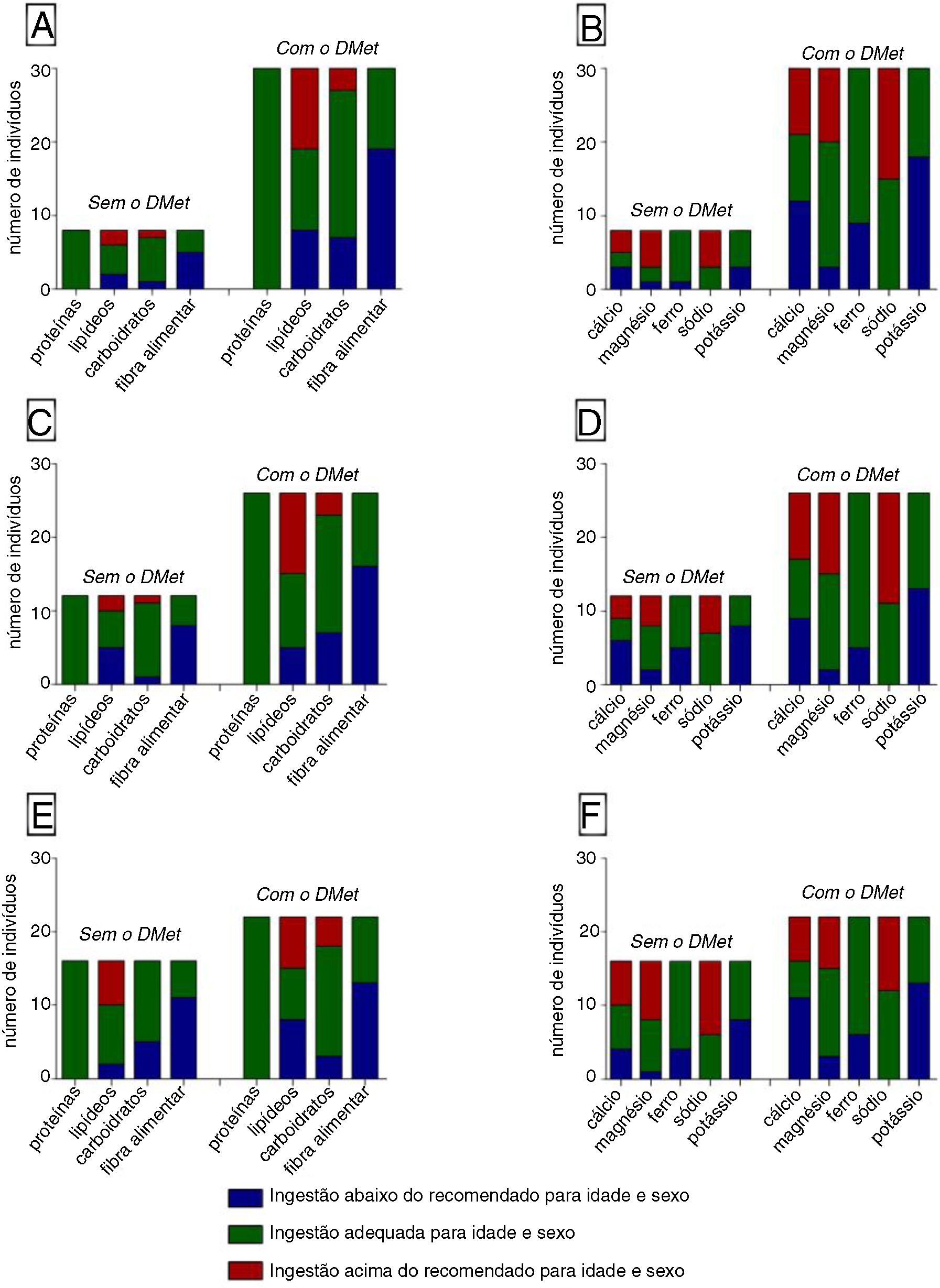
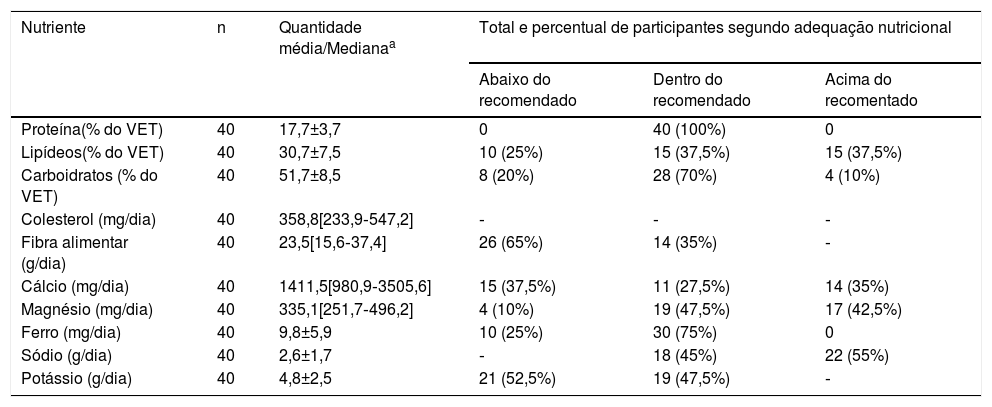
As quantidades médias de consumo de cada nutriente avaliado com base no QFA, bem como o percentual de participantes que apresentavam ingestão média dentro, acima ou abaixo das recomendações para idade e sexo segundo a DRI, estão dispostas na tabela 3.
Consumo e classificação da ingestão dos nutrientes de acordo com as recomendações da DRI para sexo e idade, com base na avaliação do QFA por faixa etária
| Nutriente | n | Quantidade média/Medianaa | Total e percentual de participantes segundo adequação nutricional | ||
|---|---|---|---|---|---|
| Abaixo do recomendado | Dentro do recomendado | Acima do recomentado | |||
| Proteína(% do VET) | 40 | 17,7±3,7 | 0 | 40 (100%) | 0 |
| Lipídeos(% do VET) | 40 | 30,7±7,5 | 10 (25%) | 15 (37,5%) | 15 (37,5%) |
| Carboidratos (% do VET) | 40 | 51,7±8,5 | 8 (20%) | 28 (70%) | 4 (10%) |
| Colesterol (mg/dia) | 40 | 358,8[233,9‐547,2] | ‐ | ‐ | ‐ |
| Fibra alimentar (g/dia) | 40 | 23,5[15,6‐37,4] | 26 (65%) | 14 (35%) | ‐ |
| Cálcio (mg/dia) | 40 | 1411,5[980,9‐3505,6] | 15 (37,5%) | 11 (27,5%) | 14 (35%) |
| Magnésio (mg/dia) | 40 | 335,1[251,7‐496,2] | 4 (10%) | 19 (47,5%) | 17 (42,5%) |
| Ferro (mg/dia) | 40 | 9,8±5,9 | 10 (25%) | 30 (75%) | 0 |
| Sódio (g/dia) | 40 | 2,6±1,7 | ‐ | 18 (45%) | 22 (55%) |
| Potássio (g/dia) | 40 | 4,8±2,5 | 21 (52,5%) | 19 (47,5%) | ‐ |
DRI, Dietary Reference Intakes; QFA, questionário de frequência alimentar; VET, valor energético total.
Valores expressos em média ± desvio‐padrão ou mediana [intervalo interquartil].
a38 pacientes foram submetidos aos testes laboratoriais.
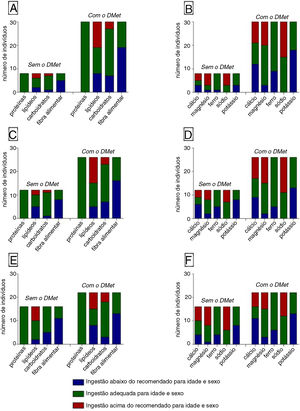
A correlação entre o padrão alimentar e os DMet mais frequentes no presente estudo está representada na figura 1. Não foram identificadas diferenças significativas em relação ao consumo médio diário de cada nutriente na presença ou ausência dos DMet, de acordo com os padrões já expressos anteriormente.
DiscussãoAs evidências atuais mostram aumento na incidência de UL na população pediátrica.3 A associação entre UL e DMet é frequente nessa população e sugere uma participação da alimentação na formação de cálculos urinários.1,3 Apesar de bem estabelecida em adultos,15 a associação entre obesidade e UL ainda é questionada entre crianças e adolescentes,16 o que fomenta uma investigação mais detalhada sobre o padrão alimentar dessa população. Nesse escopo, o presente estudo traz a vantagem de descrever quantitativa e qualitativamente o padrão alimentar de pacientes acompanhados em um centro de referência estadual em nefrologia pediátrica.
Características gerais, dados demográficos, clínicos e de imagemA maioria dos participantes era masculina, correspondia aos achados de outras séries17 (tabela 2). Apesar de ser historicamente mais frequente nesse sexo,1 a incidência de UL na população feminina já se mostra mais prevalente em alguns estudos.1,2,18,19 Entretanto, dados americanos demonstram uma distribuição uniforme entre os sexos.17,18,20 Isso sugere que não há uma relação causal entre esse e ocorrência de UL.
A idade média ao diagnóstico foi 7,2 anos, corroborou com Akin et al.,21 os quais demonstraram que essa idade costuma variar entre 4,2 e 9,4 anos. Em contraste, outros estudos demonstraram uma variação de 11,3 a 11,8 anos, média maior do que a encontrada neste estudo.18,20 Essa menor idade ao diagnóstico dos pacientes brasileiros já foi observada por Penido et al.,17 em um estudo de coorte com crianças e adolescentes americanas e brasileiras com UL. Os autores mostraram uma tendência dos pacientes brasileiros de serem mais jovens ao diagnóstico.
Distúrbios metabólicosDMet são comumente associados à UL, em especial na população pediátrica, e podem resultar em quadros recorrentes de formação de cálculos.1,21 Estudos revelam altas taxas de prevalência de DMet nessa população, variam de 76% a 91%,18,22 o que está em conformidade com este estudo, no qual 95% dos participantes apresentavam pelo menos um DMet. As altas prevalências de hipocitratúria e hipercalciúria eram esperadas, considerando que esse também foi um achado de diversos autores.17,18,23,24 Penido et al.17 apresentam a suposição de que apesar de a hipercalciúria ter grande importância na UL, e frequentemente ser o DMet mais prevalente, nem sempre ela consegue justificar a tendência à formação de cálculos isoladamente, a menos que baixo nível de citrato esteja associado.25
Estudos recentes têm apontado excreção urinária de sódio aumentada como fator de risco para UL.1,24 Os achados deste estudo estão em consonância com tal informação, 55% dos participantes apresentaram hipernatriúria na análise urinária. Já a hipomagnesiúria, frequentemente pouco prevalente,23 ocorreu em 50% dos casos deste estudo, apesar de 57,9% das crianças com esse DMet apresentarem ingestão adequada de magnésio.
É sabido que adequada ingestão hídrica previne supersaturação de substâncias na urina e formação de cálculos.1,21 Penido et al.18 mostraram alta prevalência de baixo volume urinário e em 24% das crianças e adolescentes avaliados essa era a única alteração metabólica. Já um estudo comparativo entre crianças americanas e brasileiras demonstrou oligúria em 63% e 49% dos participantes, respectivamente.17 O presente estudo apontou oligúria em 20% dos casos. É possível que essa menor porcentagem possa ser justificada pela adesão dos pacientes à insistente recomendação sobre ingestão hídrica no ambulatório onde ocorreu este estudo.
Observa‐se que os perfis bioquímicos de urina variam ao redor do mundo e dependem de fatores genéticos, ambientais, dieta e ocorrência de infecção do trato urinário.1,17 Independentemente desses fatores, nota‐se que a maioria das crianças com UL tem algum DMet.1,18,21,24
Avaliação nutricionalUm quarto dos participantes do presente estudo foi classificado com sobrepeso ou obesidade, 80% daqueles que tinham sobrepeso e 100% dos obesos eram adolescentes. Apesar da ausência de evidências na literatura sobre a associação entre IMC e faixa etária na população pediátrica com UL, os dados deste estudo sugerem que quanto mais velha for a referida população, mais frequentes serão o sobrepeso e a obesidade.
Avaliação do consumo alimentarA associação entre alimentação e a ocorrência de DMet causadores de UL há muito tem sido levantada, com algumas associações bem estabelecidas. Dentre os macronutrientes que apresentam relação descrita com a litogênese, têm destaque as proteínas.1 Neste estudo todos os indivíduos apresentaram consumo médio de proteína dentro dos valores recomendados pela literatura. Estudos afirmam que dietas ricas em proteínas, especialmente as de origem animal, levam ao aumento da excreção renal de cálcio, hiperuricosúria e redução da citratúria.1 Pois o metabolismo das proteínas gera elevação das cargas ácidas no sangue, culmina em aumento da remodelação óssea e hipercalciúria.21 Dentre as cargas ácidas geradas pelo metabolismo das proteínas, a principal é o ácido úrico, o que contribui para a hiperuricosúria.19 Com vista nisso, e nas necessidades proteicas para o adequado desenvolvimento, recomendações atuais visam a dietas normoproteicas, sem componente restritivo para as crianças portadoras de UL.1,21
Os outros dois macronutrientes, carboidratos e lipídeos, apesar de não diretamente relacionados com a litogênese, contribuem de forma direta na manutenção do peso adequado, por constituírem as principais fontes energéticas da dieta habitual. Sabe‐se que o sobrepeso/obesidade, bem como uma de suas principais consequências, a síndrome metabólica, têm apresentado relação com a formação de UL, fato que reforça as recomendações atuais de uma dieta equilibrada para esses pacientes.24 Neste estudo, a maioria dos indivíduos (70%) apresentava consumo médio de carboidratos dentro das faixas de recomendação para idade e sexo, porém mais de um terço deles apresentava consumo lipídico acima do recomendado. Considerando que a carga calórica lipídica é mais do que o dobro da carga calórica dos carboidratos, dietas hiperlipídicas contribuem significativamente para o aumento das taxas de sobrepeso/obesidade na infância.
A avaliação dos lipídeos, sem considerar o percentual correspondente de cada subtipo de molécula gordurosa (ácidos graxos saturados ou insaturados, por exemplo), é restrita, pois cada um desempenha papel diferente no metabolismo e, assim, pode ter repercussões benéficas ou não no corpo humano. No presente estudo não foram avaliados os subtipos lipídicos que formavam a alimentação dos participantes. Entretanto, foi quantificada a ingestão média de colesterol, classe importante de lipídeo. As recomendações atuais da The National Academies of Sciences Engineering Medicine, órgão responsável pela elaboração das DRI, afirmam que para o colesterol não há valor mínimo de referência para consumo diário.10 Entretanto, recomenda‐se a menor ingestão possível, considerando o importante papel da dislipidemia como fator de risco cardiovascular.26 Os participantes deste estudo apresentaram uma mediana de ingestão de colesterol de 358,8mg/dia, a variação entre os participantes foi bastante heterogênea.
No combate à dislipidemia um dos grandes agentes são as fibras alimentares, componente importante de uma alimentação saudável. Estudos com adultos demonstraram que dietas ricas em fibras relacionam‐se com menor incidência de UL.27 Contudo, a população brasileira não costuma consumir esse nutriente, o que se reflete no hábito alimentar infantil. Neste estudo 65% dos participantes apresentaram dieta pobre em fibras, com uma mediana de 23,5g/dia. Quando se considera o estado nutricional dos participantes, é possível identificar uma tendência para o maior consumo de fibras entre os eutróficos quando comparados com os que apresentaram sobrepeso e obesidade, com mediana de 27,9g/dia (16,3‐38,5), 16,7g/dia (15,5‐21,8) e 14,5g/dia (13,6‐15,9), respectivamente. Em relação à inadequação alimentar, todos os indivíduos com sobrepeso e 80% daqueles com obesidade apresentavam consumo diário inferior ao recomendado para sua idade e sexo. Já entre os eutróficos tal porcentagem era de 56,6%.
Dentre os micronutrientes com comprovada relação com a UL destaca‐se o sódio, o qual, quando em excesso, leva ao aumento da calciúria e favorece a formação de cálculos de cálcio.1,21 A ingestão de sódio entre a população infantil, assim como na adulta, é elevada, principalmente devido à grande quantidade de alimentos processados que compõe a dieta contemporânea. Segundo dados da Pesquisa de Orçamento Familiar 2008‐2009, 70% dos adolescentes consumiam sódio acima dos valores toleráveis (Tolerable Upper Intake Level segundo a DRI).28 Os achados do presente estudo não foram diferentes, 55% dos participantes consumiram sódio acima do recomendado para idade e sexo. A média de ingestão diária encontrada foi 2,6g/dia, valor superior ao nível máximo recomendado para a população adulta, de 2,3g/dia.10 Dentre os participantes que apresentaram hipercalciúria 57,7% ingeriam quantidade média diária de sódio superior ao valor recomendado. Já no grupo sem esse DMet, a minoria (41,7%) tinha ingestão de sódio acima das recomendações. Esse achado demonstra que a relação entre ingestão excessiva de sódio e hipercalciúria esteve presente, apesar de não ter sido encontrada significância estatística, o que provavelmente se justifica pelo tamanho da amostra. Dessa forma, limitar o consumo desse mineral é uma medida importante para diminuir a calciúria na prática clínica.1
O sódio e o potássio classicamente têm efeitos inversos nos valores de pressão arterial sistêmica. Essa tendência também se mantém no que diz respeito à calciúria, já que os sais de potássio diminuem a excreção urinária de cálcio.21 Na presente análise o consumo de potássio foi inverso ao encontrado para o sódio, com 52,5% dos participantes com ingestão abaixo do recomendado e média de consumo de 4,8g/dia.
O cálcio alimentar tem relação com a UL, mas sua ação não está relacionada à hipercalciúria, mas sim à hiperoxalúria. Dietas pobres em cálcio podem aumentar a absorção intestinal de oxalato e elevar o risco de UL, já que tal mineral é frequente na composição dos cálculos. Um estudo clássico conduzido por Curhan et al.29 avaliou a dieta de mais de 45 mil adultos por quatro anos e encontrou um risco significativamente menor de desenvolvimento de cálculo renal nos indivíduos que consumiam dieta rica em cálcio quando comparado com aqueles com dieta pobre nesse mineral. Nesse escopo, as recomendações atuais enfatizam a necessidade de dietas com conteúdo de cálcio dentro da normalidade.1,21 Encontramos apenas 27,5% dos participantes com ingestão dentro do recomendado, os demais se distribuíram de maneira semelhante entre abaixo e acima do valor normal. A hiperoxalúria não está entre os DMet mais comuns,18 assim como observado neste estudo, no qual apenas um participante tinha tal alteração e apresentava consumo de cálcio abaixo do valor indicado para sua idade e sexo.
O consumo de frutas e verduras, fontes importantes de magnésio, citrato e potássio, deve sempre ser incentivado na população geral, cabe especial recomendação naqueles com UL. Estudos têm demonstrado que em pessoas com hipocitratúria uma alimentação rica nesses componentes eleva a excreção renal de magnésio e citrato, aumenta os fatores urinários antilitogênicos.30 Nesta análise encontraram‐se apenas 10% dos participantes com ingestão de magnésio abaixo do recomendado, desses a maioria tinha sobrepeso/obesidade.
A maioria (75%) dos participantes também apresentou ingestão diária adequada de ferro, com média de 9,8mg/dia. Chama a atenção o fato de que o consumo médio de ferro se reduzia conforme aumentava o IMC, com 10,4mg/dia (± 6,4) entre os eutróficos, 8,8mg/dia (± 2,6) entre aqueles com sobrepeso e 7,2mg/dia (± 4,4) entre os obesos. Contudo, não foram encontrados dados na literatura sobre tal associação, o que evidencia a necessidade de mais estudos.
Avaliar a ingestão alimentar é uma tarefa difícil, considerando as diversas nuances que os métodos de avaliação atuais apresentam. Dentre as mais usadas estão o diário alimentar de três dias, o recordatório de 24h e o QFA. Neste trabalho, optou‐se pelo QFA, que, apesar de não ser o melhor método disponível, encontra‐se entre as opções mais aceitas para avaliação do padrão alimentar de uma população, é capaz de quantificar e avaliar a ingestão por períodos mais longos.
Das limitações do estudo, cabe citar principalmente o tamanho da amostra e a ausência de grupo controle, o que impossibilita analisar se o padrão alimentar e os DMet são característicos da UL no sul do Brasil e se a composição da dieta reflete o padrão alimentar de crianças e adolescentes dessa região. Em relação aos hábitos alimentares, não foram avaliados os subtipos lipídicos e a ingestão hídrica diária, a última faz parte da abordagem inicial no tratamento da UL. Outra possível restrição foi que, no momento da entrevista, os participantes já teriam recebido orientações alimentares gerais em consulta prévia com a equipe de nefrologia pediátrica, as quais já poderiam ter sido introduzidas em seus hábitos alimentares.
A UL pediátrica é frequentemente acompanhada de DMet. Esse fato confirma a necessidade de avaliação metabólica adequada ao diagnóstico, bem como a análise do padrão alimentar. Na presente amostra observou‐se baixa ingestão de fibras alimentares e potássio e elevada ingestão de sódio. Essas, por sua vez, não foram significativamente associadas com os DMet. A carência de dados na literatura acerca dos hábitos alimentares em crianças e adolescentes com UL, bem como a ainda não comprovada associação entre UL pediátrica e obesidade, suscita mais estudos sobre o tema, com o objetivo de melhorar o entendimento e a abordagem terapêutica dessa condição, que afeta cada vez mais essa população.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Como citar este artigo: Vieira MS, Francisco PC, Hallal AL, Penido MG, Bresolin NL. Association between dietary pattern and metabolic disorders in children and adolescents with urolithiasis. J Pediatr (Rio J). 2020;96:333–40.
Estudo vinculado ao Hospital Infantil Joana de Gusmão, Serviço de Nefrologia, Florianópolis, SC, Brasil.