This review article aimed to present a clinical approach, emphasizing the diagnostic investigation, to children and adolescents who present in the emergency room with acute‐onset muscle weakness.
SourcesA systematic search was performed in PubMed database during April and May 2017, using the following search terms in various combinations: “acute,” “weakness,” “motor deficit,” “flaccid paralysis,” “child,” “pediatric,” and “emergency”. The articles chosen for this review were published over the past ten years, from 1997 through 2017. This study assessed the pediatric age range, from 0 to 18 years.
Summary of the dataAcute motor deficit is fairly common presentation in the pediatric emergency room. Patients may be categorized as having localized or diffuse motor impairment, and a precise description of clinical features is essential in order to allow a complete differential diagnosis. The two most common causes of acute flaccid paralysis in the pediatric emergency room are Guillain‐Barré syndrome and transverse myelitis; notwithstanding, other etiologies should be considered, such as acute disseminated encephalomyelitis, infectious myelitis, myasthenia gravis, stroke, alternating hemiplegia of childhood, periodic paralyses, brainstem encephalitis, and functional muscle weakness. Algorithms for acute localized or diffuse weakness investigation in the emergency setting are also presented.
ConclusionsThe clinical skills to obtain a complete history and to perform a detailed physical examination are emphasized. An organized, logical, and stepwise diagnostic and therapeutic management is essential to eventually restore patient's well‐being and full health.
Apresentar uma abordagem clínica, enfatizar a investigação diagnóstica, voltada para crianças e adolescentes no pronto‐socorro com fraqueza muscular de surgimento agudo.
FontesFoi feita uma pesquisa sistemática na base de dados PubMed entre abril e maio de 2017, com os seguintes termos de pesquisa em várias combinações: “agudo”, “fraqueza”, “déficit motor”, “paralisia flácida”, “criança”, “pediátrico” e “emergência”. Os trabalhos escolhidos para esta revisão foram publicados nos últimos dez anos, de 1997 a 2017. Este trabalho aborda a faixa etária pediátrica, até 18 anos.
Resumo dos dadosO déficit motor agudo é uma causa razoavelmente comum para crianças e adolescentes procurarem o pronto‐socorro. Os pacientes podem ser classificados como com deficiência motora localizada ou difusa e uma descrição precisa das características clínicas é essencial para possibilitar um diagnóstico diferenciado completo. As duas causas mais comuns de paralisia flácida aguda no pronto‐socorro pediátrico são síndrome de Guillain‐Barré e mielite transversa, independentemente de outras etiologias serem consideradas, como encefalomielite disseminada aguda, mielite infecciosa, miastenia grave, derrame, hemiplegia alternante da infância, paralisia periódica, encefalite do tronco encefálico e fraqueza muscular funcional. Os algoritmos da investigação de fraqueza aguda localizada ou difusa na configuração de emergência também são apresentados.
ConclusõesSão enfatizadas as habilidades clínicas para obter um histórico completo e fazer um exame físico detalhado. Um manejo diagnóstico e terapêutico organizado, lógico e por etapas é essencial para eventualmente restaurar o bem‐estar e a saúde total do paciente.
O déficit motor agudo ou fraqueza é uma apresentação razoavelmente comum em crianças e adolescentes no pronto‐socorro (PS) pediátrico. Em todas as faixas etárias, 5% de todos os pacientes que procuram o PS apresentam sintomas neurológicos.1 Nesse ambiente, o pediatra deve se sentir confortável para fazer o manejo inicial, pois algumas etiologias podem ser fatais e exigem cuidado urgente. Por outro lado, as intervenções oportunas podem provavelmente restaurar o bem‐estar e a saúde total do paciente.
A fraqueza é classificada como um sinal motor negativo, bem como ataxia e apraxia. É valioso ter um entendimento preciso sobre a definição desses três sinais motores negativos. Fraqueza é definida como a incapacidade de gerar força voluntária normal em um músculo ou torque voluntário normal sobre uma articulação, ao passo que ataxia é a incapacidade de gerar uma trajetória de movimento voluntário normal, que não pode ser atribuída a fraqueza ou atividade muscular involuntária nas articulações afetadas.2 Os movimentos atáxicos são descoordenados e atrapalhados, porém não há fraqueza subjacente dos músculos envolvidos. Apraxia é a incapacidade de fazer movimentos complexos aprendidos, que não é explicada por fraqueza, ataxia ou atividade motora involuntária, ou seja, as funções motoras, sensoriais, dos gânglios da base e cerebelares estão intactas.2 Deve ser enfatizado que não existe fraqueza sensorial.
Para fins deste trabalho, o termo plegia será usado para indicar fraqueza completa ou parcial,3 porém o leitor é informado que plegia, estritamente falando, significa paralisia total e paresia implica que a força muscular é afetada apenas parcialmente. Uma descrição comum de fraqueza aguda é paralisia flácida aguda, o que significa que na configuração de PS a paralisia normalmente não é acompanhada por espasticidade ou outros sinais anormais dos tratos motores do sistema nervoso central (SNC), por exemplo, hiperreflexia, clonus ou sinal de Babinski.4
Os objetivos deste trabalho são apresentar uma abordagem de diagnóstico clínico voltada para crianças e adolescentes que apresentam déficit motor agudo no PS e revisar as etiologias mais frequentes.
MétodosFoi feita uma pesquisa sistemática na base de dados PubMed entre abril e maio de 2017, com os seguintes termos de pesquisa em várias combinações: “agudo”, “fraqueza”, “déficit motor”, “paralisia flácida”, “criança”, “pediátrico” e “emergência”. Os trabalhos escolhidos para esta revisão foram publicados nos últimos dez anos, de 1997 a 2017. Este trabalho aborda a faixa etária pediátrica, até 18 anos.
Características clínicas e diagnóstico diferenciadoA fraqueza aguda pode apresentar deficiência localizada ou difusa. Uma descrição precisa do déficit motor – sua forma de início, duração e progressão – é essencial para possibilitar um diagnóstico diferenciado completo. Nesse sentido, um histórico detalhado e um exame físico completo, inclusive um exame neurológico objetivo, fornecerão as melhores oportunidades para agilizar a identificação da etiologia. A tabela 1 descreve as informações essenciais a serem compiladas durante a abordagem inicial a um paciente que apresenta fraqueza aguda.
Histórico e exame físico de um paciente com déficit motor agudo
| Histórico |
| É a primeira vez que a criança apresenta fraqueza? |
| Início – quando e o que a criança fazia quando o déficit foi detectado? |
| Ritmo – abrupto, rápido ou lentamente progressivo, flutuante ou remitente‐recorrente? |
| A fraqueza está associada a fatores precipitantes, como um lugar, uma pessoa, um alimento, uma medicação ou um horário do dia? |
| A fraqueza melhora com descanso e piora com atividade (fatigabilidade)? |
| Houve um aumento na frequência de quedas no passado recente? |
| A fraqueza progrediu de forma ascendente ou descendente? |
| Sintomas associados de infecção (febre, dor de cabeça, vômito, diarreia) ou doença recorrente |
| Sintomas sensoriais anteriores ou concomitantes, como dor/sensibilidade, disestesias, dormência, dor de cabeça ou alterações visuais |
| Mudanças nos hábitos de micção e intestinais |
| Mudanças no estado mental – houve algum comprometimento no estado mental do paciente? |
| Histórico de infecções recentes e outras doenças |
| Uso de todos os medicamentos, inclusive fitoterapia, colírios etc. |
| Histórico do desenvolvimento – idades de aquisição de habilidades motoras, qualquer regressão, outras áreas de desenvolvimento |
| Histórico de trauma, principalmente na cabeça e no pescoço |
| Histórico de convulsões |
| Contato com outras pessoas doentes |
| Histórico psicossocial – estresse recente, interações com pares, desempenho escolar, problemas comportamentais, morte ou afastamento de pessoas queridas |
| Contato com animais de estimação e outros animais |
| Exame físico e neurológico |
| Sinais vitais |
| Perímetro cefálico |
| Parâmetros de crescimento |
| Simetria corporal |
| Rigidez nucal e outros sinais meníngeos |
| Sinais de insuficiência respiratória |
| Estado mental – alerta, irritabilidade, orientação para hora e local, habilidades linguísticas |
| Sistemas cardiovascular e respiratório e exame do abdômen |
| Exame do nervo craniano – tamanho das pupilas e reação à luz? Acuidade visual? Fundoscopia? Fraqueza facial? Movimentações musculares extraoculares? Movimentações do palato e da língua? |
| Exame motor – tônus muscular e força, reflexos do tendão profundo, clônus do tornozelo, teste de pronação |
| Sinal de Babinski |
| Exame sensorial que busca um nível sensorial |
| Coordenação – prova de dedo‐nariz, diadococinesia |
| Marcha – capacidade de sentar ou andar sem/com apoio? Andar na ponta dos pés, nos calcanhares |
| Sinais de doença muscular crônica, por exemplo, atrofia muscular, fasciculações, miotomia, sinal de Gowers |
A forma como a fraqueza se estende para outras partes do corpo pode oferecer pistas para o diagnóstico. Por exemplo, um déficit ascendente relativamente simétrico sugere síndrome de Guillain‐Barré (GBS), ao passo que a paralisia descendente gera suspeita de botulismo.5
Alguns pacientes comparecerão ao PS com o que parece ser fraqueza aguda, porém uma avaliação abrangente revelará que, de fato, ele/ela tem pseudoparalisia, ou seja, a força muscular é preservada e a função motora do paciente é prejudicada por outro mecanismo, mais frequentemente dor severa. Os exemplos pediátricos comuns dessa situação são incapacidade de andar devido a dor nas panturrilhas, secundária a miosite viral aguda, artralgia relacionada a artrite piogênica (por exemplo, artrite gonocócica em adolescentes), cotovelo da babá (pronação dolorosa) ou dor óssea secundária a osteomielite, fratura óssea ou luxação.
Após erradicação da poliomielite, as duas causas mais comuns de paralisia flácida aguda no PS são GBS e mielite transversa aguda.6 Entre outras etiologias (tabela 2), as mais relevantes para a faixa etária pediátrica são encefalomielite disseminada aguda (ADEM), mielite infecciosa, miastenia grave, derrame, hemiplegia alternante da infância, paralisia periódica, encefalite do tronco encefálico e fraqueza muscular funcional.
Etiologias de déficit motor difuso agudo
| Etiologias mais comuns |
| Síndrome de Guillain‐Barré |
| Mielite transversa |
| Outras etiologias |
| Encefalomielite disseminada aguda (ADEM) |
| Hemiplegia alternante da infância |
| Luxação atlanto‐axial |
| Botulismo |
| Abscesso cerebral |
| Infecções do SNC, por exemplo, meningite aguda |
| Lesões de massa do SNC |
| Polineuropatia desmielinizante inflamatória crônica (PDIC) |
| Enxaqueca complicada |
| Miopatias congênitas |
| Epilepsia, ou seja, paralisia de Todd |
| Paraplegia espástica familiar |
| Fraqueza muscular funcional (anteriormente chamada de distúrbio de conversão) |
| Hipoglicemia |
| Hipofosfatemia |
| Síndrome de Hopkins (associada a asma aguda) |
| Mielite infecciosa (por exemplo, por enterovírus) |
| Hemorragia intracraniana |
| Doença de Kawasaki |
| Doença metabólica |
| Miastenia grave |
| Paralisia periódica |
| Compressão da medula espinhal |
| Poliomielite associada a vacina |
| Vasculite |
| Derrame |
SNC, sistema nervoso central.
A GBS, ou polirradiculoneuropatia desmielinizante inflamatória aguda (AIDP), é uma doença autoimune que normalmente apresenta início agudo de fraqueza rapidamente progressiva, basicamente simétrica, e arreflexia em uma criança que anteriormente estava bem.7 A fraqueza aguda na GBS tende a iniciar distalmente e progredir rostralmente e, em 50‐70% dos casos, ela é precedida, em quatro semanas, por uma infecção respiratória ou gastrointestinal aguda. Os agentes etiológicos envolvidos com mais frequência são Campylobacter jejuni e Helicobacter pylori no trato gastrointestinal e Mycoplasma pneumoniae no trato respiratório. Uma incidência anual de 0,5‐2 casos por 100.000 indivíduos é relatada na faixa etária < 18 anos.8 A GBS está associada a uma vacinação nos 30 dias anteriores em menos de 10% dos casos.9
A AIDP é, na verdade, um termo descritivo para o quadro clínico mais comum da GBS, ao passo que, em 10‐15% dos casos, as características clínicas abrangem formas de variação da GBS, como neuropatia axonal motora aguda (AMAN, com evolução mais rápida e déficits motores mais graves, inexistência de déficits sensoriais), neuropatia axonal motora e sensorial aguda (AMSAN, relatada quase exclusivamente em adultos), síndrome de Miller‐Fisher (ataxia, oftalmoplegia e arreflexia sem fraqueza periférica), variante faringo‐cérvico‐braquial (ptose, fraqueza do músculo flexor facial, faríngeo, pescoço), pandisautonomia aguda e oftalmoplegia aguda.8,10,11 A AMAN deve‐se a um dano axonal e é diagnosticada com mais frequência na Ásia e na América do Sul.11
O acometimento clínico é caracterizado por dor nos membros, fraqueza nos membros e, em alguns casos, ataxia. O exame físico normalmente apresenta estado mental preservado ou irritabilidade e reflexos do tendão profundo reduzidos ou inexistentes em membros fracos.7,8 A fraqueza progride em uma direção caudo‐craniana, porém há exceções a esse padrão. O pico da fraqueza normalmente é atingido após 7‐10 dias, porém no máximo até quatro semanas. A gravidade da fraqueza dos braços é o fator de predição mais confiável de insuficiência respiratória.11
O diagnóstico tem como base achados clínicos e é embasado em dissociação albumino‐citológica em líquido cefalorraquidiano (LCR), ou seja, um aumento no nível de proteína apesar da contagem normal de leucócitos, de uma ressonância magnética (RMI) da coluna vertebral que mostre o realce, por contraste, das raízes nervosas e/ou dos achados de desmielinização ou danos axonais na eletromiografia com estudos de condução nervosa (EMG). Alguns pacientes apresentam estudos normais de EMG nas duas primeiras semanas da doença, porém, posteriormente, todos apresentam resultados anormais.6
Mielite transversaA mielite transversa aguda (MTA) representa um quinto dos eventos desmielinizantes adquiridos em crianças, tem uma incidência anual estimada em crianças com idades < 16 anos de 2 por 1.000.000 e sua proporção de sexo masculino:feminino é 1.1‐1.6:1.12 Há dois picos de incidência pediátrica, nas faixas de 0‐2 anos e 5‐17 anos, e a incidência mais alta encontra‐se na primeira.13 Em dois terços dos casos, houve uma infecção prodômica nos últimos 30 dias.
As crianças afetadas desenvolvem um início agudo de paraplegia ou tetraplegia simétricas, redução ou perda de sensação e disfunção do esfíncter e seu curso clínico se estende para mais de três fases: aguda (normalmente 2‐7 dias), nível de estabilização (1‐26 dias) e fases de recuperação (meses a anos). Em alguns pacientes, a dor é a característica presente.6
A MTA é um diagnóstico de exclusão; assim, é importante considerar com cuidado seus diagnósticos diferenciais. Nesse sentido, os critérios de diagnóstico estabelecidos pelo Grupo de Trabalho do Consórcio de Mielite Transversa podem ser valiosos (tabela 3).14
Critérios de diagnóstico para mielite transversa
| Critérios de inclusão |
| Desenvolvimento de disfunção sensorial, motora ou autonômica atribuída à medula espinhal |
| Sintomas bilaterais |
| Nível sensorial claramente definido |
| Exclusão de causas de compressão por imagem de RM ou mielografia de TC |
| Inflamação da medula espinhal demonstrada por pleocitose do líquido cefalorraquidiano, IgG elevado ou realce pelo gadolínio |
| Progresso para nadir clínico entre quatro horas e 21 dias do início dos sintomas |
| Critérios de exclusão |
| Histórico de irradiação para a lombada para a coluna vertebral em 10 anos |
| Achados clínicos compatíveis com oclusão da artéria espinhal anterior |
| Ausência de fluxo anormal na superfície do cordão compatível com malformação arteriovenosa |
| Comprovação sorológica ou clínica de doença do tecido conjuntivo (sarcoidose, doença de Behçet, síndrome de Sjögren, lúpus eritematoso sistêmico ou distúrbio misto do tecido conjuntivo) |
| Manifestações do sistema nervoso central de sífilis, doença de Lyme, HIV, HTLV‐1, Micoplasma ou outra infecção viral |
| Anormalidades cerebrais sugestivas de esclerose múltipla |
| Histórico de neurite óptica clinicamente aparente |
Fonte: Grupo de Trabalho do Consórcio de Mielite Transversa. Critérios de diagnóstico propostos e nosologia de mielite transversa aguda.14
As crianças serão beneficiadas por um resultado motor favorável, com recuperação completa de até 56%, e um estudo constatou que o tempo médio de recuperação da capacidade de andar de forma independente foi 56 dias.6
Encefalomielite disseminada aguda (ADEM)A ADEM é uma doença desmielinizante inflamatória que normalmente ocorre em dois dias a quatro semanas após uma infecção viral ou, menos comumente, vacinação.15 Ela apresenta déficits neurológicos multifocais acompanhados de encefalopatia e seu tempo médio de início é 5,7 anos, com proporção de sexo masculino/feminino de 2,3:1.15,16
As características clínicas podem incluir febre, dor de cabeça, vômito, sinais meníngeos, perda da visão, convulsões, paralisias do nervo craniano e alterações no estado mental, que vão de letargia a coma.15 Há uma controvérsia atual sobre se a ADEM e a esclerose múltipla (EM) pertencem ao mesmo espectro de doenças ou se são entidades completamente distintas.16 Apesar de a ADEM normalmente seguir um curso monofásico, seus fatores de variação recorrentes e multifásicos atrapalham na distinção de EM. A RMI do cérebro pode ser a ferramenta mais valiosa para fazer essa distinção, pois os casos de ADEM mostram grandes áreas de aumento da intensidade de sinal nas imagens ponderadas em T2 e FLAIR, com bordas mal definidas, distribuídas bilateralmente na substância branca (SB) cerebral e que normalmente afetam os gânglios da base, o tronco cerebral, a substância cinzenta do córtex cerebelar e cerebral, ao passo que os casos de EM normalmente mostram lesões bem definidas localizadas na SB periventricular.17 A ausência de encefalopatia, idade acima de 10 anos, presença de neurite óptica e bandas oligoclonais intratecais durante um evento de desmielinização do SNC aumentam o risco de possível desenvolvimento de EM.15
O LCR pode ser normal ou apresentar pleocitose leve, com ou sem níveis elevados de proteína.15
O tratamento precoce e agressivo pode obter uma boa recuperação com déficit mínimo ou nenhum déficit em mais da metade dos pacientes.18
Mielite infecciosaA paralisia flácida aguda pode resultar de infecção na medula espinhal com vários patógenos, por exemplo, vírus do Oeste do Nilo, enterovírus não pólio, vírus da dengue, sífilis, doença de Lyme, vírus da imunodeficiência humana (HIV), citomegalovírus, HTLV‐1 e micoplasma.14,19 Sua principal característica distintiva da mielite transversa é que a maior parte das crianças apresenta paralisia da medula espinhal relacionada a poliomielite focal, com sintomas sensoriais mínimos ou nenhum sintoma sensorial.20
Miosite viral agudaA miosite viral aguda se manifesta com odor muscular e fraqueza nos membros inferiores, principalmente nas panturrilhas e nas coxas.21 Ela é, na maior parte das vezes, associada à infecção pelo vírus da gripe. Dessa forma, seus sintomas prodômicos incluem febre, dor de cabeça, tosse e outros sinais respiratórios. As crianças afetadas podem deixar de mover suas pernas logo após sentir dor ou podem de fato ter fraqueza relacionada a rabdomiólise.22 Entre 35 casos com idade média de 7,5 anos, a fraqueza muscular durou de um a oito dias e a média de creatina‐quinase sérica foi de 5.507 U/L.21
Miastenia graveA miastenia grave (MG) é uma doença neuromuscular autoimune relativamente rara e seu surgimento na infância é dividido em MG neonatal transitória e MG juvenil. A primeira deve‐se à transferência placentária de anticorpos receptores de acetilcolina (AChR) e normalmente é tratada em dois meses de vida.23
O quadro clínico é caracterizado por fatigabilidade e fraqueza oscilante dos músculos oculares, faciais, dos membros, bulbares e respiratórios. Os anticorpos contra AChR, proteína quinase específica do músculo (MuSK) e relacionada aos receptores de lipoproteína (LRP4), podem participar de sua patogênese.24
Um estudo comparou 114 pacientes chineses com MG juvenil com 207 pacientes adultos com MG juvenil. Os anticorpos foram encontrados em 77, 80 e 81% dos subgrupos de 0‐8 anos, 8‐18 anos e adultos, respectivamente. Apenas um dos seis pacientes que apresentaram resultado positivo para os anticorpos MuSK e LRP4 não era adulto. A estimulação repetitiva do nervo durante a eletromiografia (EMG) pode ser útil para o diagnóstico, bem como o teste de neostigmina, porém isso deve ser feito apenas em um ambiente controlado e monitorado, na presença de uma equipe capacitada em ressuscitação cardiopulmonar. Atropina deve estar prontamente disponível.23
DerrameDerrame pode ocorrer em crianças com mais de um mês de vida, com frequência de 13/100.000 por ano. Sua incidência é maior em neonatos (25 a 40/100.000) e ainda maior entre neonatos prematuros (até 100/100.000).25 Os mecanismos subjacentes em pacientes pediátricos incluem derrame isquêmico, trombose venosa e derrame hemorrágico.26 Os pacientes afetados normalmente apresentam déficit neurológico focal de início agudo, por exemplo, hemiplegia, hemianestesia, hemiataxia, paralisia facial unilateral e/ou afasia.27 Os recém‐nascidos podem apresentar convulsões.26
Terão derrames recorrentes 20 a 30% das crianças com derrame isquêmico arterial, então um diagnóstico precoce se torna essencial.26 A investigação adequada com neuroimagem não deve ser postergada.
Hemiplegia alternante da infânciaA hemiplegia alternante da infância é um transtorno do desenvolvimento raro causado, em 75% dos casos, por uma mutação no gene ATP1A3da proteína neuronal Na+/K+ ATPase.28 O surgimento ocorre antes de 1,5 ano e suas características clínicas consistem em hemiplegia unilateral episódica, distonia, quadriplegia e movimentos oculares anormais. Cada episódio dura minutos, horas ou períodos mais longos e recorre frequentemente. As crianças afetadas pode apresentam atraso no desenvolvimento e epilepsia.28 A flunarizina (bloqueador dos canais de cálcio) pode reduzir a frequência, a gravidade e a duração dos episódios distônicos e hemiplégicos.28
Paralisia periódicaAs paralisias periódicas são associadas a mutações no gene SCN4A dos canais de sódio, gene CACNA1S dos canais de cálcio ou gene KCNJ2 dos canais de potássio e não deve ser confundida com causas secundárias de paralisia episódica, como toxicidade do medicamento.29 Os pacientes apresentam ataques episódicos de fraqueza muscular flácida, normalmente associados a hipo ou hipercalemia. Os episódios podem ser causados por carboidratos ou alimentados ricos em potássio ou por repouso após exercício. O tratamento com acetazolamide pode reduzir a frequência e a gravidade dos episódios.29
Encefalite do tronco encefálicoA encefalite do tronco encefálico (BBE) de Bickerstaff e a síndrome de Miller‐Fisher formam um espectro contínuo, com ataxia e oftalmoplegia externa, porém apenas nos pacientes em que a BBE desenvolve consciência prejudicada.30 A BBE é uma doença incomum de etiologia desconhecida, contudo é comumente associada aos anticorpos da superfície celular do SNC, principalmente anticorpos anti‐GQ1b.31 Os sintomas iniciais mais comuns são diplopia e perturbação da marcha, é encontrada dissociação albuminocitológica do LCR em metade dos pacientes durante a segunda semana da doença e pode haver fraqueza facial e dos membros.30
Infarto da medula espinhalÉ raro em crianças e pode imitar outras entidades comuns, como MTA. A ausência de pleocitose no LCR e o nível normal de proteínas ajudam a diferenciar essas duas entidades. Normalmente envolve a artéria espinhal anterior. Os fatores de risco são pequeno trauma medular, vasculopatias parainfecciosas e cirurgia.32 As crianças apresentam sinais típicos de medula espinhal, como nível sensorial, disfunção vesical e/ou intestinal e paraplegia ou tetraplegia.
Fraqueza muscular funcionalA fraqueza aguda pode decorrer de um transtorno neurológico funcional (TNF), condição anteriormente chamada de histeria e transtorno de conversão, e crianças com cinco anos podem ser afetadas.33 Em um estudo britânico de 204 crianças, faixa de 7‐15 anos, o quadro mais comum foi fraqueza (63%) e movimentações anormais (43%) e o fator de estresse antecedente mais frequente foi bullying na escola (81%).34 Esses autores estimaram que a incidência anual de TNF na faixa < 15 anos foi de 1,30/100.000. Um observador preciso detectará alguns achados incongruentes durante o exame físico de um paciente com fraqueza devido a TNF:6,33,35
- ‐
diplopia monocular – queixas de visão dupla, pela criança, que persiste quando um olho está fechado. Contudo, a diplopia monocular também pode ser causada por um erro de refração, principalmente astigmatismo.
- ‐
a criança não conseguir andar, porém conseguir erguer suas pernas, contra a gravidade, quando deitada na cama. O restante do exame motor é normal.
- ‐
fraqueza de entrega – perda repentina do tônus após resposta inicial a força boa/normal quando um músculo é testado contra resistência
- ‐
cocontração – contração esforçada de um músculo e seu agonista, resultante em quase inexistência de movimentação na articulação
- ‐
descoordenação motora – diferenças significativas do desempenho motor em diferentes condições de teste.
- ‐
sinal de Hoover – o examinador posiciona uma mão sob o calcanhar da perna “boa” e pede que o paciente erga a perna fraca contra resistência. Um paciente com TNF não fará pressão para baixo com a perna boa.
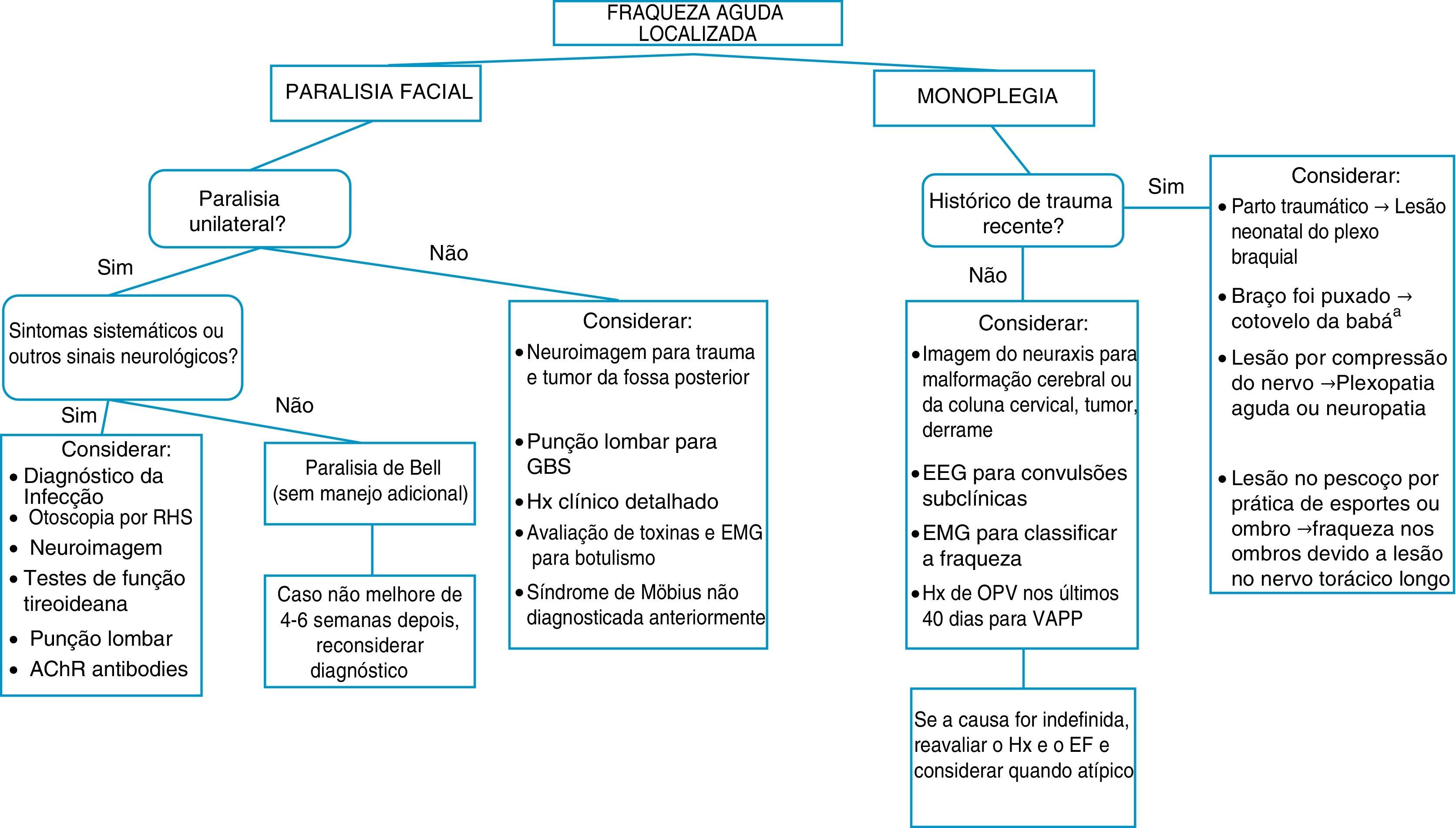
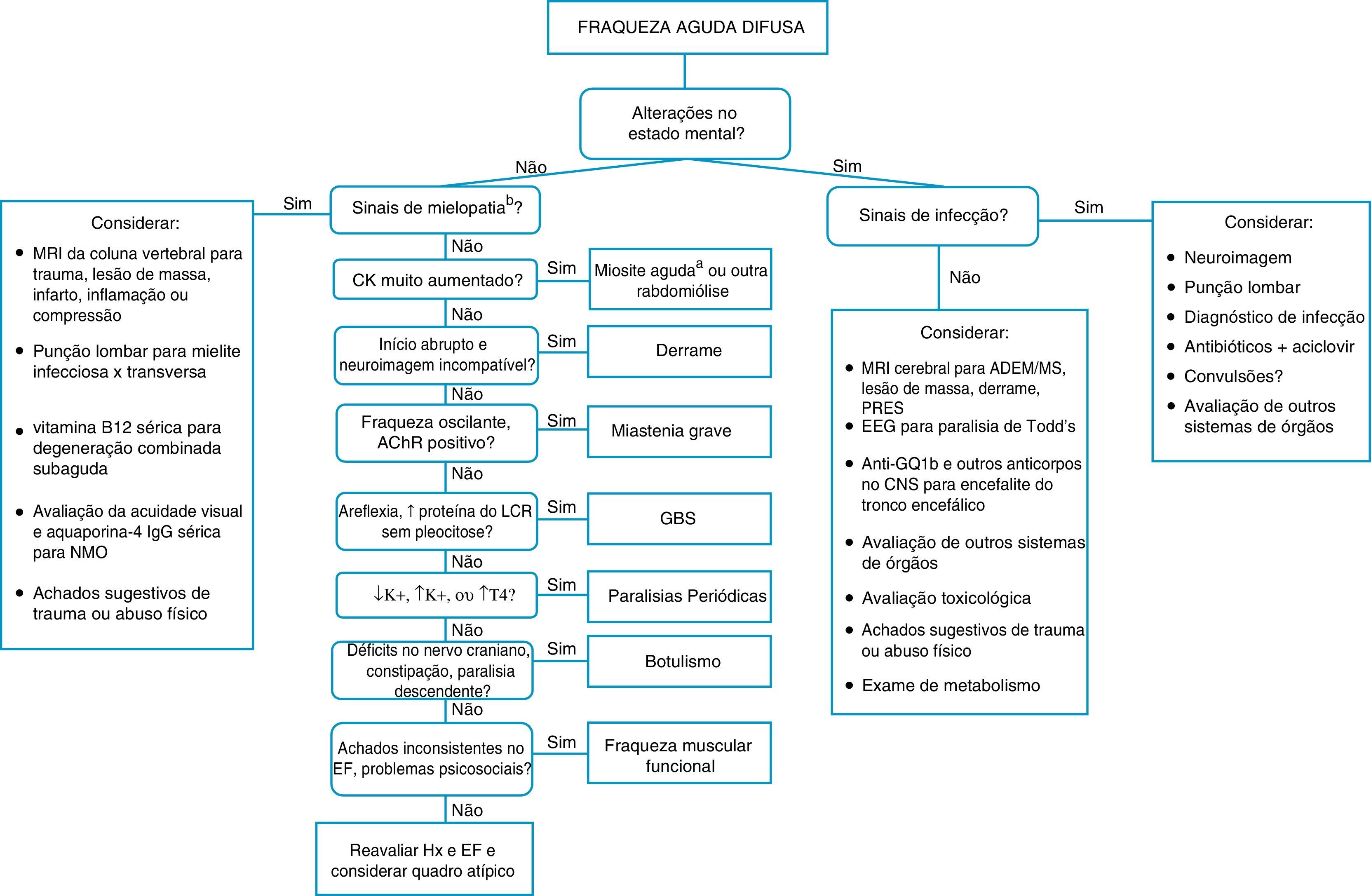
Quando um paciente pediátrico chega no PS com queixa principal de déficit motor agudo, vale prestar atenção a alguns importantes aspectos do histórico e do exame físico (tabela 1). As figuras 1 e 2 sugerem algoritmos para investigação de fraqueza aguda localizada e difusa na configuração de PS, respectivamente.
Algoritmos para investigação de fraqueza aguda localizada na configuração de emergência.
AChR, receptor de acetilcolina; SNC, sistema nervoso central; EEG, eletroencefalografia; EMG, eletromiografia; GBS, síndrome de Guillain‐Barré; Hx, histórico; VOP, vacina oral contra a poliomielite; EF, exame físico; RHS, síndrome de Ramsay‐Hunt; VAPP, poliomielite paralítica associada a vacina.a Uma causa de pseudoparalisia.
Algoritmos para investigação de fraqueza aguda difusa na configuração de emergência.
AChR, receptor de acetilcolina; CK, creatina‐quinase sérica; SNC, sistema nervoso central; LCR, líquido cerebrospinal; EEG, eletroencefalografia; EMG, eletromiografia; GBS, síndrome de Guillain‐Barré; Hx, histórico; IgG, imunoglobulina G; K+, potássio sérico; EM, esclerose múltipla; NMO, neuromielite óptica; EF, exame físico; PRES, síndrome da encefalopatia reversível posterior; RHS, Síndrome de Ramsay‐Hunt; T4, tiroxina; in., inexistente. a Uma causa de pseudoparalisia. b Os sinais de mielopatia incluem um nível sensorial, disfunção vesical e/ou intestinal e paraplegia ou tetraplegia.
Um déficit localizado, por exemplo, paralisia facial (tabela 4)36 ou monoplegia (tabela 5),3 tende a apresentar uma lista menor de etiologias, ao passo que um déficit mais difuso, por exemplo, paraplegia, hemiplegia ou tetraplegia, exigirá a consideração de várias etiologias (tabela 2). A ordem é ter cautela, pois um exame físico abrangente de um paciente que se queixa de monoplegia pode revelar fraqueza discreta de um membro adicional, então o paciente pode de fato ser afetado por hemiplegia ou paraplegia.37
Etiologias da paralisia facial
| Congênita | Adquirida |
|---|---|
| A causa mais comum | |
| Trauma de nascimento | Paralisia de Bell |
| Outras causas | |
| Síndrome perisylviana bilateral congênita Miastenia congênita Distrofia miotônica congênita Aplasia do músculo facial Distrofia muscular facioescapuloumeral Síndrome de Möbius Miastenia neonatal transitória | Otite média aguda Lesão de massa do tronco encefálico (por exemplo, glioma pontinho) Medicamentos: interferon, ribavirina Estreitamento anômalo do canal facial Schwannoma do nervo facial Hipoparatireoidismo Hipotireoidismo Infecção por herpes vírus simples Doença de Lyme Síndrome de Melkersson‐Rosenthal Caxumba Miastenia grave Outras infecções Síndrome de Ramsay‐Hunt Derrame |
Fonte: com permissão de Vasconcelos.36
Etiologias da monoplegia
| Lesão de massa do sistema nervoso central, inclusive tumor, hematoma ou abcesso |
| Enxaqueca complicada |
| Epilepsia |
| Trauma de cabeça ou espinhal |
| Neurite braquial hereditária |
| Neuropatia hereditária com predisposição a paralisia de pressão |
| Paralisia neonatal do plexo braquial |
| Neuropatia |
| Plexopatia |
| Derrame |
| Neuropatia peroneal traumática |
| Poliomielite paralítica associada a vacina |
Fonte: adaptado de Fenichel.3
Quando um paciente apresenta fraqueza difusa de início agudo, a presença ou ausência de alterações no estado mental, ou seja, encefalopatia, norteará o diagnóstico. Em pacientes com encefalopatia, uma infecção do SNC se tornar uma hipótese premente a ser considerada por estudos adequados. Outras entidades também devem ser cogitadas, como convulsões, lesões de massa, disfunção em outros sistemas orgânicos, trauma e alterações metabólicas.
Grande parte do exame neurológico aborda o local da lesão e acreditamos que um pediatra que trabalhe no PS deve saber examinar se um déficit motor agudo resulta do encéfalo, do tronco encefálico, da medula espinhal, da junção neuromuscular, do músculo esquelético ou dos nervos periféricos.
Vários testes e procedimentos estão disponíveis para investigar um paciente extremamente fraco. Como em situações semelhantes, deve‐se priorizar descartar as condições fatais e passíveis de tratamento. Um diagnóstico por etapas, com bom custo‐benefício e oportuno, é fortemente recomendado, conforme descrito nas figuras 1 e 2.
ConclusõesA maior parte dos pacientes que chegam ao PS com déficit motor agudo será beneficiada por uma abordagem investigativa prática e intervenções oportunas com base no histórico, no exame físico e em alguns testes de diagnóstico e conseguirá eventualmente recuperar seu bem‐estar e sua saúde completa.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Como citar este artigo: Vasconcelos MM, Vasconcelos LG, Brito AR. Assessment of acute motor deficit in the pediatric emergency room. J Pediatr (Rio J). 2017;93:26–35.