The population‐based cancer registries (PBCR) and the Information System on Live Births in Brazil (Sistema de Informações sobre Nascidos Vivos [SINASC]) have information that enables the test for risk factors associated with leukemia at an early age. The aim of this study was to identify maternal and birth characteristics associated with early‐age acute leukemia (EAL) in Brazil.
MethodsA case‐cohort study was performed using secondary dataset information of PBCR and SINASC. The risk association variables were grouped into (i) characteristics of the child at birth and (ii) characteristics of maternal exposure during pregnancy. The case–control ratio was 1:4. Linkage was performed using R software; odds ratio (OR) and 95% confidence interval (CI) were calculated by logistic regression models.
ResultsEAL was associated with maternal occupational exposure to chemicals (agricultural, chemical, and petrochemical industry; adjOR: 2.18, 95% CI: 1.16–4.10) and with birth defects (adjOR: 3.62, 95% CI: 1.19–11.00).
ConclusionsThe results of this study, with the identification of EAL risk factors in population‐based case‐cohort study, strengthen the knowledge and improve databases, contributing to investigations on risk factors associated with childhood leukemia worldwide.
Os registros de câncer de base populacional (RCBP) e o Sistema Nacional de Nascidos Vivos (SINASC) possuem informações que possibilitam testar hipóteses sobre fatores de riscos associados às leucemias. O objetivo principal deste projeto é identificar quais as características ao nascimento das crianças que estariam associadas ao risco de desenvolver Leucemia Aguda (LA) na primeira infância.
MétodosForam utilizadas informações de 12 RCBP e do Sistema de Informação de Nascidos Vivos das mesmas localidades. Foram elegíveis 272 casos e 1.088 controles no período de 1996 a 2010. As associações de riscos de LA foram agrupadas em, (i) características da criança ao nascer, e (ii) características de exposição materna durante a gestação da criança. A relação de casos e controles foi de 1:4. As análises para padronização, estruturação do banco de dados e análises estatísticas foram realizadas através dos aplicativos Excel, R‐Studio e SPSS 21.
ResultadosHouve associação entre anomalias congênitas (RC 3,62, IC95% 1,19‐11,00) e exposição ocupacional materna a produtos químicos (OR 2,18, p 0,002) com o risco do desenvolvimento de LA.
ConclusãoA utilização de banco de dados secundários populacionais para a identificação de fatores de risco para LA fortaleceu o intercâmbio de conhecimentos e melhoria das bases de dados, e contribuiu para investigações sobre as associações de riscos nas leucemias agudas em contexto mundial.
A leucemia é a malignidade mais comum do mundo diagnosticada em crianças com menos cinco anos de idade. A taxa de incidência de leucemia linfoblástica aguda (LLA) possui um pico acentuado entre 2 e 4 anos de idade no diagnóstico e tende a afetar mais meninos que meninas.1 A etiologia da leucemia na infância permanece um desafio, apesar da premissa de que a leucemia na primeira infância (LPI) surge de células clonais somáticas originadas durante a vida fetal e incentiva a pesquisa com relação a fatores associados a exposições ambientais.1
O conceito de causalidade tem sido estabelecido com base em comprovações da necessidade de hipóteses testadas e comprovadas adicionais. Isso é especialmente verdadeiro nas ciências de saúde pública e sociais. Para leucemia na infância, um modelo de estudo causal deve levar em consideração que as leucemias possuem subtipos diferentes, biológicos e que dependem da idade e, acima de tudo, uma patogênese sistemática. Algumas características perinatais, como peso ao nascer, ordem de nascimento, tipo de parto, idade materna e exposição ocupacional materna, têm sido associadas a leucemia na infância em estudos caso‐controle.2–6 Como os estudos de caso‐controle clássicos podem ser ineficientes no caso de doenças raras, como leucemia na infância nos dois primeiros anos de vida (LPI), uma alternativa metodológica é combinar um estudo caso‐controle em uma coorte. Nosso objetivo foi investigar as características maternas e ao nascimento associadas a fatores de risco de LPI utilizando um modelo de caso‐coorte. As variáveis foram avaliadas por meio das informações coletadas de registros secundários de base populacional.
Materiais e métodosModelo do estudoFoi realizado um estudo caso‐coorte de base populacional. Os casos e controles foram obtidos de 12 Registros de Câncer de Base Populacional (RCBP) e do Sistema de Informações sobre Nascidos Vivos (SINASC) da mesma cidade dos RCBP. Essa estratégia possibilita que todos os indivíduos da base populacional tenham a mesma probabilidade de serem selecionados para formar o grupo de controle, independentemente de quando os dados foram coletados.
DadosInicialmente, foi identificado um total de 372 casos de leucemia de 12 cidades dos RCBP: Aracaju, Belém, Belo Horizonte, Cuiabá, Curitiba, Fortaleza, João Pessoa, Manaus, Natal, Porto Alegre, Recife, e Vitoria, com informações disponíveis ao longo do período (2000‐2009). Os critérios de inclusão foram: nascimento da criança após o ano de 2000, idade entre 0 a 5 anos com diagnóstico confirmado de leucemia aguda (Leucemia Linfoblástica Aguda – LLA; Leucemia Mieloide Aguda – LMA e Leucemia Não Especificada – LNE) feito entre 2000 e 2009.
Os controles foram obtidos do Sistema de Informações sobre Nascidos Vivos (SINASC), nas mesmas cidades dos casos e também nascidos após o ano de 2000 (n = 5, 623, 179). Quatro controles por caso foram escolhidos utilizando a amostragem aleatória sistemática dos dados SINASC por ordem de nascimento, ano e sexo. A base de dados do SINASC foi acessada para seleção de controles elegíveis, bem como para obtenção das informações de gravidez e perinatais de casos e controles. Gravidezes múltiplas foram excluídas do estudo (n = 104, 757; 1,9%).
As características no nascimento analisadas foram sexo, raça/cor da pele, idade materna, escolaridade materna, trabalho materno durante a gestação da criança, ordem de nascimento da criança, tipo de parto, idade gestacional (semanas) no nascimento, índice de Apgar aos 5 minutos, peso ao nascer, crescimento fetal e defeitos congênitos (CID‐10).
A idade materna foi avaliada como variável contínua com unidades de intervalos de 5 anos e uma variável categórica com dois níveis (< 30 e ≥ 30). A exposição ocupacional materna foi classificada em uma variável categórica com três níveis: 1) não trabalha, definido como mães e estudantes que ficam em casa; 2) produtos químicos, definido como trabalhadoras no setor agrícola, de produtos químicos e petroquímico e 3) outros, não especificado de outra forma (LNE). A ordem de nascimento foi calculada a partir do número de gravidezes anteriores, contando crianças vivas e mortas mais um. Os índices de Apgar de cinco minutos foram categorizados em dois níveis: ≤ 8 e > 8. O peso ao nascer foi avaliado como variável contínua com unidades de 500g e 1.000g e variável categórica com dois níveis (≤ 3.000g e > 3.000g). Sexo, peso ao nascer e idade gestacional foram utilizados para classificar por peso em categorias de idade gestacional. Grande para idade gestacional (GIG) foi definido como peso ao nascer acima do percentil específico de 90 para sexo e idade gestacional; pequeno para idade gestacional (PIG) foi definido como peso ao nascer abaixo do percentil de 10; e adequado para idade gestacional (AIG) foi definido como peso entre os percentis de 10 e 90. Uma grande coorte de nascimento publicada de percentis de peso ao nascer na população brasileira foi utilizada como referência para essas categorias.7
Análise estatísticaFoi feito um estudo caso‐coorte de ligação de registro com as bases de dados dos RCBP e do SINASC. Como essas duas bases de dados não possuem um único identificador, foi necessário utilizar a ligação de dados probabilísticos utilizando as variáveis presentes nas duas bases de dados e para utilizar diferentes combinações para comparar e bloquear variáveis de exclusão. Todos os detalhes dessa metodologia foram descritos em outro lugar.8 Foi utilizado o software R (R Foundation for Statistical Computing, Vienna, Austria). O algoritmo probabilístico foi utilizada para identificar registros relacionados a indivíduos únicos em ambas as bases de dados combinadas. O nome da mãe foi a principal variável, o algoritmo Soundex (Brasil) foi utilizado para comparação fonética e a distância Levenshtein foi utilizada para comparar strings (ht**tp://CRAN.R‐project.org/package=soundexBR). Utilizando essa metodologia de ligação de registros, foram identificados 272 casos, representando 73% dos casos de LPI nos RCBP. 100 casos foram excluídos, porém não houve diferenças estatísticas no sexo, raça e subtipo de leucemia em comparação a 272 casos de LPI.
Foi realizada a análise de regressão logística incondicional com o SPSS (IBM Corp. Released 2012. IBM SPSS Statistics para Windows, versão 21.0. NY, EUA) para calcular as razões de chance (RC) e os intervalos de confiança (IC) de 95% para avaliar a associação entre sexo, idade materna, escolaridade materna, trabalho materno durante a gestação da criança, ordem de nascimento, idade gestacional (semanas), tipo de parto, índice de Apgar aos 5 minutos, peso ao nascer, crescimento fetal, anomalias ao nascimento e LPI. Foram feitas análises separadas para LLA, LMA e LNE. Qualquer achado univariado com valor de p < 0,20 foi tratado como possível fator de confusão e utilizado para ajustar outros achados.
ÉticaO estudo foi aprovado pelo Comitê de Ética em Pesquisa do Instituto Nacional de Câncer José Alencar Gomes da Silva, referência: 10856213.0.0000.5274.
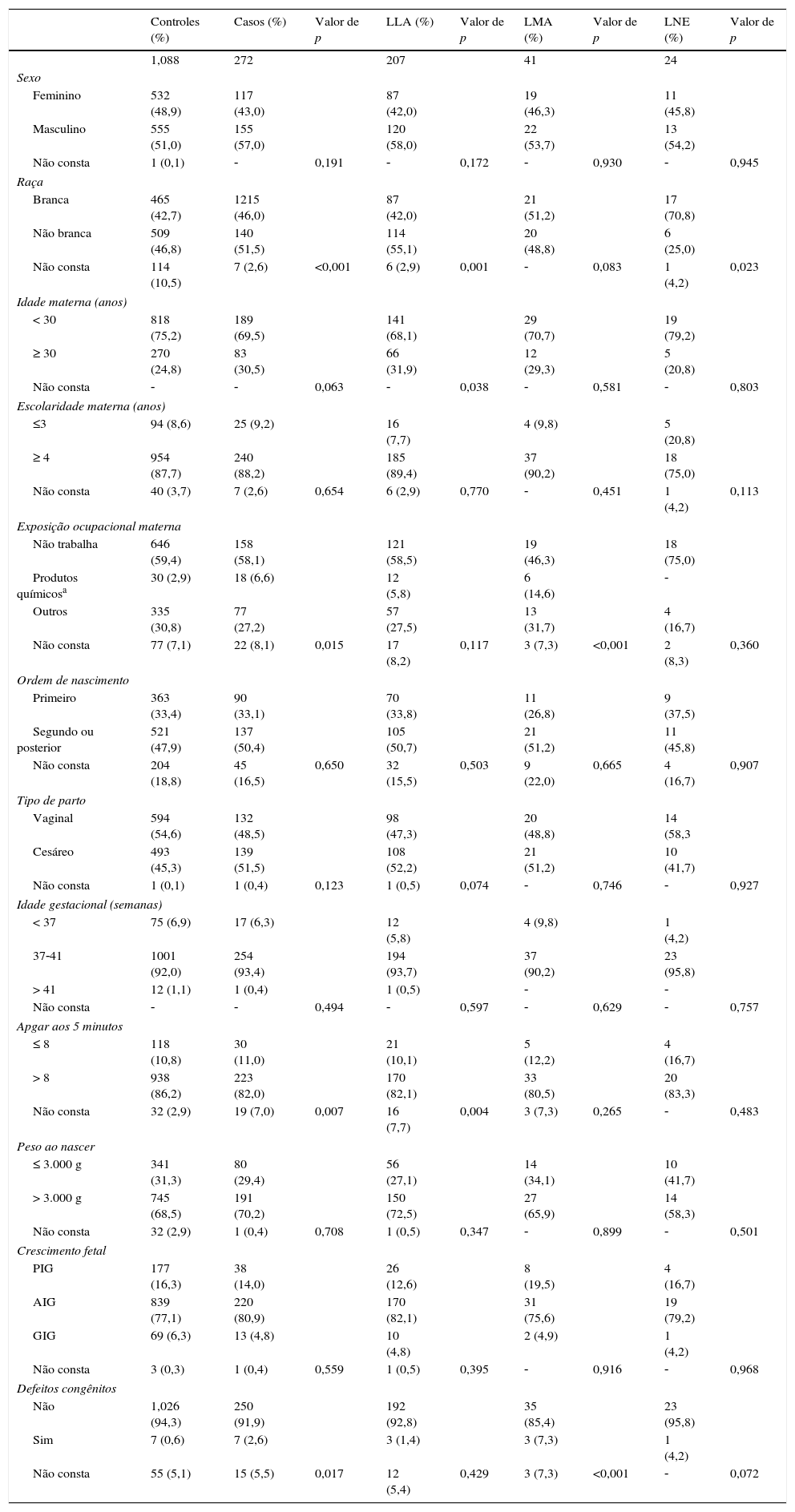
ResultadosAs distribuições de frequências de variáveis maternas e perinatais entre os casos e controles, incluindo características sociodemográficas e gestacionais, são apresentadas na tabela 1. Houve 207 casos de LLA, 41 casos de LMA e 24 casos de LME‐AL e 1.088 controles de acordo com a distribuição de 12 RCBP selecionados.
Distribuições de frequências das características maternas e perinatais de casos e controles, Brasil, 2000‐2009
| Controles (%) | Casos (%) | Valor de p | LLA (%) | Valor de p | LMA (%) | Valor de p | LNE (%) | Valor de p | |
|---|---|---|---|---|---|---|---|---|---|
| 1,088 | 272 | 207 | 41 | 24 | |||||
| Sexo | |||||||||
| Feminino | 532 (48,9) | 117 (43,0) | 87 (42,0) | 19 (46,3) | 11 (45,8) | ||||
| Masculino | 555 (51,0) | 155 (57,0) | 120 (58,0) | 22 (53,7) | 13 (54,2) | ||||
| Não consta | 1 (0,1) | ‐ | 0,191 | ‐ | 0,172 | ‐ | 0,930 | ‐ | 0,945 |
| Raça | |||||||||
| Branca | 465 (42,7) | 1215 (46,0) | 87 (42,0) | 21 (51,2) | 17 (70,8) | ||||
| Não branca | 509 (46,8) | 140 (51,5) | 114 (55,1) | 20 (48,8) | 6 (25,0) | ||||
| Não consta | 114 (10,5) | 7 (2,6) | <0,001 | 6 (2,9) | 0,001 | ‐ | 0,083 | 1 (4,2) | 0,023 |
| Idade materna (anos) | |||||||||
| < 30 | 818 (75,2) | 189 (69,5) | 141 (68,1) | 29 (70,7) | 19 (79,2) | ||||
| ≥ 30 | 270 (24,8) | 83 (30,5) | 66 (31,9) | 12 (29,3) | 5 (20,8) | ||||
| Não consta | ‐ | ‐ | 0,063 | ‐ | 0,038 | ‐ | 0,581 | ‐ | 0,803 |
| Escolaridade materna (anos) | |||||||||
| ≤3 | 94 (8,6) | 25 (9,2) | 16 (7,7) | 4 (9,8) | 5 (20,8) | ||||
| ≥ 4 | 954 (87,7) | 240 (88,2) | 185 (89,4) | 37 (90,2) | 18 (75,0) | ||||
| Não consta | 40 (3,7) | 7 (2,6) | 0,654 | 6 (2,9) | 0,770 | ‐ | 0,451 | 1 (4,2) | 0,113 |
| Exposição ocupacional materna | |||||||||
| Não trabalha | 646 (59,4) | 158 (58,1) | 121 (58,5) | 19 (46,3) | 18 (75,0) | ||||
| Produtos químicosa | 30 (2,9) | 18 (6,6) | 12 (5,8) | 6 (14,6) | ‐ | ||||
| Outros | 335 (30,8) | 77 (27,2) | 57 (27,5) | 13 (31,7) | 4 (16,7) | ||||
| Não consta | 77 (7,1) | 22 (8,1) | 0,015 | 17 (8,2) | 0,117 | 3 (7,3) | <0,001 | 2 (8,3) | 0,360 |
| Ordem de nascimento | |||||||||
| Primeiro | 363 (33,4) | 90 (33,1) | 70 (33,8) | 11 (26,8) | 9 (37,5) | ||||
| Segundo ou posterior | 521 (47,9) | 137 (50,4) | 105 (50,7) | 21 (51,2) | 11 (45,8) | ||||
| Não consta | 204 (18,8) | 45 (16,5) | 0,650 | 32 (15,5) | 0,503 | 9 (22,0) | 0,665 | 4 (16,7) | 0,907 |
| Tipo de parto | |||||||||
| Vaginal | 594 (54,6) | 132 (48,5) | 98 (47,3) | 20 (48,8) | 14 (58,3 | ||||
| Cesáreo | 493 (45,3) | 139 (51,5) | 108 (52,2) | 21 (51,2) | 10 (41,7) | ||||
| Não consta | 1 (0,1) | 1 (0,4) | 0,123 | 1 (0,5) | 0,074 | ‐ | 0,746 | ‐ | 0,927 |
| Idade gestacional (semanas) | |||||||||
| < 37 | 75 (6,9) | 17 (6,3) | 12 (5,8) | 4 (9,8) | 1 (4,2) | ||||
| 37‐41 | 1001 (92,0) | 254 (93,4) | 194 (93,7) | 37 (90,2) | 23 (95,8) | ||||
| > 41 | 12 (1,1) | 1 (0,4) | 1 (0,5) | ‐ | ‐ | ||||
| Não consta | ‐ | ‐ | 0,494 | ‐ | 0,597 | ‐ | 0,629 | ‐ | 0,757 |
| Apgar aos 5 minutos | |||||||||
| ≤ 8 | 118 (10,8) | 30 (11,0) | 21 (10,1) | 5 (12,2) | 4 (16,7) | ||||
| > 8 | 938 (86,2) | 223 (82,0) | 170 (82,1) | 33 (80,5) | 20 (83,3) | ||||
| Não consta | 32 (2,9) | 19 (7,0) | 0,007 | 16 (7,7) | 0,004 | 3 (7,3) | 0,265 | ‐ | 0,483 |
| Peso ao nascer | |||||||||
| ≤ 3.000 g | 341 (31,3) | 80 (29,4) | 56 (27,1) | 14 (34,1) | 10 (41,7) | ||||
| > 3.000 g | 745 (68,5) | 191 (70,2) | 150 (72,5) | 27 (65,9) | 14 (58,3) | ||||
| Não consta | 32 (2,9) | 1 (0,4) | 0,708 | 1 (0,5) | 0,347 | ‐ | 0,899 | ‐ | 0,501 |
| Crescimento fetal | |||||||||
| PIG | 177 (16,3) | 38 (14,0) | 26 (12,6) | 8 (19,5) | 4 (16,7) | ||||
| AIG | 839 (77,1) | 220 (80,9) | 170 (82,1) | 31 (75,6) | 19 (79,2) | ||||
| GIG | 69 (6,3) | 13 (4,8) | 10 (4,8) | 2 (4,9) | 1 (4,2) | ||||
| Não consta | 3 (0,3) | 1 (0,4) | 0,559 | 1 (0,5) | 0,395 | ‐ | 0,916 | ‐ | 0,968 |
| Defeitos congênitos | |||||||||
| Não | 1,026 (94,3) | 250 (91,9) | 192 (92,8) | 35 (85,4) | 23 (95,8) | ||||
| Sim | 7 (0,6) | 7 (2,6) | 3 (1,4) | 3 (7,3) | 1 (4,2) | ||||
| Não consta | 55 (5,1) | 15 (5,5) | 0,017 | 12 (5,4) | 0,429 | 3 (7,3) | <0,001 | ‐ | 0,072 |
LLA, Leucemia Linfoblástica Aguda; LMA, Leucemia Mieloide Aguda; LNE, Leucemia não especificada.
Os defeitos congênitos foram predominantes nos subtipos de LMA (p = 0,07). Sete casos apresentaram defeitos congênitos (Q35.9 – Fissura Palatina, LNE, Q66.1 – Talipes calcaneovarus, Q79.3 – Gastrosquise, Q89.9 – Malformação Congênita, LNE e Q90.9 – Síndrome de Down, LNE), representando 2,6% de LPIs. As anomalias congênitas no grupo de controle (0,6%) foram (Q17.9 – Malformação da orelha, LNE, Q27.0 – Ausência de hipoplasia de artéria umbilical, Q37.9 – Fissura palatina com fissura labial LNE, Q54.9 ‐ Hipospadia, LNE, Q89.8 – Outras malformações congênitas especificadas e Q90.9 – Síndrome de Down, LNE).
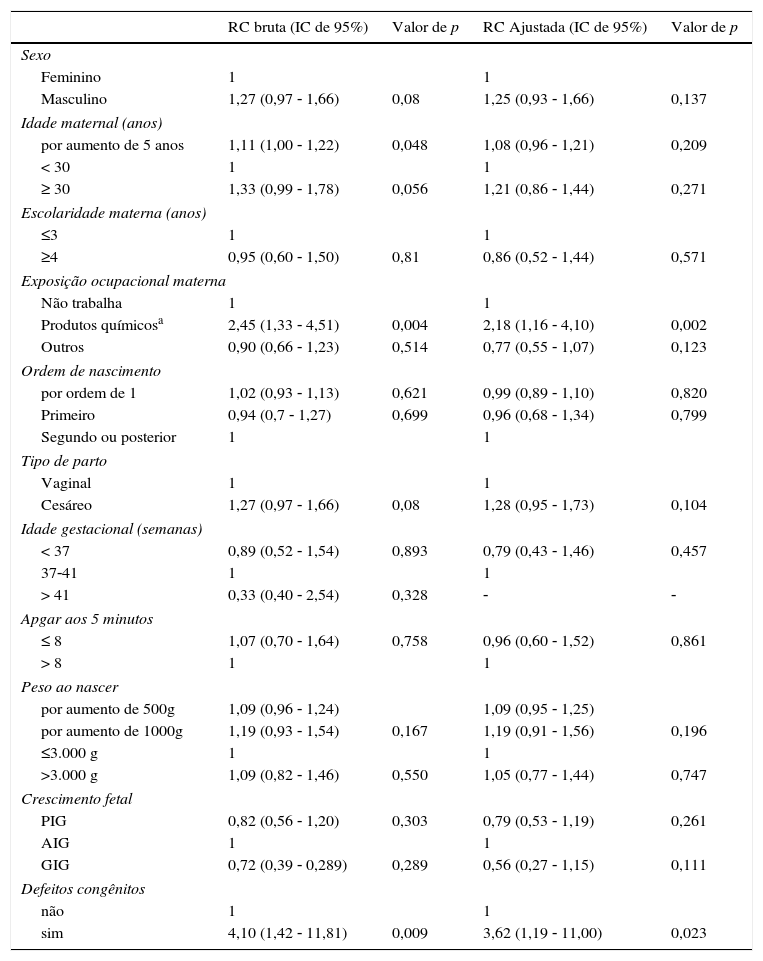
A associação entre as variáveis maternas e perinatais e a LPI são apresentadas na tabela 2, por meio de análises brutas e ajustadas [adj]. Houve aumento nas associações significativas de risco entre LPI e exposições ocupacionais maternas a produtos químicos (RCbruta = 2,45; IC de 95%: 1,33‐4,51); e defeitos congênitos (RCbruta = 4,10; IC de 95%: 1,42‐11,81). Os resultados após a análise ajustada, a exposição ocupacional materna a produtos químicos e os defeitos congênitos continuaram fortemente associados a LPI (RC[adj] = 2,18; IC de 95%: 1,16‐4,10; RC[adj] = 3,62; IC de 95%: 1,19‐11,00, respectivamente). A idade maternal foi testada como variável contínua com unidades de 5 anos (RCbruta = 1,11; IC de 95%: 1,00‐1,22, Cesárea (RCbruta = 1,28; IC de 95%: 0,95‐1,73) e o peso ao nascer possui efeitos de associação significativa estatisticamente insignificantes. A ocorrência de variáveis ausentes excluiu a variável de casos pós‐termo (> 41 semanas de gestação) da análise de ajuste, quando realizada a RC[adj].
Associação entre as características maternas e perinatais e leucemia aguda precoce, Brasil, 2000‐2009
| RC bruta (IC de 95%) | Valor de p | RC Ajustada (IC de 95%) | Valor de p | |
|---|---|---|---|---|
| Sexo | ||||
| Feminino | 1 | 1 | ||
| Masculino | 1,27 (0,97 ‐ 1,66) | 0,08 | 1,25 (0,93 ‐ 1,66) | 0,137 |
| Idade maternal (anos) | ||||
| por aumento de 5 anos | 1,11 (1,00 ‐ 1,22) | 0,048 | 1,08 (0,96 ‐ 1,21) | 0,209 |
| < 30 | 1 | 1 | ||
| ≥ 30 | 1,33 (0,99 ‐ 1,78) | 0,056 | 1,21 (0,86 ‐ 1,44) | 0,271 |
| Escolaridade materna (anos) | ||||
| ≤3 | 1 | 1 | ||
| ≥4 | 0,95 (0,60 ‐ 1,50) | 0,81 | 0,86 (0,52 ‐ 1,44) | 0,571 |
| Exposição ocupacional materna | ||||
| Não trabalha | 1 | 1 | ||
| Produtos químicosa | 2,45 (1,33 ‐ 4,51) | 0,004 | 2,18 (1,16 ‐ 4,10) | 0,002 |
| Outros | 0,90 (0,66 ‐ 1,23) | 0,514 | 0,77 (0,55 ‐ 1,07) | 0,123 |
| Ordem de nascimento | ||||
| por ordem de 1 | 1,02 (0,93 ‐ 1,13) | 0,621 | 0,99 (0,89 ‐ 1,10) | 0,820 |
| Primeiro | 0,94 (0,7 ‐ 1,27) | 0,699 | 0,96 (0,68 ‐ 1,34) | 0,799 |
| Segundo ou posterior | 1 | 1 | ||
| Tipo de parto | ||||
| Vaginal | 1 | 1 | ||
| Cesáreo | 1,27 (0,97 ‐ 1,66) | 0,08 | 1,28 (0,95 ‐ 1,73) | 0,104 |
| Idade gestacional (semanas) | ||||
| < 37 | 0,89 (0,52 ‐ 1,54) | 0,893 | 0,79 (0,43 ‐ 1,46) | 0,457 |
| 37‐41 | 1 | 1 | ||
| > 41 | 0,33 (0,40 ‐ 2,54) | 0,328 | ‐ | ‐ |
| Apgar aos 5 minutos | ||||
| ≤ 8 | 1,07 (0,70 ‐ 1,64) | 0,758 | 0,96 (0,60 ‐ 1,52) | 0,861 |
| > 8 | 1 | 1 | ||
| Peso ao nascer | ||||
| por aumento de 500g | 1,09 (0,96 ‐ 1,24) | 1,09 (0,95 ‐ 1,25) | ||
| por aumento de 1000g | 1,19 (0,93 ‐ 1,54) | 0,167 | 1,19 (0,91 ‐ 1,56) | 0,196 |
| ≤3.000 g | 1 | 1 | ||
| >3.000 g | 1,09 (0,82 ‐ 1,46) | 0,550 | 1,05 (0,77 ‐ 1,44) | 0,747 |
| Crescimento fetal | ||||
| PIG | 0,82 (0,56 ‐ 1,20) | 0,303 | 0,79 (0,53 ‐ 1,19) | 0,261 |
| AIG | 1 | 1 | ||
| GIG | 0,72 (0,39 ‐ 0,289) | 0,289 | 0,56 (0,27 ‐ 1,15) | 0,111 |
| Defeitos congênitos | ||||
| não | 1 | 1 | ||
| sim | 4,10 (1,42 ‐ 11,81) | 0,009 | 3,62 (1,19 ‐ 11,00) | 0,023 |
IC, intervalo de confiança; IC, razão de chance.
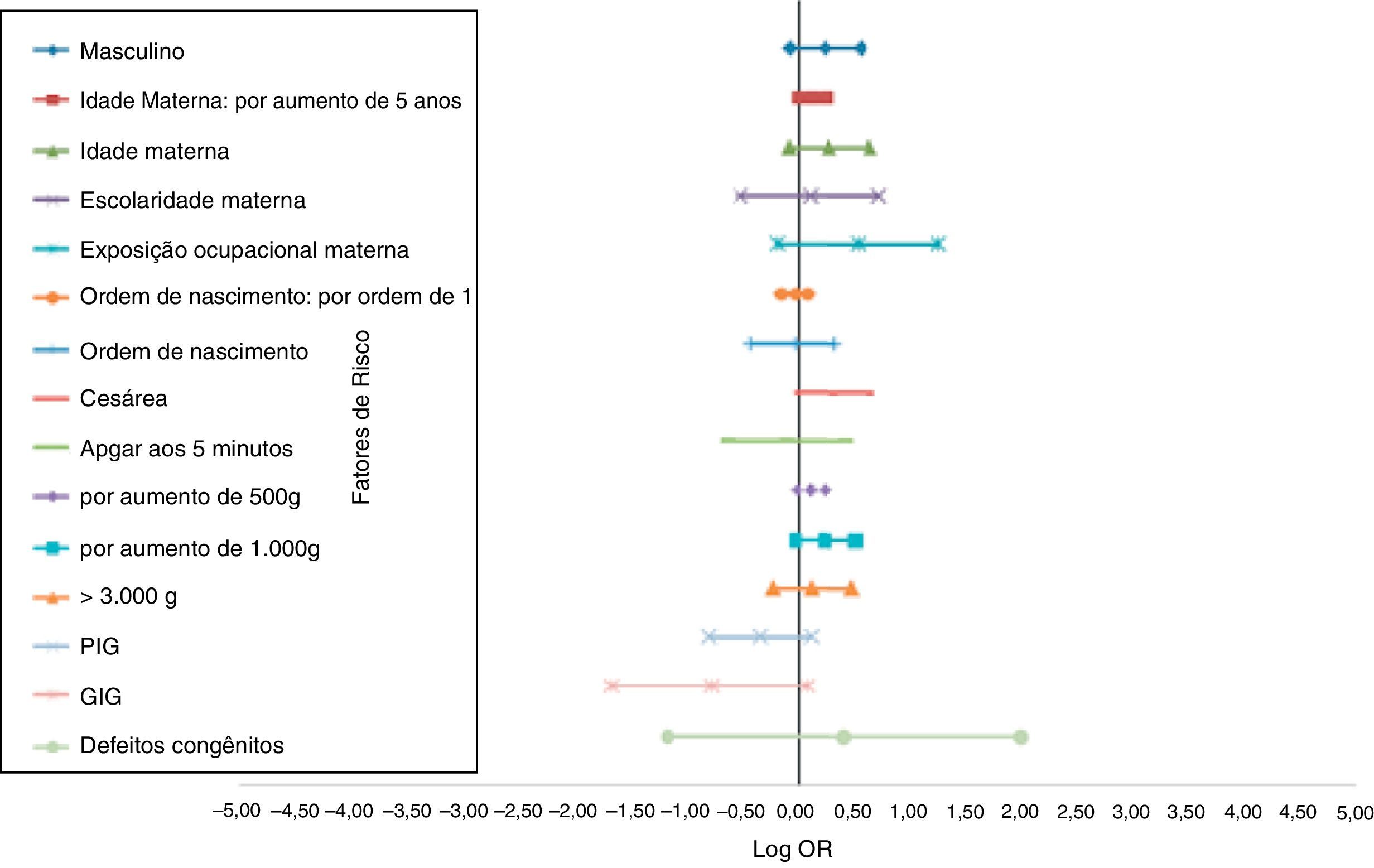
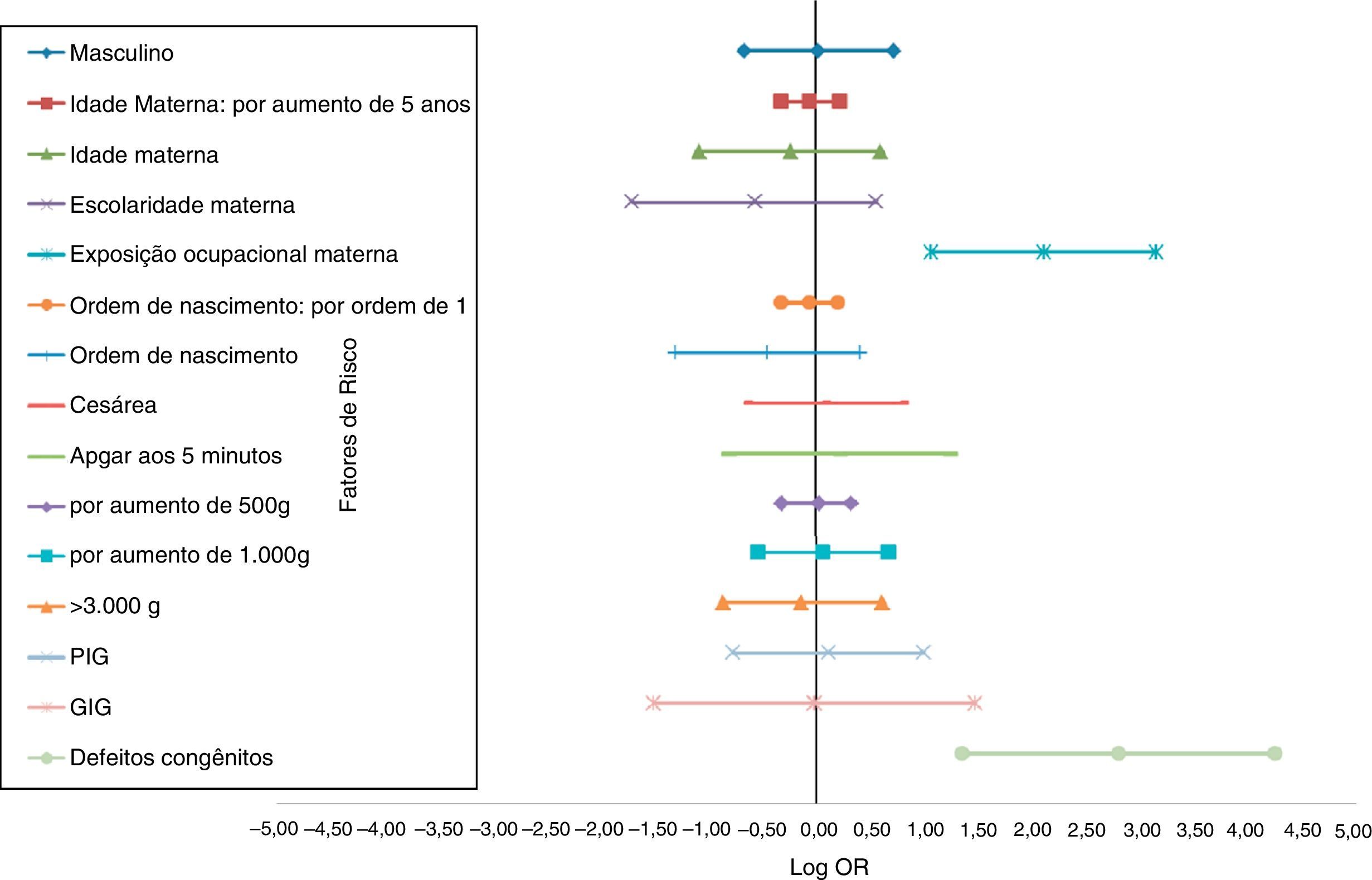
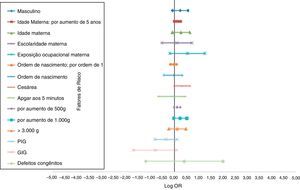
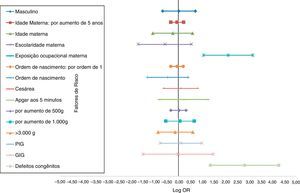
A magnitude distinta das associações de risco entre as características maternas e perinatais e a LLA está descrita na figura 1, ao passo que com LMA está mostrada na figura 2. Os fatores de risco independentes marginalmente significativos para LLA foram: sexo (RC[adj] = 1,29; IC: 0,93‐1,78; idade materna contínua (por aumento de 5 anos) (RC[adj] = 1,78; IC de 95%: 1,00‐1,30; idade materna ≥ 30 anos (RC[adj] = 1,33; IC de 95%: 0,92‐1,93; parto cesáreo (RC[adj] = 1,35; IC de 95%: 0,97‐1,89; peso ao nascer contínuo (por 500g) (RC[adj] = 1,13; IC de 95%: 0,99‐1,29; e peso ao nascer contínuo (por 1.000g) (RC[adj] = 1,28; IC de 95%: 0,98‐1,68). Entre LMA, apenas dois fatores de risco independentes foram associados: exposição ocupacional materna a produtos químicos (RC[adj] = 8,24; IC de 95%: 2,91‐23,39) e presença de defeitos congênitos (RC[adj] = 16,39; IC de 95%: 3,86‐ 69,55).
A leucemia na infância é a malignidade pediátrica mais comum e a idade de incidência de pico é entre 2 e 5 anos de idade na maior parte das populações, sugerindo um desenvolvimento iniciado dentro do útero. As características maternas e perinatais são descritas como possíveis fatores de risco.1 Foi realizado um estudo caso‐coorte de ligação de registro, no qual foram explorados os dados coletados de dois estudos de base populacional. Uma das bases de dados utilizadas, o SINASC, foi criada em 1990 e, depois de 2000, foi reconhecida como um registro de nascimento de boa qualidade com informações precisas.9 Da mesma forma, o RCBP brasileiro utilizado neste estudo é considerado de boa qualidade pela Agência Internacional de Pesquisa do Câncer (IARC); foi classificado como cobertura grupo B (cerca de 50%), com parâmetros sugeridos para análise de taxa de incidência.10 Portanto, o presente estudo com abordagem de caso‐coorte de base populacional com ligação de registro forneceu resultados confiáveis com relação aos fatores de risco associados a LPI no Brasil. As características perinatais, de ocupação maternal e mãe‐filho com relação a LPI foram exploradas neste documento.
Alguns estudos mostraram aumento no risco de leucemia na infância associado a exposições ocupacionais maternas durante a gestação, principalmente em mulheres que trabalham diretamente com atividades agrícolas ou expostas a pesticidas ou solventes.11,12 Neste estudo caso‐coorte de base populacional, foi observado um aumento na taxa de risco associado entre mães autoidentificadas como trabalhadoras nos setores agrícolas, de produtos químicos e petroquímicos. Foi encontrada magnitude de risco de 8 vezes em crianças com LMA. Esses resultados corroboram o estudo caso‐controle de base hospitalar anterior realizado que encontrou forte associação da exposição materna a pesticidas e leucemia infantil no Brasil.12
A concepção em idade maternal avançada foi descrita como fator de risco para leucemia na infância, apesar de com um resultado incompatível em alguns estudos.13,14 Na presente análise, foi encontrada uma associação significativa estatisticamente insignificante entre LPI e idade materna avaliada como variável contínua. Contudo, foi observado um risco significativo em relação a LLA (RC = 1,7). Uma possível explicação para a idade materna avançada ser suscetível a associação a LLA nos filhos pode ser a exposição de longo prazo dos gametas a agentes ambientais.15 O tipo de parto por cesárea também foi associado a LLA (HR = 1,35). Uma análise internacional combinada de estudos de caso‐controle constatou que o parto por cesárea esteve associado a LLA em hispânicos.16 Juntamente com essa comprovação epidemiológica, a escolaridade materna também parece estar associada a aumento no risco de desenvolvimento de LLA quando as mães tinham nível de escolaridade superior ao ensino médio (HR = 1,21, IC de 95%, 1,0 a 1,47) em países desenvolvidos.17 Um estudo recente, que analisou a LLA e a escolaridade materna em crianças egípcias, mostrou a associação entre o alto nível de escolaridade e o risco para LLA (RC = 2,05, IC de 95% = 1,46‐2,88).18 Utilizando a escolaridade maternal como variável secundária para o nível de indicação socioeconômica (SES‐i), houve uma associação nula entre LPI e SES‐i em todos os ambientes brasileiros de RCBP. Contudo, com base nessas informações, como comparação implícita, os resultados observados neste estudo devem ser analisados de forma prudente pelos motivos mencionados. O SES‐i com base na educação materna não é perfeito; contudo, a base de dados do SINASC possui boa completude e forte associação positiva com menor escolaridade materna (ht**tp://www.ibge.gov.br). A escolaridade maternal em casos e controles pode refletir a experiência no ambiente social de todos os participantes nesta análise.
Outras variáveis, como idade gestacional, índice de Apgar no nascimento, ordem de nascimento e peso ao nascer não foram associadas à LPI. As crianças que apresentaram baixo índice de Apgar aos 5 minutos apresentaram alguns resultados desfavoráveis de parto e variável preditora de câncer na infância, principalmente tumores sólidos, porém não com leucemia na infância.19–22
Dentre todas as características no nascimento, o peso ao nascer tem sido bem descrito como um fator de risco para LLA em idades precoces e para alguns tumores embrionários pediátricos.2–5 Apesar de o peso ao nascer não apresentar risco associado a LPI na presente investigação, em um estudo brasileiro de caso‐controle anterior, o risco de associação entre LLA e peso ao nascer foi RC = 1,30, após ajustar as variáveis de confusão como sexo, idade materna, renda familiar e exposição a pesticidas durante a gestação. Nesse modelo de estudo, os controles de base hospitalar foram utilizados na pesagem de 4.000g ou mais, de forma comparativa àqueles que nasceram com peso entre 2.500 e 2.999g.23 Para entender os possíveis mecanismos biológicos que podem explicar a ligação entre alto peso ao nascer e risco para LLA, é importante diferenciar alto peso absoluto e alto peso relativo no nascimento. O peso ao nascer ajustado à idade gestacional foi examinado primeiro para o risco de LLA de duas bases de dados da Inglaterra e não foi encontrada nenhuma associação significativa (peso ao nascer absoluto e ajustado à idade gestacional).24 Recentemente, o Consórcio Internacional sobre Leucemia Infantil – CLIC utilizando uma análise combinada de estudos de caso‐controle mostrou que crescimento fetal acelerado está associado a aumento no risco de LLA.4 Essa comprovação gera especulações sobre a função da família de genes receptores de insulina, principalmente o fator de crescimento semelhante à insulina tipo 1 (IGF‐1).Foi explorada a concentração do nível do IGF‐1 medida no sangue do cordão umbilical e positivamente associada a peso ao nascer, peso placentário e foram relatados os altos níveis de circulação do IGF‐I em neonatos com alto peso ao nascer.25,26
As crianças nascidas com defeitos congênitos representam um forte fator de risco associado para câncer na infância. A síndrome de Down é um fator de risco bem conhecido para leucemia na infância, principalmente para LMA.27,28 Em nosso estudo, foi observado um risco elevado para LMA (3 anomalias no nascimento dentre 41 casos). As três anomalias no nascimento foram síndrome de Down, fissura palatina e malformação congênita não especificada (cada).
Devemos mencionar algumas considerações com relação às limitações de nossos resultados. Em primeiro lugar, a perda de 27% dos casos não encontrados entre as ligações das duas bases de dados (RCBP/SINASC) comprometeria a interpretação dos resultados, apesar de que o efeito seria perda de poder estatístico, e não alteração no risco. Como um todo, foi descrito que 35% dos brasileiros não moram na cidade de nascimento.9,29 A explicação mais provável da perda de casos‐controles combinados é que a migração é muito comum no Brasil, devido principalmente ao fato de os pais buscarem oportunidades em cidades grandes, consequentemente com perda de resultados na cidade de nascimento. Outra limitação foi com relação a exposições ocupacionais maternas específicas consideradas de baixa completude no SINASC. A definição de categorias no SINASC e RCBP com relação à profissão segue a resolução que atualiza a Classificação Internacional Uniforme de Ocupações (ISCO‐08). A profissão é definida como um conjunto de atividades cujas principais atividades são caracterizadas por um nível elevado de similaridade na ISCO‐8, apesar de não relacionadas a exposições específicas.11 Devido ao pequeno número em cada avaliação de categorias, as variáveis do setor agrícola, de produtos químicos e petroquímicos foram coletadas em um único grupo como exposições ocupacionais a possíveis substâncias carcinogênicas. Um modelo de estudo causal deve levar em consideração os diferentes subtipos de células de leucemia infantil, e a baixa completude dessas variáveis no RCBP representa outra limitação desta análise.
Por fim, outra armadilha deste estudo é a descrição do defeito congênito no SINASC e no RCBP, que precisa de melhoria, devido ao alto número de “Malformações congênitas não especificadas” (Q89.9). Já foi descrito que as informações de ligação de um registro hospitalar mostraram ausência de relatos de categorias específicas de defeitos congênitos.28,29 Contudo, acreditamos que essa falta de definição não tenha levado a uma direção de erro diferencial em nossos resultados de fatores de risco absoluto para LPI no Brasil.
Os pontos fortes deste estudo também devem ser enfatizados. Primeiro, o modelo de caso‐coorte pressupõe que todas as variáveis foram obtidas no início do estudo (na linha de base), assim, os dados foram obtidos antes do desenvolvimento de qualquer doença. Segundo, foram utilizados os dados das duas bases de dados de base populacional de boa qualidade, o que aumenta a probabilidade de que esses achados representem fatores de risco reais. Apesar de todas as limitações mencionadas, devemos enfatizar o grande avanço deste estudo, que foi o primeiro estudo no Brasil a analisar duas bases de dados secundárias para estabelecer uma associação entre os fatores de risco e o desenvolvimento precoce de leucemia em crianças. Por fim, acreditamos que estes achados fornecem uma comprovação de que as exposições maternas durante a gravidez e as características infantis no nascimento devem ser estudadas mais profundamente como causa‐efeito de leucemogênese in utero.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Os autores são gratos a todos os coordenadores dos RCBPs e do SINASC no Brasil que contribuíram para este trabalho, incluindo aqueles em Aracaju/SE, Belém/PA, Belo Horizonte/MG, Cuiabá/MT, Curitiba/PR, Fortaleza/CE, João Pessoa/PB, Manaus/AM, Natal/RN, Porto Alegre/RS, Recife/PE e Vitória/ES.
Como citar este artigo: Reis RS, Silva NP, Santos MO, Oliveira JF, Thuler LC, de Camargo B, et al. Mother and child characteristics at birth and early age leukemia: a case‐cohort population‐based study. J Pediatr (Rio J). 2017;93:610–8.
Trabalho vinculado ao Instituto Nacional do Câncer (INCA), Centro de Pesquisa, Rio de Janeiro, RJ, Brasil.