Two randomized controlled clinical trials have shown that Lactobacillus (L) reuteri DSM 17938 reduces the duration of diarrhea in children hospitalized due to acute infectious diarrhea. This was the first trial evaluating the efficacy of L.reuteri DSM 17938 in outpatient children with acute infectious diarrhea.
MethodsThis was a multicenter, randomized, single‐blinded, case control clinical trial in children with acute watery diarrhea. A total of 64 children who presented at outpatient clinics were enrolled. The probiotic group received 1×108 CFU L. reuteri DSM 17938 for five days in addition to oral rehydration solution (ORS) and the second group was treated with ORS only. The primary endpoint was the duration of diarrhea (inhours). The secondary endpoint was the number of children with diarrhea at each day of the five days of intervention. Adverse events were also recorded.
ResultsThe mean duration of diarrhea was significantly reduced in the L. reuteri group compared to the control group (approximately 15hours, 60.4±24.5hours [95% CI: 51.0‐69.7hours] vs. 74.3±15.3hours [95% CI: 68.7‐79.9hours], p<0.05). The percentage of children with diarrhea was lower in the L. reuteri group (13/29; 44.8%) after 48 hours than the control group (27/31; 87%; RR: 0.51; 95% CI: 0.34‐0.79, p<0.01). From the 72nd hour of intervention onwards, there was no difference between the two groups in the percentage of children with diarrhea. No adverse effects related to L. reuteri were noted.
ConclusionL. reuteri DSM 17938 is effective, safe, and well‐tolerated in outpatient children with acute infectious diarrhea.
Dois ensaios clínicos randomizados controlados demonstraram que o Lactobacillus (L) reuteri DSM 17938 reduz a duração de diarreia em crianças hospitalizadas devido a diarreia infecciosa aguda. Este é o primeiro ensaio que avalia a eficácia do L. reuteri DSM 17938 em crianças com diarreia infecciosa aguda no ambulatório.
MétodosEnsaio clínico multicêntrico, randomizado, único cego, com grupos paralelos e controlado em crianças com diarreia aguda. Foram inscritas 64 crianças internadas na clínica ambulatorial. O grupo probiótico recebeu 1×108 CFU L. reuteri DSM 17938 por cinco dias, além de uma solução de reidratação oral (SRO), e o segundo grupo foi tratado apenas com SRO. O desfecho principal foi a duração da diarreia (em horas). O desfecho secundário foi o número de crianças com diarreia em cada um dos cinco dias da intervenção. Os eventos adversos também foram registrados.
ResultadosA duração média da diarreia foi significativamente reduzida no grupo L. reuteri em comparação com o grupo de controle (aproximadamente 15 horas; 60,4±24,5 horas [51,0‐69,7 horas, IC de 95%] em comparação com 74,3±15,3 horas [68,7‐79,9 horas, IC de 95%], p<0,05). O percentual de crianças com diarreia foi menor no grupo L. reuteri (13/29; 44,8%) após 48 horas do que no grupo de controle (27/31; 87%) (RR: 0,51; 0,34‐0,79; IC de 95%,<0,01). A partir da 72a hora de intervenção, não havia diferença entre os dois grupos no percentual de crianças com diarreia. Nenhum efeito adverso com relação ao L. reuteri foi observado.
ConclusãoO L. reuteri DSM 17938 é eficaz, seguro e bem tolerado por crianças com diarreia infecciosa aguda no ambulatório.
A diarreia continua sendo uma importante causa de morbidez e mortalidade em crianças em todo o mundo.1 A Sociedade Europeia de Gastroenterologia, Hepatologia e Nutrição Pediátrica (ESPGHAN) e a Sociedade Europeia de Doenças Infecciosas Pediátricas (ESPID) juntas publicaram diretrizes com base em evidências sobre a administração da gastroenterite aguda e confirmaram que a reidratação é o tratamento chave e que os probióticos selecionados poderão reduzir a duração e a intensidade de sintomas e podem ser usados como um adjuvante à solução de reidratação oral (SRO).2 Evidências atuais também indicam que os efeitos probióticos são específicos de uma cepa.3 Várias cepas da espécie Lactobacillus (L.) reuteri foram estudadas na diarreia aguda e descobriu‐se serem benéficas. A L. reuteri DSM 17938 é uma nova cepa probiótica com traços de resistência transferível para tetraciclina e lincomicina removidos da cepa original L. reuteri ATCC 55730.4 Foi anteriormente relatado que a L. reuteri DSM 17938 reduziu a duração da diarreia e o tempo de internação em crianças com necessidade de internação devido a diarreia infecciosa aguda.5 Uma metanálise recente da L. reuteri DSM 17938 em crianças com diarreia infecciosa aguda indicou a duração reduzida da diarreia e concluiu que são necessários dados ambulatoriais e análise de custo‐benefício por país.6 Este estudo é o primeiro relatório sobre os efeitos da L. reuteri DSM 17938 sobre a diarreia infecciosa aguda em uma configuração pediátrica ambulatorial.
Pacientes e métodosEste foi um ensaio clínico multicêntrico, randomizado, único cego, caso controle em crianças de ambos os sexos, com idade entre três e 60 meses, com diarreia aguda [definida como a passagem de três ou mais fezes moles ou líquidas por dia] com duração de 12 a 72 horas antes da apresentação na clínica ambulatorial. O principal investigador (ECD) não inscreveu crianças e foi cego para o tratamento dos pacientes. A aprovação para o estudo foi concedida pelo Comitê de Ética Local e o consentimento informado por escrito foi obtido dos pais das crianças. Este estudo foi registrado em clinicaltrials.gov. (NCT01927094).
As crianças presentes na clínica ambulatorial com diarreia infecciosa aguda e acompanhadas com atendimento ambulatorial foram inscritas no estudo. Os critérios de exclusão foram a exigência de internação, uso de antibióticos ou probióticos por um mês antes de um novo episódio de diarreia, desnutrição severa ou doença de base crônica grave, incluindo doenças de comprometimento imunológico.
Todas as crianças foram aleatoriamente designadas ao grupo probiótico ou de controle com o uso de uma lista de randomização gerada no computador. A randomização do bloco foi aplicada com uma lista de números aleatórios gerada no computador pelo investigador principal (ECD), que não inscreveu paciente. O primeiro grupo recebeu a intervenção destinada como cinco gotas contendo 1×108 CFU L. reuteri DSM 17938 (BioGaia®, Estocolmo, Suécia, distribuído por Eczacibasi) por cinco dias além de SRO e o segundo grupo recebeu a intervenção destinada como SRO (grupo de controle). Foi usada a SRO hipo‐osmolar (glicose 20g; sódio 60mmol/L; potássio 20mmol/L; bicarbonato 30mmol/L). O desfecho principal foi a duração da diarreia (em horas). O desfecho secundário foi o número de crianças com diarreia em cada um dos cinco dias da intervenção. Os eventos adversos também foram registrados. A duração da diarreia foi definida como o tempo em horas da internação até a cessação da diarreia, que, por sua vez, foi definida como as primeiras fezes normais de acordo com a escala de Bristol (uma escala de<5 foi considerada a normalização das fezes).
O tamanho da amostra necessário foi calculado com base na duração média da diarreia e no desvio padrão (DP) de estudos anteriores semelhantes. Com a premissa da diferença média da duração da diarreia de um dia (24horas) entre o tratamento e o grupo de controle, calculamos que uma amostra de 64 crianças seria necessária para que o estudo apresentasse um poder de 80% com um nível de significância=0,05 e sigma=2 (teste bicaudal). A análise estatística foi feita com o software SPSS, versão 16.0 (SPSS Inc., IL, EUA). As variáveis foram testadas para verificar a existência de distribuição normal e comparadas com o teste U de Mann‐Whitney e o teste t (para a diferença média) e χ2 ou testes exatos de Fisher, conforme adequado. O programa MedCalc® (Microsoft Partner Network, EUA) foi usado para calcular o risco relativo (RR). A relevância estatística foi estabelecida em p<0,05.
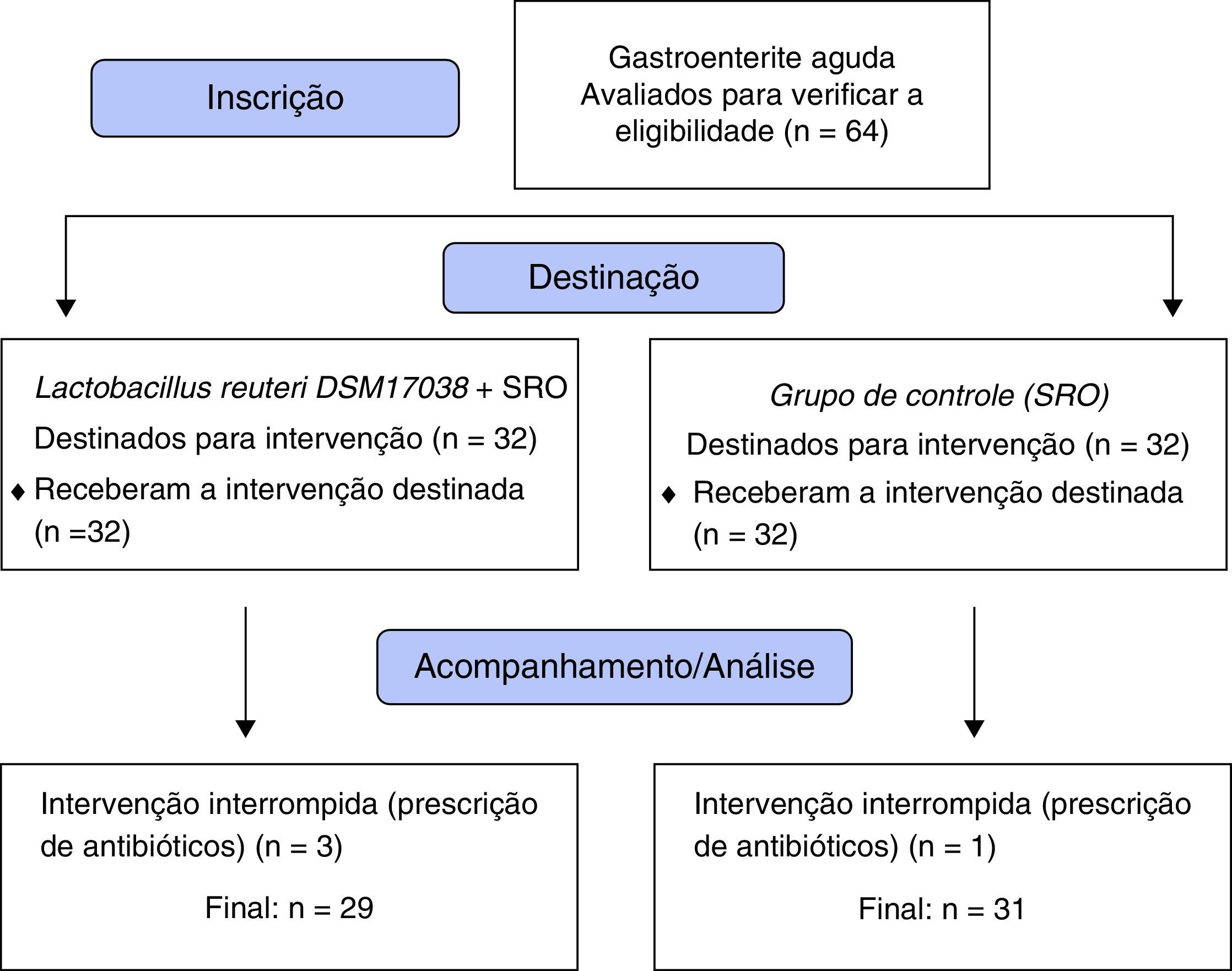
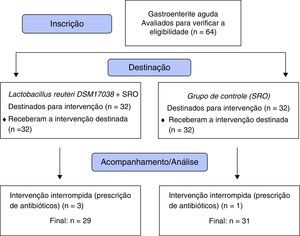
ResultadosO estudo incluiu 64 crianças. Após a exclusão de três crianças do grupo L. reuteri e uma do grupo de controle devido à prescrição antibiótica após a randomização (fig. 1), 60 crianças permaneceram para avaliação; 29 (20 do sexo masculino, nove do feminino) no grupo L. reuteri e 31 (22 do sexo masculino, nove do feminino) no grupo de controle. Os achados demográficos, a duração média da diarreia antes da intervenção e o número médio de defecações 24 horas antes da inclusão estão resumidos na tabela 1.
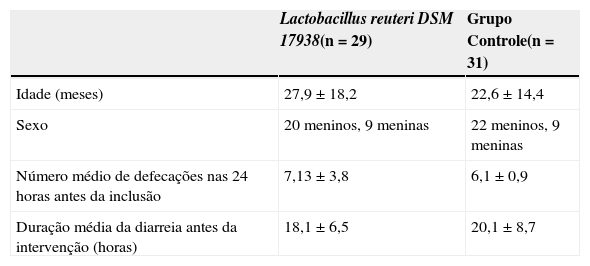
Achados demográficos e clínicos dos grupos de estudo
| Lactobacillus reuteri DSM 17938(n=29) | Grupo Controle(n=31) | |
|---|---|---|
| Idade (meses) | 27,9±18,2 | 22,6±14,4 |
| Sexo | 20 meninos, 9 meninas | 22 meninos, 9 meninas |
| Número médio de defecações nas 24 horas antes da inclusão | 7,13±3,8 | 6,1±0,9 |
| Duração média da diarreia antes da intervenção (horas) | 18,1±6,5 | 20,1±8,7 |
Valores expressos como média±DP.
A duração média da diarreia foi significativamente reduzida no grupo L. reuteri em comparação com o grupo de controle, aproximadamente 15 horas; 60,4±24,5 horas [51,0‐69,7 horas, IC de 95%] em comparação com 74,3±15,3 horas [68,7‐79,9 horas, IC de 95%], p<0,05 (tabela 2).
Duração da diarreia nos grupos de estudo
| Lactobacillus reuteri DSM 17938(n=29) | Grupo Controle(n=31) | |
|---|---|---|
| Duração da diarreia (horas) | 60,4±24,5a | 74,3±15,3 |
Valores expressos como média±DP (IC de 95%).
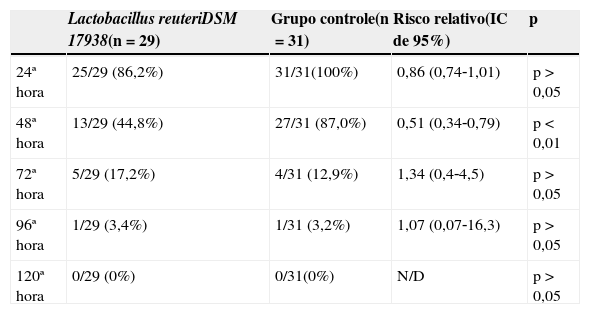
Na 48a hora do estudo, 45% das crianças que receberam L. reuteri DSM 17938 apresentaram diarreia aquosa, ao passo que esse ainda era o caso em 87% das crianças no grupo de controle (13/29; 44,8% em comparação com 27/31; 87%; RR: 0,51; 0,34‐0,79; IC de 95%,<0,01). A partir da 72a hora da intervenção, o percentual de crianças livres de diarreia entre os grupos era semelhante (tabela 3). Nenhum efeito adverso com relação ao L. reuteri DSM 17938 foi observado.
Percentual de crianças com diarreia nos grupos de estudo
| Lactobacillus reuteriDSM 17938(n=29) | Grupo controle(n=31) | Risco relativo(IC de 95%) | p | |
|---|---|---|---|---|
| 24ª hora | 25/29 (86,2%) | 31/31(100%) | 0,86 (0,74‐1,01) | p>0,05 |
| 48ª hora | 13/29 (44,8%) | 27/31 (87,0%) | 0,51 (0,34‐0,79) | p<0,01 |
| 72ª hora | 5/29 (17,2%) | 4/31 (12,9%) | 1,34 (0,4‐4,5) | p>0,05 |
| 96ª hora | 1/29 (3,4%) | 1/31 (3,2%) | 1,07 (0,07‐16,3) | p>0,05 |
| 120ª hora | 0/29 (0%) | 0/31(0%) | N/D | p>0,05 |
Os resultados deste estudo mostraram que a SRO em combinação com cinco dias de L. reuteri DSM 17938 reduziu a duração da diarreia infecciosa aguda para aproximadamente 15 horas em crianças com idade entre três e 60 meses. O efeito foi principalmente observado após 48 horas de intervenção, pois 55% das crianças no grupo de intervenção estavam livres da diarreia, ao passo que esse era o caso em apenas 13% das crianças no grupo de controle. Em um estudo anterior, feito com a mesma equipe do estudo e com o mesmo modelo, exceto pelo fato de que o estudo foi aplicado a crianças hospitalizadas, 137 crianças com idade entre 3‐60 meses foram inscritas para participar. Em crianças hospitalizadas, a administração de L. reuteri DSM 17938 reduziu a duração da diarreia significativamente para cerca de 33 horas.5 O efeito (percentual de crianças livres de diarreia) do L. reuteri DSM 17938 começou a ser observado após 24 horas de intervenção e foi maior após 48 e 72 horas. Também foi observado que o tempo médio de internação foi reduzido em mais de 24 horas no grupo com L. reuteri DSM 17938.5 Francavilla et al.7 fizeram um ensaio clínico duplo‐cego randomizado controlado por placebo em 74 crianças com idade entre seis e 36 meses com diarreia aguda, randomizadas para receber L. reuteri DSM 17938 ou placebo por sete dias, em três hospitais no sul da Itália. Comparado com o grupo placebo, o grupo L. reuteri DSM 17938 teve uma redução significativa: i) na duração da diarreia; ii) no risco de diarreia aquosa no Dia 2 e no Dia 3; e iii) no risco de recorrência de diarreia, apesar de em iv) não haver redução na duração da hospitalização.7 Szajewska et al.6 reuniram os dados decorrentes desses dois ensaios clínicos randomizados (RCT) de crianças hospitalizadas e confirmaram que o L. reuteri DSM 17938 reduziu significativamente a duração da diarreia para aproximadamente 32 horas e aumentou a chance de cura no Dia 3.6 Dois estudos independentes, um na Indonésia e um no México, mostraram que o uso profilático do L. reuteri DSM 17938 reduz a frequência e a duração dos episódios de diarreia,8,9 embora a relevância clínica possa ser questionada.10O L. reuteri DSM 17938 foi bem tolerado e nenhum evento adverso correspondente foi relatado em qualquer período de teste.6
O estudo atual tem algumas limitações, já que não foi um ensaio clínico duplo‐cego controlado por placebo. Para acessar a consistência fecal, usamos a Escala de Fezes de Bristol, que tem uma validação limitada para as crianças mais novas, apesar de oferecer um modo mais objetivo de acessar a consistência fecal, em vez de apenas basear‐se nas percepções dos cuidadores.11 A duração da diarreia foi usada como a medida principal do resultado, o que não é considerado ideal. Entretanto, há uma grande relutância dos cuidadores e prestadores de serviços de saúde em fazer a incômoda coleta de fezes. A questão da generalização de achados em ensaios clínicos, especificamente com relação à gastroenterite infecciosa e aos probióticos, é desafiadora. Entretanto, esses achados podem ser considerados generalizados, pois a gastroenterite viral ao redor do mundo é a causa mais comum. Ademais, como um estudo multicêntrico, os participantes vinham de regiões urbanas e rurais, incluindo áreas economicamente desenvolvidas e áreas pobres. Assim, esses achados têm probabilidade de permitir a generalização.
O Grupo de Trabalho sobre Probióticos da Sociedade Europeia de Gastroenterologia, Hepatologia e Nutrição Pediátrica (ESPGHAN) concluiu que o uso de L. reuteri DSM 17938 pode ser considerado uma intervenção adjunta à SRO na administração da gastroenterite aguda.3 Os probióticos podem ajudar na administração da diarreia aguda. Entretanto, o efeito é específico da cepa e a eficácia precisa ser comprovada em diferentes contextos, como o hospitalar ou o ambulatorial. Os resultados deste estudo mostraram que o L. reuteri DSM 17938 como um adjunto à terapia com SRO é eficaz no tratamento da diarreia aguda e reduz a duração da doença em um contexto ambulatorial.
Conflitos de interesseE.C. Dinleyici é palestrante e membro do conselho consultivo da Biocodex. M. Ozen é palestrante da Pfizer Consumer Health. Y. Vandenplas é consultor da Biocodex e United Pharmaceuticals. Os outros autores declaram não haver conflitos de interesse.
Como citar este artigo: Dinleyici EC, Dalgic N, Guven S, Metin O, Yasa O, Kurugol Z, et al. Lactobacillus reuteri DSM 17938 shortens acute infectious diarrhea in a pediatric outpatient setting. J Pediatr (Rio J). 2015;91:392–6.