To validate the Pediatric Obstructive Sleep Apnea Screening tool for use in Brazil.
Materials and methodsThe Brazilian version of this questionnaire, originally validated and tested in the United States, was developed as follows: (a) translation; (b) back‐translation; (c) completion of the final version; (d) pre‐testing. The questionnaire was applied prior to polysomnography to children aged 3–9 years from October 2015 to October 2016, and its psychometric properties (i.e., validity and reliability) were evaluated. The accuracy was assessed from comparisons between polysomnographic results and corresponding questionnaire scores.
ResultsSixty patients were enrolled, and based on polysomnographic findings, 48% patients had normal apnea‐hypopnea index, while the remaining 52% met the criteria for obstructive sleep apnea. Minimum O2 saturation level was obstructive sleep apnea children (p=0.021). Satisfactory concordance was found between individual apnea-hypopnea index and questionnaire scores. Bland–Altman plot‐derived bias was 0.1 for the difference between measures, with 5.34 (95% CI: 4.14–6.55) and −5.19 (95%CI: −6.39 to −3.98) for the upper and lower agreement range. Internal consistency derived from Cronbach's alpha was 0.84 (95%CI: 0.78–0.90).
ConclusionThe questionnaire was translated to and validated into Brazilian‐Portuguese version, and showed good reliability and concordance with apnea‐hypopnea index. This questionnaire offers a reliable screening option for sleep‐disordered breathing in children.
Validar o questionário Pediatric Obstructive Sleep Apnea Screening Tool para o seu uso no Brasil.
Materiais e métodosA versão brasileira desse questionário, originalmente validado e testado nos Estados Unidos, foi desenvolvida a partir das seguintes etapas: a) tradução; b) retrotradução; c) conclusão da versão final; d) pré‐teste. O questionário foi aplicado previamente ao início da polissonografia em crianças de 3 a 9 anos incluídas no estudo de outubro de 2015 a outubro de 2016. As propriedades psicométricas avaliadas foram validade e confiabilidade. A acurácia foi avaliada pela comparação entre os resultados da polissonografia com o escore do questionário.
ResultadosForam incluídos no estudo 60 pacientes. Conforme a polissonografia, 48% dos pacientes apresentaram índices de apneia e hipopneia normais e 51% apresentaram resultados alterados. A SpO2 mínima foi significativamente menor (p = 0,021) nas crianças com diagnóstico de síndrome de apneia obstrutiva do sono. O índice de apneia e hipopneia apresentou concordância satisfatória com os resultados do questionário. O viés médio de Bland‐Altman foi de 0,1 para a diferença entre as medidas, com um limite superior de 5,34 (IC95%4,14 a 6,55) e um limite inferior de ‐5,19 (IC95%‐6,39 a ‐3,98). A consistência interna do questionário avaliada pelo α de Cronbach foi de 0,84 (IC95%0,78 a 0,90).
ConclusãoO questionário foi traduzido e validado adequadamente para a versão em português brasileiro, apresentando boa confiabilidade e concordância com o índice de apneia e hipopneia. Esse questionário oferece uma opção confiável de triagem de distúrbios respiratórios do sono em crianças.
Os distúrbios respiratórios do sono (DRS) abrangem um conjunto de padrões respiratórios alterados durante o sono que incluem ronco primário, síndrome da resistência das vias aéreas superiores e síndrome da apneia obstrutiva do sono (SAOS).1 A prevalência dos DRS é estimada em torno de 4‐11% na população pediátrica.2 O principal fator de risco para o desenvolvimento dessa patologia é a hipertrofia adenotonsilar.3
O diagnóstico dos DRS e o encaminhamento para o tratamento têm como objetivo minimizar morbidades associadas, principalmente disfunções cardiológicas,4 cognitivas5 e metabólicas.6 A Academia Americana de Pediatria recomenda a polissonografia (PSG) noturna em laboratório como exame padrão‐ouro para o diagnóstico de SAOS em crianças com manifestações clínicas dos DRS.7,8 Entretanto, em países onde esse acesso à PSG é precário, as avaliações feitas a partir de questionários assumem grande importância clínica, com baixo custo operacional.9,10
Atualmente, no Brasil, existem cinco questionários validados para avaliação de distúrbios do sono em pediatria11–15 e apenas um15 apresenta validação específica para distúrbios respiratórios do sono. Porém, esse é indicado para uma faixa etária que inclui adolescentes.15 Não existe, até o momento, questionário validado para DRS específico para uso em pré‐escolares e escolares, fases da infância nas quais é sabido ocorrer um aumento da incidência desses distúrbios.
O Pediatric Obstructive Sleep Apnea Screening Tool (PosaST) é um questionário desenvolvido e validado por Gozal et al.16,17 que apresenta alta sensibilidade e moderada especificidade para diagnóstico de SAOS moderada a grave em pré‐escolares e escolares. Esse instrumento consegue discriminar crianças com maior risco para SAOS e, consequentemente, indica quem apresenta maior urgência para feitura de PSG e tratamento subsequente da patologia de base.16,17
O objetivo desse trabalho é traduzir, adaptar culturalmente e validar o PosaST, para o seu uso na população pediátrica do Brasil, uma vez que essa ferramenta tem alto potencial na suspeita de DRS, fato que adquire ainda maior importância pela dificuldade de acesso dos pacientes a exames de PSG.
Material e métodosParticipantes do estudoCrianças de três a nove anos referenciadas aos laboratórios do sono pelos seus médicos assistentes para a feitura de polissonografia por suspeita de DRS foram convidadas a participar do estudo. Os centros participantes do estudo foram: Laboratório de Neurofisiologia Clínica, do Serviço de Neurologia do Hospital São Lucas da PUC‐RS, Laboratório do Sono do Serviço de Pneumologia do Hospital de Clínicas de Porto Alegre (HCPA) e Laboratório do Sono do Hospital Mãe de Deus Center (HMDC). O recrutamento foi feito de maneira consecutiva em cada centro, de outubro de 2015 a outubro de 2016. Previamente, os responsáveis pelas crianças assinaram termo de consentimento e as crianças participantes maiores de seis anos assinaram o termo de assentimento. O uso do questionário para validação na língua portuguesa do Brasil foi autorizada pelo autor do artigo original.16,17 O estudo foi aprovado pelo Comitê de Ética e Pesquisa da PUCRS em setembro de 2015, CAAE 46804215.0.0000.5336.
Excluíram‐se pacientes com diagnóstico prévio de SAOS, pacientes com malformações craniofaciais, doenças neurológicas, síndromes genéticas ou os que não aceitaram participar do estudo.
Além da aplicação do questionário PosaST, a partir de agora denominado em português, Ferramenta de Triagem de Apneia Obstrutiva do Sono em Pediatria (FASP), os pacientes também foram avaliados quanto a dados demográficos e sua história clínica, como tempo de sono por noite, tempo do início dos sintomas, presença de doenças crônicas associadas, presença de doenças nasossinusais e uso de medicações. Fez‐se a avaliação antropométrica em todos os pacientes, o estado nutricional foi classificado de acordo com o Z‐escore do IMC com peso e idade.18 Foi considerado eutrófico quem estivesse com os valores de Z‐escore ≥ ‐2 e < +1, com sobrepeso se ≥ +1 e < +2, com obesidade se ≥ +2 e ≤ +3. Foi considerado magreza se o Z‐escore estivesse ≥ ‐3 e < ‐2.18
O questionário foi aplicado sob forma de entrevista, com duração de aproximadamente dez minutos, por técnica padronizada. Após a entrevista, os pacientes foram encaminhados para a PSG originalmente solicitada pelo seu médico assistente.
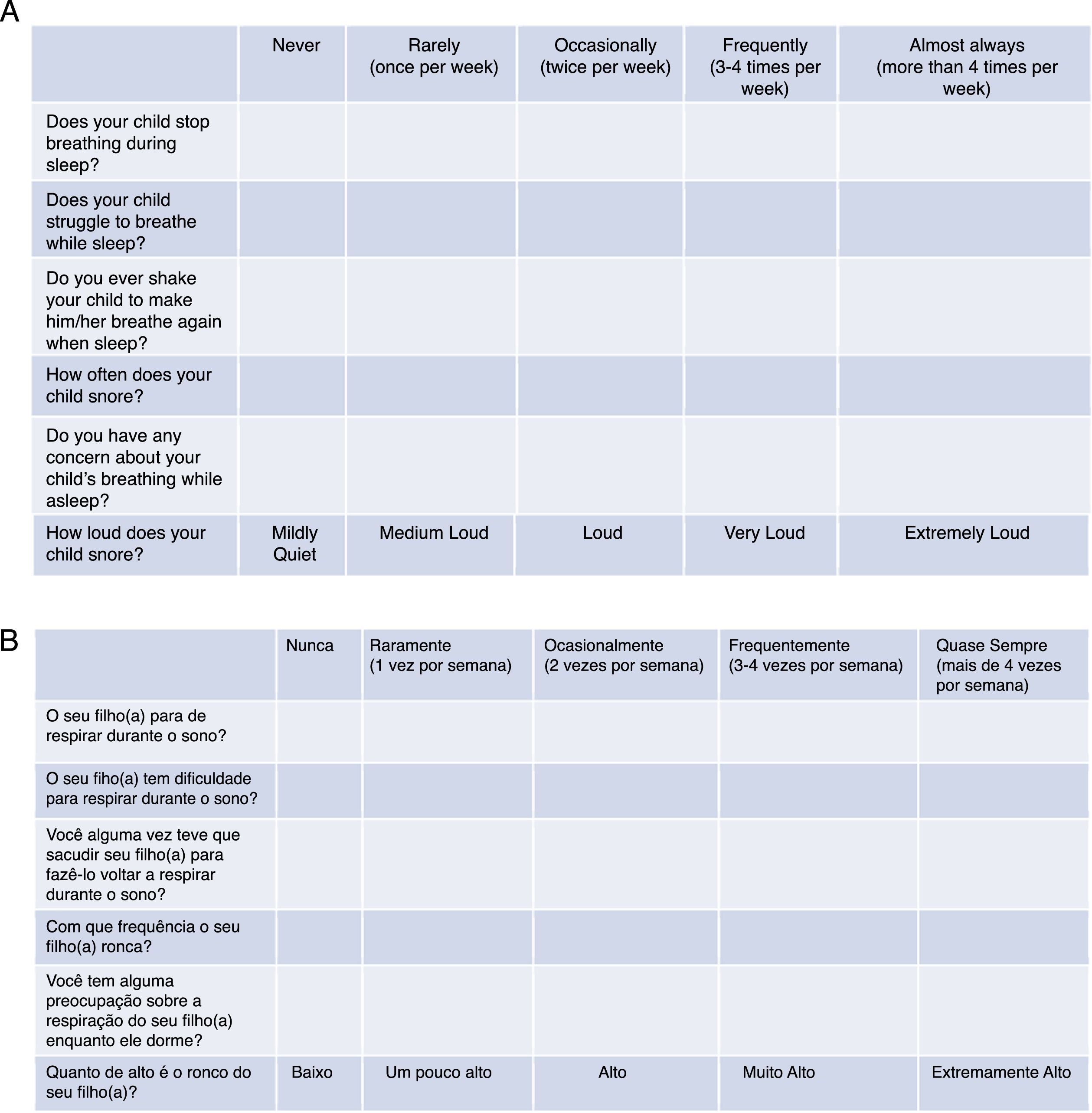
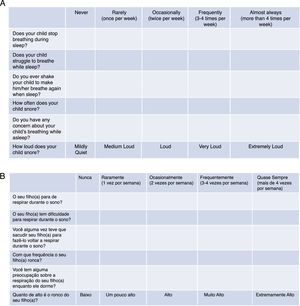
Validação do instrumentoO PosaST foi traduzido da sua versão original (fig. 1A) para o português, por dois tradutores independentes, fluentes e bilíngues na língua inglesa. As duas versões foram avaliadas e comparadas por dois revisores. Divergências em relação às questões foram modificadas de maneira a se chegar a um consenso.
A versão final em português foi retrotraduzida para o inglês por outros dois tradutores bilíngues que não participaram da etapa inicial e as divergências foram analisadas. Quando necessário as questões em português eram reescritas até uma concordância ser obtida. A versão final foi acordada com o autor principal da versão original, que tem conhecimento da língua portuguesa.
A versão final em português da FASP foi testada em um grupo de dez pais de pacientes com sintomas de DRS, randomizados nos três laboratórios de polissonografia. As seis questões necessitavam ser compreendidas por pelo menos 80% dos adultos entrevistados.13 Como houve adequada compreensão da versão final em português, nenhuma alteração necessitou ser feita e se concluiu a versão final para heteroavaliação (fig. 1B).
PolissonografiaAs polissonografias foram feitas no Laboratório de Neurofisiologia do Hospital São Lucas da PUC‐RS, no Laboratório do Sono do HCPA e no Laboratório do Sono do HMDC (respectivamente, Enza Brain‐Net 36® com software Poliwin 53, 36 canais; Brain Wave III® com software BW analysis versão 1.85, 16 canais, MF Neurovirtual/Brasil; Alice 5® com software Sleepware G3 versão 3.4.1, Philips Respironics, 16 canais. Em todos os laboratórios, a montagem do exame foi feita de acordo com as normas da Academia Americana de Medicina do Sono (AASM)19 com o uso de: eletroencefalografia, eletro‐oculograma, eletrocardiografia, eletromiografia, transdutor de pressão nasal, sensores de piezo‐cristal para identificação de esforço respiratório torácico e abdominal, sensor de ronco, sensor de posição e oximetria de pulso. Profissionais cegados laudaram os escores dos exames seguindo as orientações internacionais, com a distribuição dos estágios de sono em sono NREM (N1, N2, N3) e sono REM.19 As PSGs foram feitas à noite em sala silenciosa e escura com temperatura ambiente média de 24° C. O sono era espontâneo, sem privação prévia. Simultaneamente, as imagens do paciente eram gravadas em vídeo para auxiliar na identificação de eventos clínicos.
Os eventos respiratórios foram identificados conforme os critérios recomendados pela AASM.19 As apneias obstrutivas foram classificadas como uma cessação do fluxo de ar, associado a uma queda de ≥ 90% do sinal basal do sensor oronasal, por dois ou mais ciclos respiratórios na presença de movimentos paradoxais do abdome e do tórax. Hipopneia foi definida como uma redução do sinal do termistor de pressão nasal de ≥ 30%, com duração de dois ciclos respiratórios. O evento deveria ser associado à dessaturação de oxigênio de no mínimo 3% ou de despertar.19 Apneia central foi definida como ausência de fluxo de ar tanto pelo nariz quanto pela boca, assim como a ausência do esforço inspiratório com duração mínima de 20 segundos ou com duração de dois ciclos respiratórios, foi associada a despertares ou dessaturação de oxigênio de no mínimo 3%.19 A apneia mista foi classificada quando preenchia critérios de apneia por pelo menos dois ciclos respiratórios durante a respiração de base, foi associada à ausência de esforço respiratório durante uma porção do evento, com presença de esforço respiratório na outra parte do evento, não importava qual porção ocorresse primeiramente.19
O índice de apneia e hipopneia (IAH) foi definido como o número de apneias e hipopneias por hora do total do tempo de sono. Foram considerados como portadores de SAOS leve os pacientes que apresentaram ≥ 1,5 e < 5, SAOS moderada os que apresentaram ≥ 5 e < 10 e SAOS grave os que apresentaram ≥ 10 eventos/hora.17
A dessaturação de oxigênio foi definida como uma queda na SpO2 maior ou igual a 3% em valores sustentados menores do que 90%. No estudo, foi determinada a SpO2 na vigília, sua média durante o sono, seu nadir e a porcentagem do tempo total do sono em que a SpO2 permaneceu abaixo de 90%. Também foi determinado o índice de dessaturação ≥ 3% do basal por hora de sono.19
Avaliação das propriedades psicométricasAs propriedades psicométricas avaliadas foram validade e confiabilidade. A validade foi avaliada mediante o método de concordância de Bland‐Altman entre o questionário e o IAH. A confiabilidade foi avaliada pelo Coeficiente Alfa de Cronbach. O valor aceitável do Alfa de Cronbach foi definido em > 0,7.
Avaliação da acuráciaForam comparados pacientes com resultados normais e alterados do questionário com os resultados da PSG, com o objetivo de avaliar sua capacidade de detecção da doença.
Com relação ao questionário, foi considerado o escore cumulativo das respostas para diagnóstico provável de SAOS. O escore cumulativo é representado pela média de todas as seis questões de acordo com a seguinte fórmula (na qual Q1 corresponde à questão 1, Q2 corresponde à questão 2 e assim sucessivamente): A = (Q1+Q2)/2; B = (A+Q3)/2; C = (B+Q4)/2; D = (C+Q5)/2 e o escore cumulativo = (D+Q6)/2. Conforme a avaliação original,16,17 um escore ≥ 2,72 foi usado e considerado indicativo de alto risco para SAOS. Todas as questões foram respondidas com o uso da escala Likert: “nunca” (0), “raramente” (uma vez por semana; 1), “ocasionalmente” (duas vezes por semana; 2), “frequentemente” (três a quatro vezes por semana; 3) e “quase sempre” (mais do que quatro vezes na semana; 4). A questão que considera a intensidade do ronco foi pontuada da seguinte maneira: muito baixo: 0, um pouco alto: 1, alto: 2, muito alto: 3 e extremamente alto: 4.16
Análise estatísticaO tamanho da amostra foi estimado em 46 pacientes (23 com diagnóstico de SAOS e 23 sem). Estabelecemos nível de significância de 0,05 e poder de efeito de 90%. O software usado para o cálculo da estimativa da amostra foi o Winpepi versão 11.65.
As variáveis contínuas foram descritas em média e desvio‐padrão e aquelas com distribuição assimétrica, em mediana e intervalo interquartil (IIQ). As variáveis categóricas foram descritas em frequência absoluta e relativa. Para calcular as diferenças entre os grupos, foi usado o teste t independente para variáveis com distribuição normal e teste de Mann‐Whitney para variáveis com distribuição não normal. A acurácia do estudo avaliou a proporção de testes corretos, a partir da soma dos resultados verdadeiramente positivos e os verdadeiramente negativos sobre todos os resultados obtidos.
A definição dos pontos de corte para os índices do questionário foi obtida pela curva Receiver Operating Characteristic (ROC). Também foram registradas a sensibilidade e a especificidade para avaliação dos distúrbios. A área sob a curva foi considerada significativa quando valores ≥ 0,5 foram obtidos.
A análise e o processamento dos dados foram feitos pelo programa SPSS versão 17.
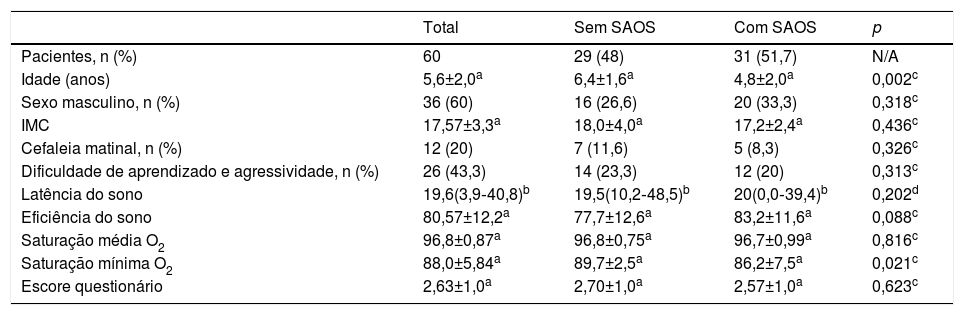
ResultadosParticipantes do estudoForam recrutados 86 pacientes para o presente estudo. Foram excluídos 21 (19 por apresentarem diagnóstico concomitante de doenças neurológicas e dois por malformações craniofaciais). Das 65 crianças incluídas, cinco foram posteriormente excluídas por não concluírem a PSG. Nesses 60 pacientes a média foi de 5,6 ± 2,0 anos, a maioria meninos, 36 (60%), e brancos, 55 (91%). A maioria dos pacientes que participaram do estudo era proveniente do HMDC (66%), seguido pela PUC‐RS (26%) e pelo HCPA (8%). A metade da amostra era eutrófica, 15 (25%) apresentavam sobrepeso e 15 (25%), diagnóstico de obesidade. Os dados clínicos e demográficos dos pacientes sem e com SAOS são apresentados na tabela 1.
Dados clínicos e demográficos dos pacientes sem e com síndrome da apneia obstrutiva do sono
| Total | Sem SAOS | Com SAOS | p | |
|---|---|---|---|---|
| Pacientes, n (%) | 60 | 29 (48) | 31 (51,7) | N/A |
| Idade (anos) | 5,6±2,0a | 6,4±1,6a | 4,8±2,0a | 0,002c |
| Sexo masculino, n (%) | 36 (60) | 16 (26,6) | 20 (33,3) | 0,318c |
| IMC | 17,57±3,3a | 18,0±4,0a | 17,2±2,4a | 0,436c |
| Cefaleia matinal, n (%) | 12 (20) | 7 (11,6) | 5 (8,3) | 0,326c |
| Dificuldade de aprendizado e agressividade, n (%) | 26 (43,3) | 14 (23,3) | 12 (20) | 0,313c |
| Latência do sono | 19,6(3,9‐40,8)b | 19,5(10,2‐48,5)b | 20(0,0‐39,4)b | 0,202d |
| Eficiência do sono | 80,57±12,2a | 77,7±12,6a | 83,2±11,6a | 0,088c |
| Saturação média O2 | 96,8±0,87a | 96,8±0,75a | 96,7±0,99a | 0,816c |
| Saturação mínima O2 | 88,0±5,84a | 89,7±2,5a | 86,2±7,5a | 0,021c |
| Escore questionário | 2,63±1,0a | 2,70±1,0a | 2,57±1,0a | 0,623c |
DP, desvio‐padrão; IAH, índice de apneia e hipopneia; IMC, índice de massa corporal.
As indicações mais frequentes para PSG foram roncos e suspeita de apneia do sono 47 (78,3%) e sono agitado 13 (21,7%). As queixas clínicas mais comuns foram respiração oral predominante, dificuldade de aprendizado, agressividade e cefaleia matinal (tabela 1).
Resultados da polissonografiaApresentaram resultados normais 29 (48%) pacientes e 31 (51,7%), alterados; 22 (36,6%) foram diagnosticados com SAOS leve, sete (11,7%) com SAOS moderada e dois (3,3%) SAOS grave. A latência para o início do sono (p = 0,161), a eficiência do sono (p = 0,088) e a saturação média de O2 (p = 0,816) não apresentaram diferença entre os grupos com e sem SAOS. A SpO2 mínima foi significativamente menor no grupo com SAOS (89,7 ± 2,5 versus 86,2 ± 7,5 p = 0,021). Ao fazer a comparação entre os dois grupos de pacientes se identificou uma diferença significativa (p = 0,046) da SpO2 mínima entre os pacientes sem SAOS e os pacientes que apresentavam SAOS moderada a grave (IAH ≥ 5). Não foi observada diferença significativa entre os pacientes sem SAOS e os pacientes com SAOS leve.
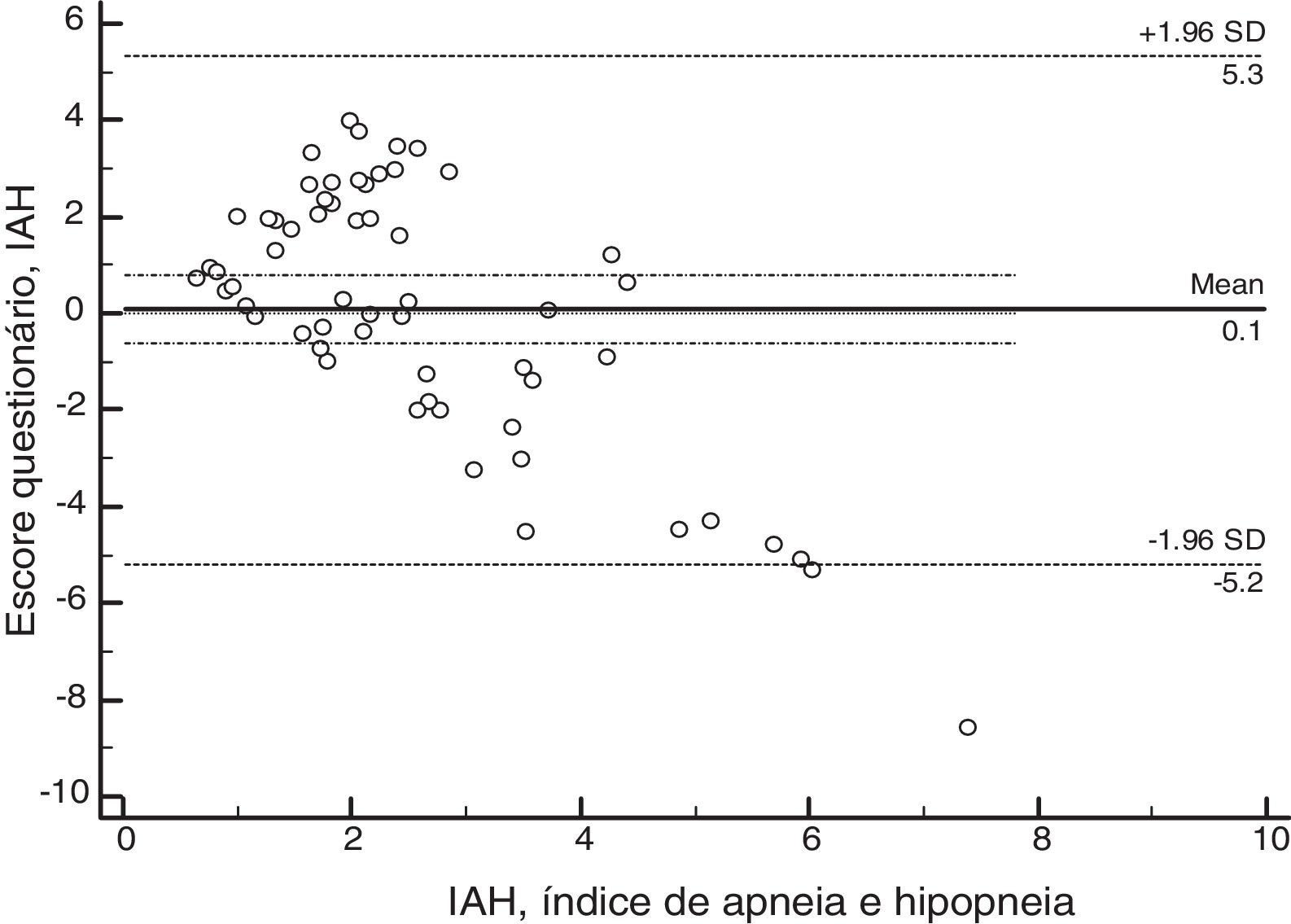
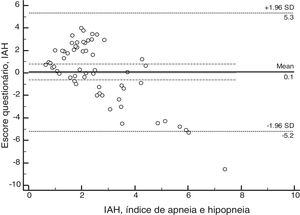
Propriedades psicométricasA análise de concordância entre os resultados do questionário e o índice de apneia e hipopneia identificou um viés médio de 0,1 para a diferença entre as medidas, com um limite superior de 5,34 (IC95% 4,14 a 6,55) e um limite inferior de ‐5,19 (IC95% ‐6,39 a ‐3,98) como pode ser avaliado pelo Gráfico Bland‐Altman (fig. 2). Esses resultados indicam que a validade foi aceitável. A consistência interna do questionário avaliada pelo α de Cronbach foi de 0,84 (IC95% 0,78‐0,90).
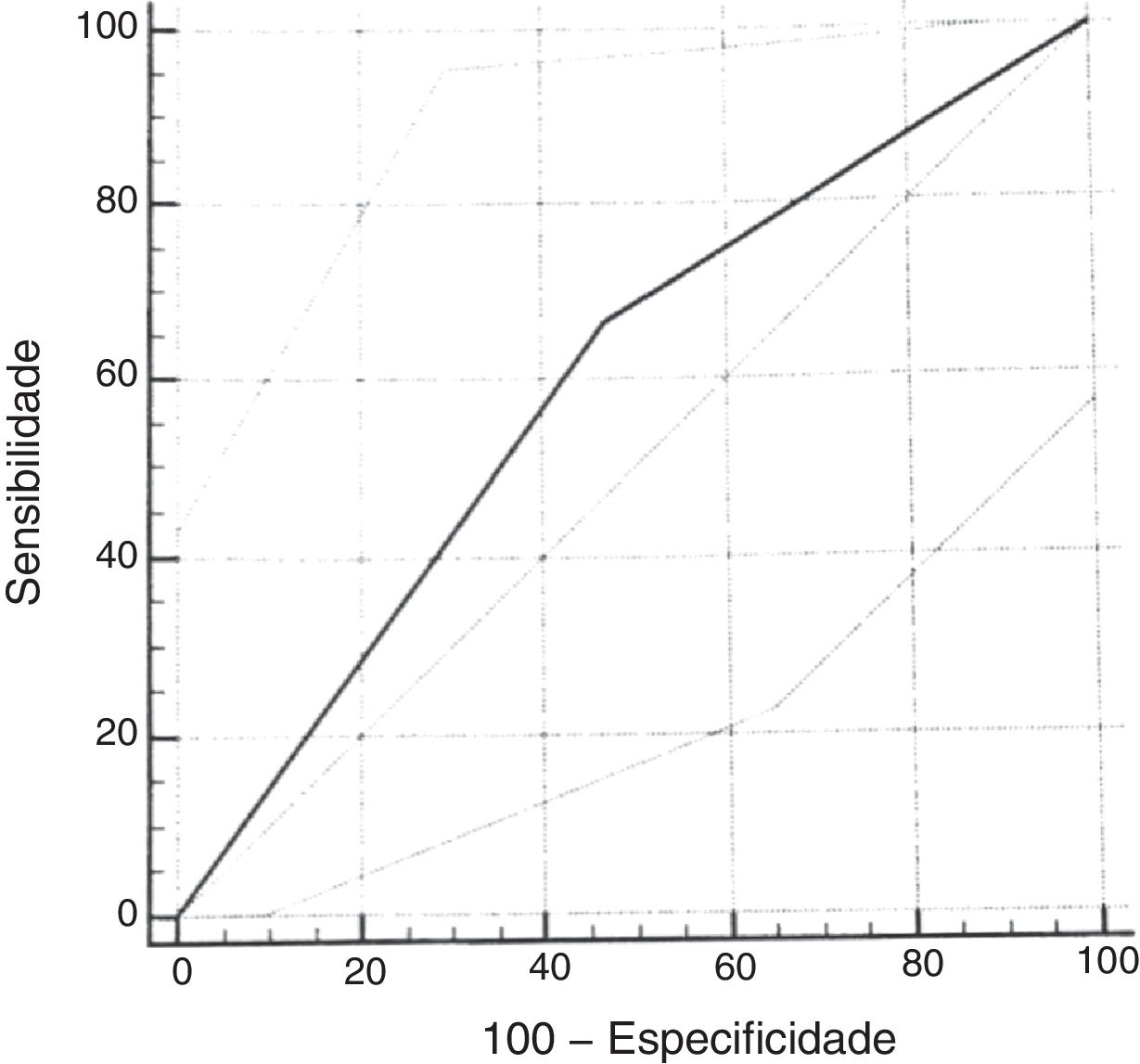
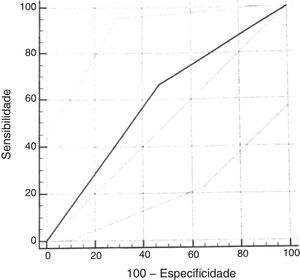
Curva ROCCom o uso do escore cumulativo ≥ 2,72da escala original, a sensibilidade para o diagnóstico de SAOS moderada ou grave (IAH ≥ 5) foi de 67% (IC95% 29,9‐92,5) e a especificidade foi de 53% (IC95% 38,5‐67,1). A análise da curva ROC mostrou uma área sob a curva de 0,598. (fig. 3)
DiscussãoO questionário PosaST foi traduzido e validado a partir do questionário original na língua inglesa para a versão em português brasileiro FASP, a qual apresentou boa confiabilidade e concordância com o índice de apneia e hipopneia numa população com alta probabilidade de SAOS.
A confiabilidade não foi calculada no estudo original,16 portanto não temos uma base para comparação entre os trabalhos, mas podemos afirmar que a confiabilidade no estudo atual foi alta a julgar pela consistência interna de 0,84. A presença de elementos básicos como uma boa confiabilidade mostra a capacidade da reprodução dos resultados ao longo do tempo em indivíduos estáveis, com sensibilidade a possíveis mudanças nos padrões de sono dos indivíduos. Esses são requisitos importantes a serem considerados na escolha de um questionário de triagem de SAOS.
Avaliamos as taxas de concordância entre o escore cumulativo do questionário e os resultados do IAH por meio da análise estatística proposta por Bland‐Altman.20 Encontramos taxas de concordância satisfatórias entre o questionário e os resultados do IAH para sujeitos com SAOS leve. Esses resultados são relevantes pois mostram que o instrumento pode ser usado para identificação de pacientes com SAOS leve, diferentemente da proposta inicial, na qual o questionário teria mostrado melhor desempenho na triagem de pacientes moderados a graves.
Essa aplicação mais ampla sinaliza a possibilidade de um uso mais abrangente da ferramenta, uma vez que o manejo da SAOS leve costuma ser diferente da SAOS moderada e grave. Estudos atuais sugerem que a opção de aguardar/acompanhar cautelosamente pela evolução dos sintomas pode ser uma opção razoável em crianças com SAOS leve, especialmente na ausência de obesidade. Já foi observado que, após sete meses de acompanhamento, até 42% dos pacientes previamente diagnosticados com sintomas leves de SAOS evoluem com resolução do quadro clínico pela normalização do exame de PSG.21 Sugere‐se que o uso de corticoide intranasal (CIN) ou de antagonistas aos leucotrienos nos pacientes classificados com SAOS leve durante esse período de acompanhamento pode auxiliar a reduzir os sintomas da SAOS.8 Outra possibilidade de terapia inicial para o tratamento de SAOS leve é a associação do CIN com montelucaste por pelo menos três meses. O uso concomitante dessas medicações já demonstrou ser uma opção efetiva à cirurgia, principalmente em pacientes não obesos e em menores de sete anos, apresentou taxas de sucesso de 80%.22 Enquanto isso, nos pacientes com SAOS moderada a grave, o encaminhamento para tratamento cirúrgico é em geral a melhor opção.10
Outros trabalhos também já usaram a análise de concordância Bland‐Altman para avaliação do sono. Werner et al. em 2008 concluíram que actigrafia e diários do sono podem ser usados para avaliação da latência do sono, do tempo para o despertar e tempo total de sono em crianças de quatro a sete anos.23 Outro estudo mais recente, de 2016, usou a análise Bland‐Altman para avaliar a concordância do teste‐reteste na versão brasileira do questionário Índice de Qualidade do Sono de Pittsburgh em adolescentes, com boa concordância nas duas aplicações do questionário.24 A aplicação do método Bland‐Altman nos nossos dados indicou que a FASP tem características satisfatórias para triagem dos pacientes sintomáticos que necessitam de encaminhamento ao estudo de polissonografia.
Assim como no trabalho original, foi calculada a curva ROC para a validação do questionário, considerou‐se o escore cumulativo ≥ 2,72. Ao usar pontos de corte do IAH de 1,0 ou 1,5 para o cálculo não foi encontrado um bom desempenho diagnóstico. Ao usar o escore cumulativo ≥ 2,72 e o IAH ≥ 5 como ponto de corte, observamos resultados ligeiramente piores do que os da escala original, com uma AUC de 0,59 (versus AUC 0,64). Foi encontrada uma menor sensibilidade (67%) e especificidade (53%) para o diagnóstico de SAOS moderada a grave do que no estudo de referência. A escolha de um escore cumulativo ≥ 2,72 está baseada em referências que usaram esse mesmo ponto de corte.16 Esse desempenho diagnóstico regular do escore cumulativo do questionário com a PSG provavelmente está relacionado ao número pequeno de pacientes com diagnóstico de SAOS moderada a grave na amostra incluída no estudo. Em estudos mais recentes de validação do questionário em outras línguas, o ponto de corte necessitou ser modificado para melhor adaptação às características clínicas da população.25
Uma limitação do estudo foi que a coleta dos dados se restringiu a pacientes referidos a laboratórios de sono, criou‐se o viés de não representar adequadamente a população pediátrica em geral. No entanto, o desenvolvimento e a validação do questionário original foram feitos em um serviço primário e, após, sua aplicabilidade foi validada em um centro de referência para sono pediátrico.16,17 Mesmo sabendo que as amostras populacionais são diferentes, como o questionário já havia sido validado em um serviço terciário optamos por coletar os dados dos pacientes nos laboratórios de PSG tal como outros estudos.25
No Brasil existe uma dificuldade na inclusão de questionários em pesquisas devido ao número reduzido dessas ferramentas que tenham passado por um processo de validação de alto rigor acadêmico. Observa‐se na literatura um número crescente de instrumentos validados, mas a qualidade dessas validações nem sempre está de acordo com os protocolos recomendados.13,26 A presença de um teste para heteroavaliação e triagem de DRS em pré‐escolares e escolares é de extrema relevância clínica, principalmente em países em desenvolvimento, onde existe uma disponibilidade reduzida de exames mais sofisticados e dispendiosos.
A FASP foi validada para identificação de pacientes pediátricos com DRS. Por ser composta de seis questões hierárquicas sobre o sono pediátrico, ela se mostrou um instrumento de triagem breve e de aplicação simples, o que facilita seu uso no dia a dia. Além disso, mostrou boa concordância para identificação de pacientes com SAOS leve, indicou quais crianças deveriam iniciar tratamento clínico e ser, ou não, encaminhadas para exames diagnósticos.
A versão brasileira do questionário PosaST apresentou um bom desempenho. Embora tenha sido validado para seu uso no Brasil, ele ainda necessita ser mais explorado no campo do sono, com sua aplicação em um maior número de pacientes, especialmente naqueles com doença mais grave. No entanto, ele se mostrou um instrumento rápido, de abordagem simples e com concordância satisfatória entre os pacientes com SAOS leve, pode ser facilmente implantado para uso clínico.
FinanciamentoCoordenação de Aperfeiçoamento do Pessoal de Nível Superior (Capes).
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Como citar este artigo: Pires PJ, Mattiello R, Lumertz MS, Morsch TP, Fagondes SC, Nunes ML, et al. Validation of the Brazilian version of the Pediatric Obstructive Sleep Apnea Screening Tool questionnaire. J Pediatr (Rio J). 2019;95:233–9.
Trabalho vinculado ao Programa de Pós‐Graduação em Pediatria e Saúde da Criança, Pontifícia Universidade Católica do Rio Grande do Sul (PUC‐RS), Porto Alegre, RS, Brasil.