to assess the use of the Brazilian criteria for reporting of hospital‐acquired infections (HAIs) in the neonatal unit and compare them with the criteria proposed by the National Healthcare Safety Network (NHSN).
Methodsthis was a cross‐sectional study conducted from 2009 to 2011. It included neonates with HAI reporting by at least one of the criteria. Statistical analysis included calculation of incidence density of HAIs, distribution by weight, and by reporting criterion. Analysis of sensitivity, specificity, positive predictive value (PPV), and negative predictive value (NPV) for the national criteria was performed considering the NHSN as the gold standard, with agreement assessed by kappa.
Resultsa total of 882 newborns were followed, and 330 had at least one infection notified by at least one of the criteria. A total of 522 HAIs were reported, regardless of the criteria. An incidence density of 27.28 infections per 1,000 patient‐days was observed, and the main topographies were sepsis (58.3%), candidiasis (15.1%), and conjunctivitis (6.5%). A total of 489 (93.7%) were notified by both criteria, eight infections were notified only by the national criteria (six cases of necrotizing enterocolitis and two cases of conjunctivitis), and 25 cases of clinical sepsis were reported by NHSN criteria only. The sensitivity, specificity, PPV, and NPV were 95.1%, 98.6%, 98.4%, and 95.7%, respectively, for all topographies, and were 91.8%, 100%, 100%, and 96.3% for the analysis of sepsis. Kappa analysis showed an agreement of 96.9%.
Conclusionthere was a high rate of agreement between the criteria. The use of the national criteria facilitates the reporting of sepsis in newborns, and can help to improve the specificity and PPV.
avaliar a aplicação dos critérios nacionais para notificação de infecções relacionadas à assistência à saúde (IRAS) em Unidade Neonatal e comparar com os critérios propostos pelo National Healthcare Safety Network (NHSN).
Métodosestudo transversal realizado de 2009 a 2011. Forma incluídos os neonatos que apresentaram notificação de IRAS por pelo menos um dos critérios. Análise estatística incluiu cálculo de densidade de incidência de IRAS e distribuição por peso e por critério de notificação. Foi realizada análise da sensibilidade, especificidade, valor preditivo positivo (VPP) e valor preditivo negativo (VPN) para os critérios nacionais, considerando o NHSN como padrão‐ouro e a concordância avaliada pelo Kappa.
Resultadosforam acompanhados 882 neonatos, e 330 apresentaram pelo menos uma infecção notificada por, no mínimo, um dos critérios. Foram notificadas 522 IRAS, independentemente do critério. Observou‐se densidade de incidência de 27,28 infecções por 1.000 pacientes‐dia, e as principais topografias foram sepse (58,3%), monilíase (15,1%) e conjuntivite (6,5%). Um total de 489 (93,7%) notificações foram por ambos os critérios; oito infecções foram notificadas apenas pelo critério nacional (duas conjuntivites e seis enterocolites necrosantes); e 25 casos de sepse clínica foram notificadas apenas pelo NHSN. A sensibilidade, especificidade, VPP e VPN foram de 95,1%, 98,6%, 98,4%, 95,7%, respectivamente, para todas as topografias, e para análise de sepse foram 91,8%, 100%, 100% e 96,3%. O Kappa revelou concordância de 96,9%.
Conclusãoverificou‐se uma elevada concordância entre os critérios. A utilização dos critérios nacionais facilita a notificação da sepse em neonatologia e podem contribuir para melhorar a especificidade e VPP.
O controle das infecções relacionadas à assistência à saúde (IRAS) representa um desafio para as equipes de saúde e administradores hospitalares, por se tratar de eventos infecciosos graves, responsáveis pela elevação da morbimortalidade, aumento dos custos e impacto social.1,2
Para o efetivo controle destes agravos, as Comissões de Controle de Infecção Hospitalar (CCIH) devem estruturar e manter um sistema de vigilância epidemiológica de IRAS, especialmente em setores críticos, como unidades de tratamento intensivo adulto, pediátrico e neonatal.3–5
A organização da vigilância epidemiológica de IRAS foi iniciada nos Estados Unidos, em 1986, quando foi implantado o National Nosocomial Infections Surveillance (NNIS), sistema de vigilância do Centro de Controle de Doenças (CDC), organizado e subdividido em componentes que incluem vigilância global, unidade de tratamento intensivo (UTI), componente cirúrgico e unidade neonatal.6
O método proposto pelo NNIS foi ampliado e revisado em 2005 e recebeu a denominação de The National Healthcare Safety Network (NHSN),7 com o estabelecimento de critérios de infecção associada a dispositivos invasivos (ventilação mecânica, cateter vascular central e sonda vesical de demora), componente de vigilância cirúrgico, introdução do componente de vigilância em diálise e a adoção do protocolo do componente de segurança para o profissional. Os critérios são revistos e novas versões do NHSN são publicadas periodicamente.7
No Brasil, o controle de IRAS foi regulamentado em 1983 pela portaria 196/1983, revogada pelas portarias 930/92 e 2616/1998.5 Desde 1994 o Ministério da Saúde adotou como recomendação o uso do método proposto pelo NNIS para a vigilância epidemiológica das IRAS nos hospitais brasileiros, com a publicação da tradução do manual. Assim, os protocolos do NHSN constituem o referencial para vigilância epidemiológica e notificação das IRAS nos hospitais brasileiros.6 O método NNIS foi adotado oficialmente pela CCIH do Hospital das Clínicas da Universidade Federal de Minas Gerais (HC/ UFMG) em 1994, direcionando a coleta de dados, o diagnóstico e a notificação das IRAS.
Desde 2008 a Agência Nacional de Vigilância Sanitária (ANVISA) vem publicando manuais que abordam definições, indicadores e estratégias de prevenção das principais infecções relacionadas à assistência à saúde. Os critérios nacionais para vigilância de IRAS em neonatologia foram publicados em 2008 e atualizados em 2010, com objetivo de padronizar a vigilância epidemiológica, direcionar ações de controle e possibilitar a comparação dos indicadores entre instituições brasileiras.8
No entanto, devido à escassez de dados nacionais consolidados publicados sobre a incidência de IRAS, especialmente em neonatologia, a monitorização destes indicadores nas instituições brasileiras, geralmente, é realizada por meio de comparações com dados americanos, obtidos por relatórios do NHSN, publicados anualmente. A utilização de critérios para vigilância epidemiológica definido pelo CDC não representa o diagnóstico da situação do controle de infecção nas instituições brasileiras.2,8
Considerando a introdução dos critérios da ANVISA para vigilância epidemiológica em neonatologia e a rotina de serviço do HC/ UFMG com utilização do método do CDC/NHSN desde 1994, é importante avaliar os avanços e contribuições da proposta nacional.
Assim, este estudo pretende avaliar a aplicação dos critérios nacionais de notificação de IRAS8 para a vigilância epidemiológica e comparar com critérios internacionais propostos pelo NHSN7, utilizados em uma Unidade Neonatal de hospital universitário de referência.
MétodosTrata‐se de estudo transversal realizado de 1° de janeiro de 2009 a 31 de dezembro de 2011, na Unidade Neonatal de Cuidados Progressivos (UNCP) do Hospital das Clínicas da Universidade Federal de Minas Gerais (HC/UFMG).
O HC/UFMG é um hospital universitário geral e público, de referência nos sistemas municipal e estadual de saúde. A vigilância é realizada, conforme legislação nacional, em pacientes de risco, que inclui recém‐nascidos de baixo peso, em uso de ventilação mecânica, com cateter venoso central, em uso de antimicrobianos para tratamento de quadro infeccioso com manifestação sistêmica e submetidos a procedimentos cirúrgicos.5,7,8
As variáveis foram coletadas por meio de busca ativa nos prontuários por profissional especializado e treinado da CCIH e registradas em banco de dados do Núcleo de Epidemiológica da referida comissão. A amostra incluiu todos os neonatos sob risco admitidos na UNCP, considerando para notificação de IRAS os critérios do NHSN7 e/ou critérios da ANVISA.8
Os dados dos pacientes e notificações de IRAS foram digitados no programa Excel 2003 e analisados no Statistical Package for the Social Sciences (SPSS), versão 13.0.
A análise estatística incluiu cálculo da densidade de incidência (DI) de infecções (número de infecções por 1.000 pacientes‐dia), distribuição de IRAS por faixa de peso e por critério de vigilância e notificação. A sensibilidade, especificidade, valor preditivo positivo (VPP) e valor preditivo negativo (VPN) foram calculados para os critérios propostos pela ANVISA,8 considerando os critérios definidos pelo NHSN7 como padrão‐ouro, para o número total de IRAS e uma análise exclusiva para casos notificados de sepse, uma vez que esta representou a maioria das infecções em que foi utilizado apenas um dos critérios para notificação de IRAS.
Para a análise da concordância entre os métodos foi utilizada a medida do Kappa, que é baseada no número de respostas concordantes para além do que seria esperado pelo acaso.9
O Kappa varia de ‐1 (ausência total de concordância) até+1 (concordância total). Valores de Kappa acima de 0,75 são considerados para uma concordância excelente, entre 0,4 e 0,75 boa, e abaixo de 0,4 a concordância é considerada fraca.9
O projeto foi aprovado pelo Comitê de Ética em Pesquisa do HC/UFMG, conforme parecer COEP: ETIC 312/08. Não há qualquer procedimento que possa interferir nas ações assistenciais e as rotinas da UNCP do HC/UFMG.
ResultadosUm total de 882 pacientes foi admitido na UNCP, totalizando 19.137 pacientes‐dia, e 330 recém‐nascidos apresentaram pelo menos um episódio de infecção notificada por pelo menos um dos critérios.
Foi notificado um total de 522 episódios de IRAS independentemente do critério, com densidade de incidência (DI) de 27,28 infecções/1.000 pacientes‐dia. Dos pacientes acompanhados pela vigilância epidemiológica (n=882), 73,8% encontravam‐se na faixa de peso acima de 1.501 gramas; entretanto, a DI e o percentual de pacientes com IRAS apresentaram‐se mais elevados na faixa de peso abaixo de 750 gramas em comparação com as demais (p<0,001). A quantidade total de pacientes, número de IRAS e densidade de incidência foram apresentados por faixa de peso na tabela 1.
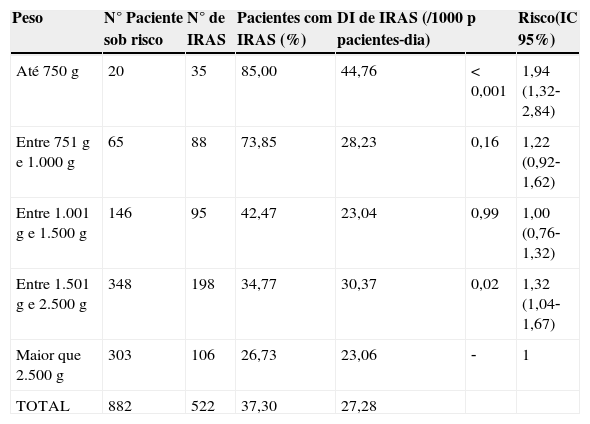
IRAS por estratificação de peso ao nascimento, UNCP, HC/UFMG, 2009 a 2011
| Peso | N° Paciente sob risco | N° de IRAS | Pacientes com IRAS (%) | DI de IRAS (/1000 pacientes‐dia) | p | Risco(IC 95%) |
|---|---|---|---|---|---|---|
| Até 750 g | 20 | 35 | 85,00 | 44,76 | <0,001 | 1,94 (1,32‐2,84) |
| Entre 751g e 1.000 g | 65 | 88 | 73,85 | 28,23 | 0,16 | 1,22 (0,92‐1,62) |
| Entre 1.001g e 1.500 g | 146 | 95 | 42,47 | 23,04 | 0,99 | 1,00 (0,76‐1,32) |
| Entre 1.501g e 2.500 g | 348 | 198 | 34,77 | 30,37 | 0,02 | 1,32 (1,04‐1,67) |
| Maior que 2.500 g | 303 | 106 | 26,73 | 23,06 | ‐ | 1 |
| TOTAL | 882 | 522 | 37,30 | 27,28 |
IRAS, infecções relacionadas à assistência à saúde; DI, densidade de incidência de IRAS; UNCP, Unidade Neonatal de Cuidados Progressivos; IC, intervalo de confiança.
Foi preenchido um total de 522 notificações de IRAS em 17 topografias diferentes, independentemente do critério de vigilância utilizado. A sepse foi a complicação infecciosa mais frequente, com 305 casos (58,3%), sendo 122 (40%) precoces e 183 (60%) tardias.
A sepse clínica (n=197) correspondeu a 37,7% do total de infecções notificadas e a sepse com confirmação laboratorial (n=108) a 20,6% do total de IRAS, independentemente do critério utilizado. Após a sepse, as infecções mais frequentes foram as de pele (monilíase) (15,1%), seguidas de conjuntivite (6,5%) e pneumonia com diagnóstico clínico (6,1%).
Das 522 notificações de IRAS, 489 (93,7%) foram preenchidas utilizando‐se ambos os critérios, oito infecções foram notificadas apenas pelo critério nacional e 25 exclusivamente pelo NHSN. Os 25 casos de infecção em que foi possível empregar apenas o critério do NHSN para notificação de IRAS correspondiam a episódios de sepse clínica precoce ou tardia, enquanto aqueles que atenderam apenas ao critério nacional foram dois casos de conjuntivite e seis notificações de enterocolite necrosante (tabela 2).
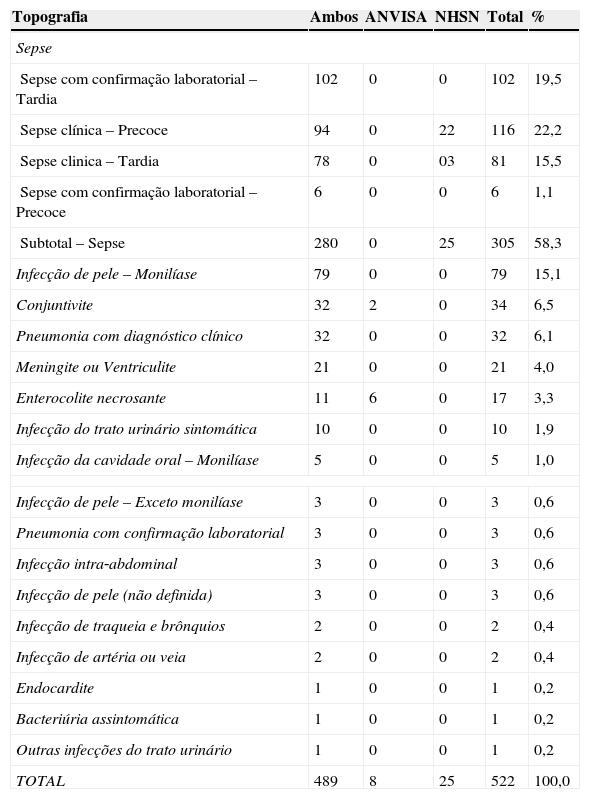
Distribuição de IRAS por critério de vigilância, UNCP, HC/UFMG, 2009 a 2011
| Topografia | Ambos | ANVISA | NHSN | Total | % |
|---|---|---|---|---|---|
| Sepse | |||||
| Sepse com confirmação laboratorial – Tardia | 102 | 0 | 0 | 102 | 19,5 |
| Sepse clínica – Precoce | 94 | 0 | 22 | 116 | 22,2 |
| Sepse clinica – Tardia | 78 | 0 | 03 | 81 | 15,5 |
| Sepse com confirmação laboratorial – Precoce | 6 | 0 | 0 | 6 | 1,1 |
| Subtotal – Sepse | 280 | 0 | 25 | 305 | 58,3 |
| Infecção de pele – Monilíase | 79 | 0 | 0 | 79 | 15,1 |
| Conjuntivite | 32 | 2 | 0 | 34 | 6,5 |
| Pneumonia com diagnóstico clínico | 32 | 0 | 0 | 32 | 6,1 |
| Meningite ou Ventriculite | 21 | 0 | 0 | 21 | 4,0 |
| Enterocolite necrosante | 11 | 6 | 0 | 17 | 3,3 |
| Infecção do trato urinário sintomática | 10 | 0 | 0 | 10 | 1,9 |
| Infecção da cavidade oral – Monilíase | 5 | 0 | 0 | 5 | 1,0 |
| Infecção de pele – Exceto monilíase | 3 | 0 | 0 | 3 | 0,6 |
| Pneumonia com confirmação laboratorial | 3 | 0 | 0 | 3 | 0,6 |
| Infecção intra‐abdominal | 3 | 0 | 0 | 3 | 0,6 |
| Infecção de pele (não definida) | 3 | 0 | 0 | 3 | 0,6 |
| Infecção de traqueia e brônquios | 2 | 0 | 0 | 2 | 0,4 |
| Infecção de artéria ou veia | 2 | 0 | 0 | 2 | 0,4 |
| Endocardite | 1 | 0 | 0 | 1 | 0,2 |
| Bacteriúria assintomática | 1 | 0 | 0 | 1 | 0,2 |
| Outras infecções do trato urinário | 1 | 0 | 0 | 1 | 0,2 |
| TOTAL | 489 | 8 | 25 | 522 | 100,0 |
IRAS, infecções relacionadas à assistência à saúde; UNCP, Unidade Neonatal de Cuidados Progressivos.
Os resultados da análise dos critérios nacionais de notificação de IRAS em todas as topografias e que apresentam alta sensibilidade, especificidade, VPP e VPN, além da concordância excelente, foram apresentados na tabela 3.
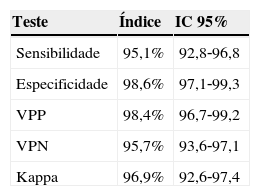
Comparação entre o critério nacional e o critério NHSN para notificação de IRAS em todas as topografias, UNCP, HC/UFMG, 2009 a 2011
| Teste | Índice | IC 95% |
|---|---|---|
| Sensibilidade | 95,1% | 92,8‐96,8 |
| Especificidade | 98,6% | 97,1‐99,3 |
| VPP | 98,4% | 96,7‐99,2 |
| VPN | 95,7% | 93,6‐97,1 |
| Kappa | 96,9% | 92,6‐97,4 |
IRAS, infecções relacionadas à assistência à saúde; VPP, valor preditivo positivo; VPN, valor preditivo; UNCP, Unidade Neonatal de Cuidados Progressivos; IC, intervalo de confiança.
Verificou‐se que a sensibilidade do critério nacional para notificação de sepse apresentou proporção relativamente menor de notificações, mas apresentou maior especificidade quando comparado à notificação pelos critérios do NHSN, quando se empregou os critérios para todas as topografias. Os resultados de sensibilidade, especificidade, VPP, VPN e Kappa para as notificações de sepse pelo critério nacional foram apresentados na tabela 4.
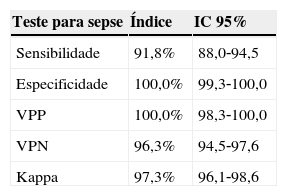
Comparação entre o critério nacional e o critério NHSN para notificação de sepse, UNCP, HC/UFMG, 2009 a 2011
| Teste para sepse | Índice | IC 95% |
|---|---|---|
| Sensibilidade | 91,8% | 88,0‐94,5 |
| Especificidade | 100,0% | 99,3‐100,0 |
| VPP | 100,0% | 98,3‐100,0 |
| VPN | 96,3% | 94,5‐97,6 |
| Kappa | 97,3% | 96,1‐98,6 |
VPP, valor preditivo positivo; VPN, valor preditivo negativo; UNCP, Unidade Neonatal de Cuidados Progressivos; IC, intervalo de confiança.
A densidade de incidência de IRAS neste estudo, considerando‐se os dois critérios de vigilância, foi de 27,28 infecções por 1.000 pacientes‐dia, e apresentou‐se mais elevada na faixa de peso abaixo de 750 gramas, em comparação com as demais. Os resultados reforçam os dados da literatura que indicam o baixo peso ao nascimento como risco para infecções, considerando a maior necessidade de procedimentos invasivos e o tempo prolongado de hospitalização dos neonatos com peso abaixo de 750g.10,11
As topografias com maior incidência de IRAS notificadas foram a sepse (58,3%), infecção de pele (15,1%) e conjuntivite (6,5%). Estes resultados foram semelhantes a um estudo conduzido em uma Unidade de Tratamento Intensivo Neonatal (UTIN) de Belo Horizonte, que apontou a sepse como principal complicação infecciosa no neonato (46%), seguida de conjuntivite (12,1%) e infecção de pele (9,5%).12 Outro estudo, conduzido durante cinco anos na Alemanha, identificou como principais sítios de IRAS, em recém‐nascidos com peso abaixo de 1.500g, sepse (78%), pneumonia associada à ventilação mecânica (11%) e enterocolite necrosante (10%).13
Dentre todas as topografias de IRAS, a sepse clínica foi a complicação infecciosa neonatal com maior número de notificações, respondendo por 37,7% do total, independentemente do critério de notificação. A maior incidência de sepse clínica em neonatos pode ser explicada pela dificuldade de comprovação laboratorial nesta população. A confirmação da sepse se dá pelo crescimento de patógenos em hemocultura ou em caso de microrganismo comensal e crescimento em duas hemoculturas, que é considerado padrão ouro para o diagnóstico da infecção da corrente sanguínea. Entretanto, isso nem sempre ocorre no neonato, devido a inúmeros fatores, como amostra de sangue insuficiente e administração de antimicrobianos à mãe antes do parto.14–17
Alguns autores consideram que determinados fatores dificultam o diagnóstico da sepse no período neonatal, em função dos sinais clínicos inespecíficos, que se confundem com as condições próprias do período, como taquipneia transitória e apneia da prematuridade. As alterações clínicas em neonatos são consideradas de baixo valor preditivo para sepse, sendo necessários outros parâmetros para a confirmação do quadro infeccioso. Por isso o diagnóstico da sepse neonatal é considerado difícil, tanto do ponto de vista clínico quanto laboratorial. Além disso, o resultado negativo da hemocultura não implica em inexistência da sepse no neonato, já que este exame possui baixa sensibilidade.16,17
Alguns trabalhos evidenciam a variabilidade e baixo valor preditivo de sinais clínicos de infecção em neonatos. Um estudo brasileiro conduzido em UTIN, com acompanhamento de 55 neonatos com suspeita de infecção, identificou que os sinais clínicos da sepse neonatal podem variar, com manifestações como hipotermia e hipertermia (33%), taquicardia (11%) e hipoatividade (94%).18
Outro estudo, com análise de 220 episódios de sepse clínica em UTIN na Índia, identificou como sinais clínicos sugestivos mais frequentes a hipoatividade, (46,4%), apneia (33,6%) e estase gástrica (33,6%). Com a análise do escore clínico para sepse proposto neste estudo, evidenciou‐se que os sinais clínicos são reduzidos do momento da suspeita de infecção para as 24 horas seguintes, com sensibilidade de 90% (0 hora) e 75% (24 horas), com baixo VPP de 30,3% (0 hora) e 41,7% (24 horas).19 Este resultado é semelhante a outro estudo conduzido em Bangladesh20 com análise dos preditores clínicos de sepse em neonatos prematuros com cultura positiva (n=105), em que a aplicação de escore clínico apresentou baixa sensibilidade de 56,6%, especificidade de 52,1% e VPP de 78,1%. Outra investigação realizada por Singh et al.21 analisou 16 sinais clínicos de sepse e identificou valores de sensibilidade de 47%, 40% e 30%, respectivamente, para apneia, letargia e taquicardia, como os melhores resultados.
Como os sinais e sintomas de sepse em recém‐nascido são inespecíficos, considera‐se que a associação dos sinais clínicos a alterações laboratoriais pode contribuir para diagnóstico e notificação da sepse neonatal. Em 1988, Rodwell et al.22 propuseram o uso de escore hematológico para predição de sepse em neonatos com quadro compatível, com padronização de parâmetros de referência para global de leucócitos, total de neutrófilos, neutrófilos imaturos, relação de neutrófilos imaturos por maduros, contagem de plaquetas e alterações degenerativas. Ao aplicar o escore, verificou‐se que 96% dos neonatos com sepse comprovada e 100% daqueles com sepse provável apresentavam valor igual maior que três escores alterados. Em estudo conduzido em UTIN, na Bélgica, um escore contendo variáveis clínicas e laboratoriais (PCR, fração de neutrófilos, trombocitopenia, febre e exposição prolongada a nutrição parenteral) foi considerado útil na identificação de neonatos com quadro de sepse, com sensibilidade de 95%, especificidade de 43%, VPP de 54% e VPN de 93%.23
Outra investigação realizada por Sankar et al.24, em que se analisou escore hematológico, incluindo total de leucócitos, total de neutrófilos, fração de neutrófilos imaturos e PCR, obteve sensibilidade de 93% a 100% e especificidade de 83%, na presença de dois parâmetros alterados, para neonatos com suspeita de sepse. A PCR também tem sido considerada marcador útil para acompanhamento dos neonatos com quadro de sepse, devido ao alto VPN. A queda do nível deste marcador, aliada à melhora clínica do paciente, tem sido usada como parâmetro para a interrupção da antibioticoterapia.18 Um estudo prospectivo, realizado durante três anos em UTIN do Rio de Janeiro, obteve resultados de leucograma alterado em 64,3% dos casos de sepse provável com quadro clínico compatível, e a medida da Proteína C Reativa (PCR) mostrou‐se elevada no grupo de pacientes com sepse comprovada.17
Neste estudo, a concordância entre os critérios nacionais em relação ao NHSN para notificação de IRAS e sepse em neonatologia foi considerada elevada (Kappa=96,9% e 97,3%, respectivamente). No entanto, as notificações de IRAS em que se observou maior diferença entre os métodos foram as de sepse clínica. Ressalta‐se que a notificação de sepse clínica ainda é recomendada pela ANVISA,8 embora tenha sido excluído do NHSN7 na versão do protocolo de julho de 2011, quando já estava finalizada a coleta de dados deste estudo.
Todas as 25 notificações de sepse clínica que não foram preenchidas pelo critério ANVISA, notificadas apenas com base no NHSN, ocorreram em função da exigência de maior número de itens, incluindo a necessidade de alterações laboratoriais (hemograma com três ou mais parâmetros alterados e/ou Proteína C Reativa quantitativa alterada), o que pode contribuir para tornar mais fidedigna a notificação. A ANVISA também acrescenta um número maior de sinais clínicos para a notificação de sepse clínica, como intolerância alimentar, instabilidade hemodinâmica, piora do esforço respiratório, intolerância à glicose e letargia.8
A proposta da ANVISA8 se aproxima da conduta clínica e da literatura,18,23,24 que tendem a valorizar alterações laboratoriais para o diagnóstico da sepse e início ou manutenção da antibioticoterapia.
Em estudo conduzido previamente no mesmo serviço, com utilização exclusiva dos critérios nacionais para a notificação de infecções em neonatologia, verificou‐se que os principais indicadores de IRAS e topografias foram semelhantes a outros estudos realizados previamente com base em critérios internacionais do NHSN.25
Em trabalho um realizado durante dois anos em UTIN de Hospital Universitário do Rio de Janeiro, foram empregados os critérios nacionais de IRAS8 visando aprimorar o diagnóstico e a notificação da sepse em neonatos de baixo peso. Neste estudo observou‐se que, com a aplicação dos critérios clínicos, hematológicos e dosagens de PCR propostos pela ANVISA, houve uma redução do diagnóstico e notificação de sepse precoce, com consequente diminuição da utilização de antimicrobianos.26 Kaufman comenta e descreve a importância da implementação de protocolos contendo critérios para diagnóstico da sepse neonatal precoce e tardia, visando a interrupção da terapia antimicrobiana, baseada em dados hematológicos e dosagem de PCR.27
Considera‐se, portanto, que o menor número de notificações pelos critérios nacionais em relação ao NHSN observada, com sensibilidade de 95,1%, pode ocorrer devido ao acréscimo dos parâmetros laboratoriais necessários para as notificações de sepse pelo critério da ANVISA, com sensibilidade de 91,8% quando consideradas apenas as notificações de infecção da corrente sanguínea.
O maior número de parâmetros laboratoriais para notificação de sepse clínica auxilia na exclusão de possíveis quadros não infecciosos, aumentando a especificidade e VPP, como observado no presente estudo, com uma especificidade de 98,6% para notificação de IRAS em todas as topografias e 100% quando analisada exclusivamente a sepse, além do alto valor preditivo negativo de 98,4% e 96,3%, respectivamente.
A enterocolite necrosante foi a segunda topografia em que houve maior diferença entre os critérios para vigilância e notificação de IRAS. Das 17 notificações de enterocolite, seis foram preenchidas apenas pelo critério ANVISA e 11 por ambos os critérios. Observa‐se que para as notificações de enterocolite necrosante, diferentemente do critério NHSN, a ANVISA não impõe a necessidade da presença de sangue nas fezes como condição para a notificação da infecção. Nesse caso, há um aumento do número de notificações de enterocolite, que aumenta a sensibilidade do critério nacional.
Os sinais de enterocolite no neonato mostram uma ampla variação quanto à forma de apresentação, desde quadros inespecíficos, com distensão abdominal leve, aumento do resíduo gástrico, letargia e instabilidade térmica, até os mais evidentes, com distensão abdominal, enterorragia e presença de sangue nas fezes, o que nem sempre ocorre.28,29
Alguns autores consideram que a ausência de critérios predeterminados pelo CDC para a caracterização de infecções exclusivamente do período neonatal e a rápida evolução destes processos entre os recém‐nascidos dificultam a classificação de algumas infecções. Isto é evidente na classificação de sepse, que apresenta ampla variação entre estudos na área.2,17,18,30
Além de todas as dificuldades para o diagnóstico da sepse nesta faixa etária, a Unidade Neonatal é considerada unidade crítica e de vigilância prioritária e obrigatória, que demanda cuidados especializados para pacientes criticamente doentes e de maior exposição aos riscos. A prevenção e o controle das IRAS nessa população representam um desafio para os hospitais, e para definir intervenções é necessário manter um sistema de vigilância ativa das infecções.9,10,12
ConclusãoVerificou‐se uma elevada concordância entre a utilização dos critérios nacionais propostos pela ANVISA em relação ao método do NHSN para a notificação das IRAS em unidades neonatais. A utilização dos critérios nacionais para a vigilância epidemiológica das IRAS nestas unidades fornece ferramentas que auxiliam na notificação das infecções, pois a associação de dados laboratoriais aos dados clínicos proposta pela ANVISA podem contribuir para melhorar a especificidade e VPP do diagnóstico e da notificação das infecções neonatais, considerando‐se a baixa sensibilidade e o baixo valor preditivo dos sinais clínicos na vigência de suspeita de infecção.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Como citar este artigo: Ferreira J, Bouzada MC, de Jesus LA, Cortes MdC, Armond GA, Clemente WT, et al. Evaluation of national health‐care related infection criteria for epidemiological surveillance in neonatology. J Pediatr (Rio J). 2014;90:389–95.