To develop Brazilian growth charts for body mass index (BMI‐for‐age) for individuals with Down syndrome (DS). The secondary objective was to compare the BMI‐for‐age with the Centers for Disease Control and Prevention standards (CDC).
MethodsA retrospective and cross‐sectional growth study of 706 youth with DS (56.7% males) was performed in 51 centers in São Paulo state, Brazil. Weight and height were used to calculate the BMI (kg/m2). The LMS method was applied to construct the growth charts. Z‐scores were based on the CDC 2000 growth standards.
ResultsThe BMI‐for‐age reference charts showed excellent goodness of fit statistics for boys and girls with DS aged 2–18 years. At 2 years of age, the mean BMI Z‐scores of boys and girls with DS were lower compared to those of the CDC (Z‐score=−0.2). In contrast, children with DS aged 3‐18 years had higher mean Z‐scores for BMI‐for‐age when compared to those of the CDC (Z‐scores=+0.2 to +1.3).
ConclusionsThe BMI of Brazilian youth with DS differs from those references established by CDC. These are the first Brazilian BMI‐for‐age charts for individuals with DS and will hopefully guide clinicians and parents in the evaluation and management of the nutritional status in children and adolescents with DS in Brazil.
Desenvolver curvas específicas de índice de massa corporal (IMC‐para‐idade) para população brasileira com síndrome de Down (SD). O objetivo secundário foi comparar os valores de IMC‐para‐idade com os valores normativos dos Centros de Controle e Prevenção de Doenças dos Estados Unidos (CDC).
MétodosEstudo do tipo retrospectivo e transversal. A amostra foi constituída de 706 jovens com SD (56,7%, meninos) recrutados em 51 instituições no Estado de São Paulo, Brasil. Peso e estatura foram obtidos e empregados para o cálculo de IMC (Kg/m2). O método LMS foi usado para a construção das curvas. Escores Z foram calculados com base na referência do CDC 2000.
ResultadosAs curvas de referência de IMC‐para‐idade para meninos e meninas com SD na faixa entre 2‐18 anos apresentaram excelente ajuste estatístico. Aos 2 anos, o escore Z médio IMC de crianças com SD apresentou‐se menor quando comparado com o CDC (escore Z=‐0,2). Em contraste, os escores Z médios de IMC de jovens com SD foram superiores entre 3‐18 anos (escores Z=+0,2 a +1,3).
ConclusõesA população brasileira com SD apresentou diferentes padrões de IMC quando comparada com as referências do CDC. As curvas desenvolvidas neste estudo representam a primeira referência nacional de IMC‐para‐idade para jovens com SD. Espera‐se, portanto, que essas curvas possam guiar pais e profissionais na avaliação do estado nutricional de crianças e adolescentes com SD no território brasileiro.
Síndrome de Down (SD) é uma desordem cromossômica com estimativa aproximada entre 3,05 e 14 em 10.000 nascidos vivos em países como Estados Unidos e China.1,2 Em relação à prevalência populacional mais recente, estudos mostram variação entre 6,1 e 13,1 por 10.000 pessoas.3,4 A expectativa de vida entre pessoas com SD tem aumentado consideravelmente nas últimas décadas. Estudo sugere que 94,4% das crianças com SD nascidas em 2000 devem sobreviver em 2020, 90,8% em 2030 e 76,3% em 2050.3 O aumento na expectativa de vida relaciona‐se ao desenvolvimento de pesquisas e ofertas de serviços.5 Apesar dos avanços, crianças com SD apresentam condições de saúde que afetam a qualidade de vida, incluindo cardiopatias congênitas, hipotireoidismo, distúrbios gastrointestinais e apneia obstrutiva do sono.6 Segundo as diretrizes da Academia Americana de Pediatria e do Ministério da Saúde, pessoas com SD também apresentam restrição no crescimento e sobrepeso.7,8
Acompanhar adequadamente o estado nutricional de jovens com SD permite prevenir e identificar problemas gerais de saúde. O índice de massa corporal (IMC) é um indicador de saúde comumente usado para classificar o estado nutricional de crianças, adultos e idosos. Os Centros de Controle e Prevenção de Doenças dos Estados Unidos (CDC) têm recomendado o uso do IMC para avaliar as condições de saúde de crianças acima de 2 anos. No entanto, jovens com SD apresentam diferentes padrões de peso, estatura e IMC quando comparados com as crianças da população geral.9 Quando comparados com o CDC, jovens com SD entre 2‐20 anos apresentaram baixa estatura, bem como valores superiores de IMC após os 2 anos, o que sugere a necessidade de curvas específicas de crescimento para a população jovem com SD.10 No Brasil, o Ministério da Saúde recomenda o uso das curvas de peso‐para‐idade de Cronk et al. (1988)11 para o acompanhamento do estado nutricional de jovens brasileiros com SD entre 2 e 18 anos.7 Essas curvas combinam dados transversais e longitudinais e incluem 730 jovens americanos com SD entre 1 mês e 18 anos.11 Essas curvas, no entanto, foram contestadas pela Academia Americana de Pediatria para aplicação clínica e prática.8
Devido às limitações das curvas existentes e à ausência de valores normativos de IMC‐para‐idade para jovens brasileiros com SD, o presente estudo teve como objetivo desenvolver curvas específicas de IMC‐para‐idade para a população brasileira com SD entre 2 e 18 anos. O objetivo secundário foi comparar os valores de IMC‐para‐idade dos participantes do presente estudo com os valores normativos estabelecidos pelo CDC 2000.
MétodosCrianças e adolescentes com SD entre 2 e 18 anos foram recrutados a partir de um estudo do tipo retrospectivo e transversal desenvolvido entre 2012 e 2015. O estudo foi feito na Universidade Estadual de Campinas (Unicamp), em 48 centros especializados para o atendimento de pessoas com deficiência intelectual e em dois centros especializados para pessoas com SD, todos no Estado de São Paulo. O estudo foi aprovado pelo Comitê de Ética da Faculdade de Ciências Médicas da Unicamp (140.186/2012). O termo de consentimento livre e esclarecido foi assinado pelos pais e responsáveis.
Dados de registros clínicos foram obtidos por meio de entrevistas com as famílias e de prontuários médicos. Um questionário foi aplicado aos pais e responsáveis, incluindo informações de idade, sexo, idade gestacional, comorbidades, medicamentos, peso, estatura e perímetro cefálico. Na entrevista, também foram obtidas informações do cartão da criança e de formulários fornecidos aos pais (por unidades de saúde, clínicas médicas e hospitais da região de Campinas). Peso e estatura foram coletados por uma equipe de avaliadores treinados em 2012, 2013 e 2014. Os participantes foram medidos descalços e vestiam roupas leves. Em Campinas, a estatura foi avaliada mediante estadiômetro portátil, modelo E210 (Wiso®, SC, Brasil) e o peso foi aferido em balança digital, modelo W801 (Wiso®, SC, Brasil).
O tratamento dos dados foi feito em diferentes etapas, com exclusão de dados nas seguintes situações: 1) dados duplicados observados mediante o código de identificação, data de nascimento e data da avaliação; 2) dados discrepantes (cinco desvios‐padrão acima ou abaixo da média); 3) identificação de perda de estatura em amostras longitudinais. No caso de inconsistência dos dados, os questionários e registros clínicos foram reexaminados. Dados de peso e estatura foram usados para o cálculo do IMC, com a seguinte fórmula: IMC = Peso dividido pela estatura ao quadrado (Kg/m2). Modelos aditivos generalizados para posição, escala e forma (GAMLSS)12 foram usados para a construção das curvas de IMC/idade, com o software R (R Foundation for Statistical Computing, versão 3.2.2, Viena, Áustria). O método LMS e gráficos worm plots foram usados para modelagem das curvas.13,14
Os percentis gerados para IMC/idade foram os seguintes: 5, 10, 25, 50, 75, 85, 90, e 95. Escores Z médios foram calculados para comparar o IMC/idade com as referências normativas estabelecidas pelo CDC,15 mediante a seguinte equação: Z = [(X / M)L‐1] / L * S, na qual X foi a medida observada (IMC) de cada participante, M a mediana, L o valor de assimetria, ‐1 a constante e S o valor do coeficiente de variação. Os valores de L, M e S foram obtidos das tabelas normativas do CDC 2000.
ResultadosParticipantesA amostra foi constituída de 706 participantes com SD entre 2 e 18 anos nascidos entre 1978 e 2012 (56,7%, meninos). No estudo, foram coletadas 1.986 observações de IMC. No que se refere à idade gestacional, 10,1% foram prematuros (< 37 semanas de gestação). Observando‐se a frequência de comorbidades, 17,9% apresentaram cardiopatias congênitas, 13,1% foram submetidos à cirurgia cardíaca e 22% apresentaram hipotireoidismo (todos controlados laboratorialmente). Informações faltantes relacionadas à idade gestacional, cardiopatias e hipotireoidismo foram de 57,9%, 31,3%, e 27,2%, respectivamente.
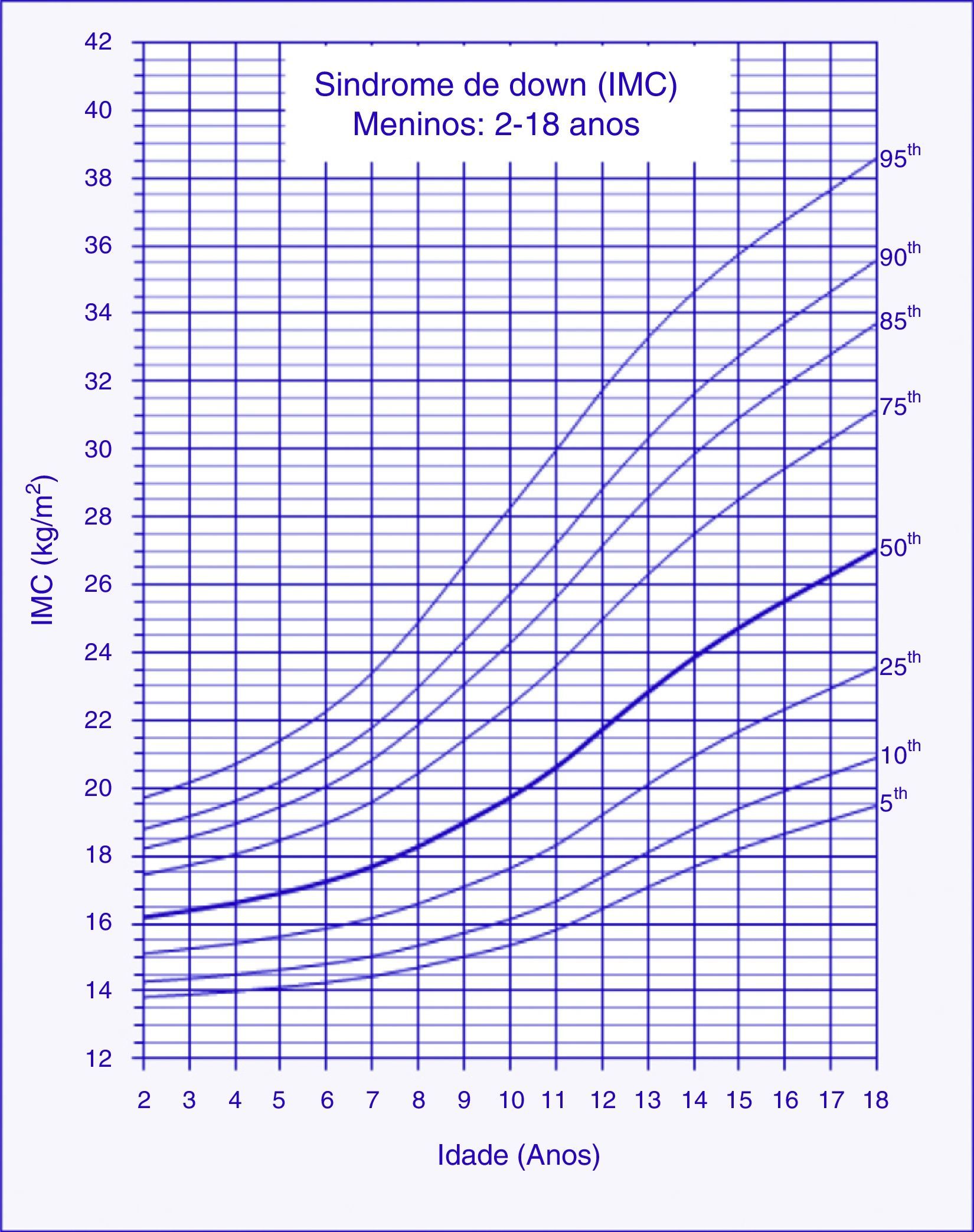
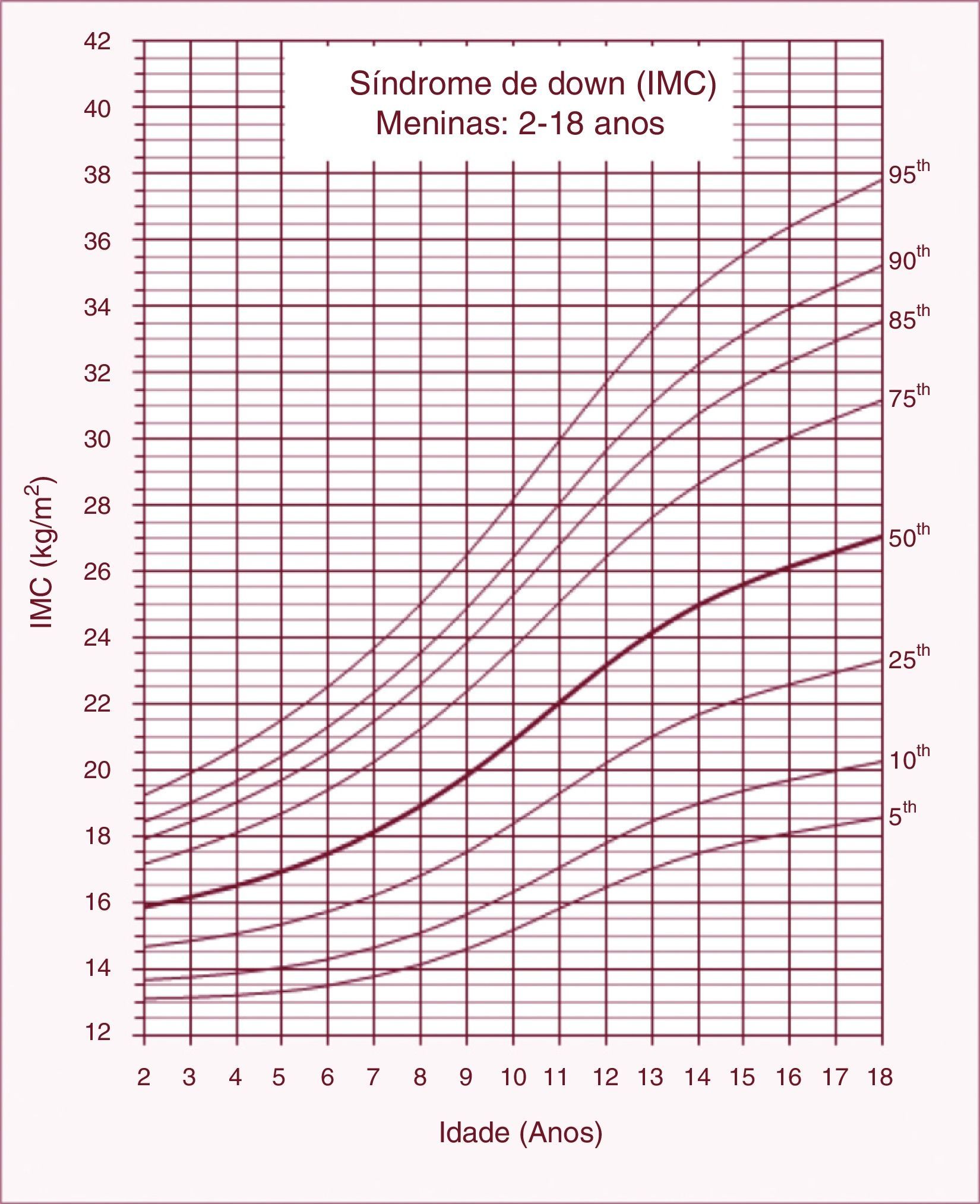
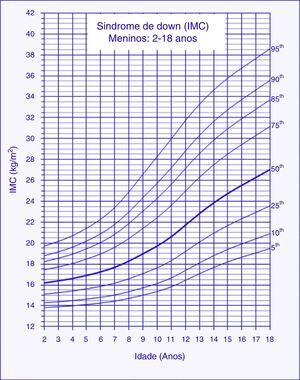
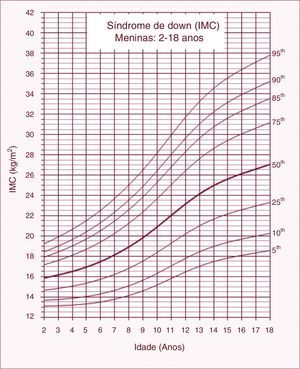
Gráfico de IMCAs curvas de referência de IMC‐para‐idade para meninos e meninas com SD entre 2‐18 anos apresentaram excelente ajuste estatístico. A maioria dos indivíduos apresentou mais do que uma única observação (82%). Número de observações, médias, desvios‐padrão, LMS e percentis por idade e sexo estão apresentados nas tabelas 1 e 2. Gráficos com os percentis de IMC/idade de meninos e meninas com SD podem ser observados nas figuras 1 e 2. Aos 2 anos, o escore Z médio de IMC de crianças com SD foi menor comparado com os valores normativos do CDC (escore Z = ‐0,2). Em contraste, os escores Z médios de IMC de crianças e adolescentes com SD de ambos os sexos foram superiores entre 3 e 18 anos (escores Z = +0,2 a +1,3).
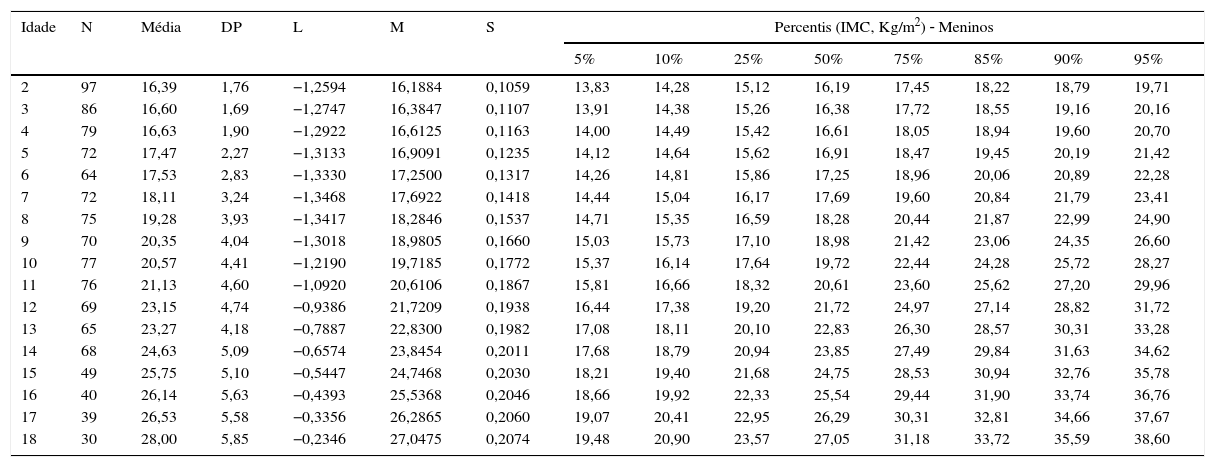
Valores de índice de massa corporal (IMC) de crianças e adolescentes com síndrome de Down do sexo masculino entre 2 e 18 anos
| Idade | N | Média | DP | L | M | S | Percentis (IMC, Kg/m2) ‐ Meninos | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 5% | 10% | 25% | 50% | 75% | 85% | 90% | 95% | |||||||
| 2 | 97 | 16,39 | 1,76 | −1,2594 | 16,1884 | 0,1059 | 13,83 | 14,28 | 15,12 | 16,19 | 17,45 | 18,22 | 18,79 | 19,71 |
| 3 | 86 | 16,60 | 1,69 | −1,2747 | 16,3847 | 0,1107 | 13,91 | 14,38 | 15,26 | 16,38 | 17,72 | 18,55 | 19,16 | 20,16 |
| 4 | 79 | 16,63 | 1,90 | −1,2922 | 16,6125 | 0,1163 | 14,00 | 14,49 | 15,42 | 16,61 | 18,05 | 18,94 | 19,60 | 20,70 |
| 5 | 72 | 17,47 | 2,27 | −1,3133 | 16,9091 | 0,1235 | 14,12 | 14,64 | 15,62 | 16,91 | 18,47 | 19,45 | 20,19 | 21,42 |
| 6 | 64 | 17,53 | 2,83 | −1,3330 | 17,2500 | 0,1317 | 14,26 | 14,81 | 15,86 | 17,25 | 18,96 | 20,06 | 20,89 | 22,28 |
| 7 | 72 | 18,11 | 3,24 | −1,3468 | 17,6922 | 0,1418 | 14,44 | 15,04 | 16,17 | 17,69 | 19,60 | 20,84 | 21,79 | 23,41 |
| 8 | 75 | 19,28 | 3,93 | −1,3417 | 18,2846 | 0,1537 | 14,71 | 15,35 | 16,59 | 18,28 | 20,44 | 21,87 | 22,99 | 24,90 |
| 9 | 70 | 20,35 | 4,04 | −1,3018 | 18,9805 | 0,1660 | 15,03 | 15,73 | 17,10 | 18,98 | 21,42 | 23,06 | 24,35 | 26,60 |
| 10 | 77 | 20,57 | 4,41 | −1,2190 | 19,7185 | 0,1772 | 15,37 | 16,14 | 17,64 | 19,72 | 22,44 | 24,28 | 25,72 | 28,27 |
| 11 | 76 | 21,13 | 4,60 | −1,0920 | 20,6106 | 0,1867 | 15,81 | 16,66 | 18,32 | 20,61 | 23,60 | 25,62 | 27,20 | 29,96 |
| 12 | 69 | 23,15 | 4,74 | −0,9386 | 21,7209 | 0,1938 | 16,44 | 17,38 | 19,20 | 21,72 | 24,97 | 27,14 | 28,82 | 31,72 |
| 13 | 65 | 23,27 | 4,18 | −0,7887 | 22,8300 | 0,1982 | 17,08 | 18,11 | 20,10 | 22,83 | 26,30 | 28,57 | 30,31 | 33,28 |
| 14 | 68 | 24,63 | 5,09 | −0,6574 | 23,8454 | 0,2011 | 17,68 | 18,79 | 20,94 | 23,85 | 27,49 | 29,84 | 31,63 | 34,62 |
| 15 | 49 | 25,75 | 5,10 | −0,5447 | 24,7468 | 0,2030 | 18,21 | 19,40 | 21,68 | 24,75 | 28,53 | 30,94 | 32,76 | 35,78 |
| 16 | 40 | 26,14 | 5,63 | −0,4393 | 25,5368 | 0,2046 | 18,66 | 19,92 | 22,33 | 25,54 | 29,44 | 31,90 | 33,74 | 36,76 |
| 17 | 39 | 26,53 | 5,58 | −0,3356 | 26,2865 | 0,2060 | 19,07 | 20,41 | 22,95 | 26,29 | 30,31 | 32,81 | 34,66 | 37,67 |
| 18 | 30 | 28,00 | 5,85 | −0,2346 | 27,0475 | 0,2074 | 19,48 | 20,90 | 23,57 | 27,05 | 31,18 | 33,72 | 35,59 | 38,60 |
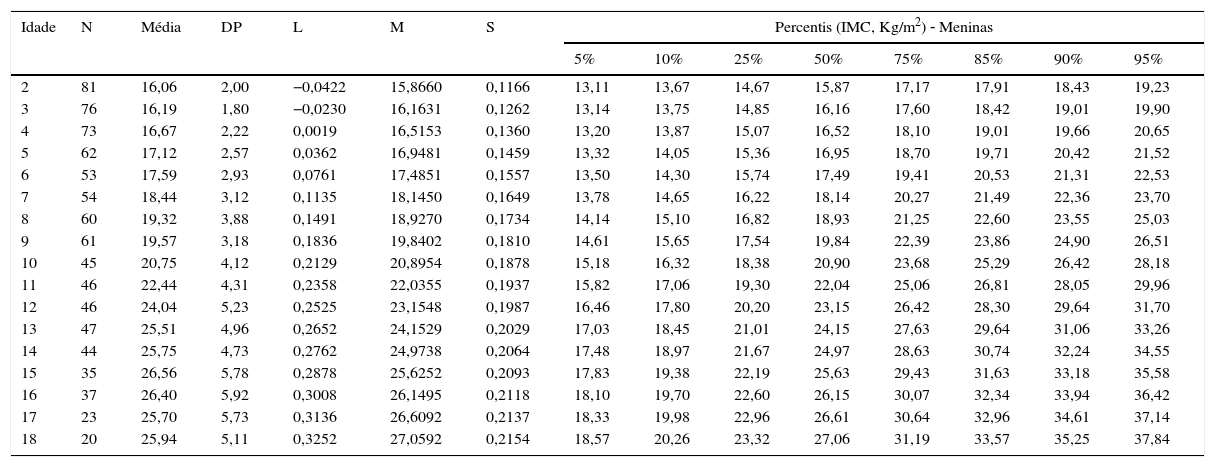
Valores de índice de massa corporal (IMC) de crianças e adolescentes com síndrome de Down do sexo feminino entre 2 e 18 anos
| Idade | N | Média | DP | L | M | S | Percentis (IMC, Kg/m2) ‐ Meninas | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 5% | 10% | 25% | 50% | 75% | 85% | 90% | 95% | |||||||
| 2 | 81 | 16,06 | 2,00 | −0,0422 | 15,8660 | 0,1166 | 13,11 | 13,67 | 14,67 | 15,87 | 17,17 | 17,91 | 18,43 | 19,23 |
| 3 | 76 | 16,19 | 1,80 | −0,0230 | 16,1631 | 0,1262 | 13,14 | 13,75 | 14,85 | 16,16 | 17,60 | 18,42 | 19,01 | 19,90 |
| 4 | 73 | 16,67 | 2,22 | 0,0019 | 16,5153 | 0,1360 | 13,20 | 13,87 | 15,07 | 16,52 | 18,10 | 19,01 | 19,66 | 20,65 |
| 5 | 62 | 17,12 | 2,57 | 0,0362 | 16,9481 | 0,1459 | 13,32 | 14,05 | 15,36 | 16,95 | 18,70 | 19,71 | 20,42 | 21,52 |
| 6 | 53 | 17,59 | 2,93 | 0,0761 | 17,4851 | 0,1557 | 13,50 | 14,30 | 15,74 | 17,49 | 19,41 | 20,53 | 21,31 | 22,53 |
| 7 | 54 | 18,44 | 3,12 | 0,1135 | 18,1450 | 0,1649 | 13,78 | 14,65 | 16,22 | 18,14 | 20,27 | 21,49 | 22,36 | 23,70 |
| 8 | 60 | 19,32 | 3,88 | 0,1491 | 18,9270 | 0,1734 | 14,14 | 15,10 | 16,82 | 18,93 | 21,25 | 22,60 | 23,55 | 25,03 |
| 9 | 61 | 19,57 | 3,18 | 0,1836 | 19,8402 | 0,1810 | 14,61 | 15,65 | 17,54 | 19,84 | 22,39 | 23,86 | 24,90 | 26,51 |
| 10 | 45 | 20,75 | 4,12 | 0,2129 | 20,8954 | 0,1878 | 15,18 | 16,32 | 18,38 | 20,90 | 23,68 | 25,29 | 26,42 | 28,18 |
| 11 | 46 | 22,44 | 4,31 | 0,2358 | 22,0355 | 0,1937 | 15,82 | 17,06 | 19,30 | 22,04 | 25,06 | 26,81 | 28,05 | 29,96 |
| 12 | 46 | 24,04 | 5,23 | 0,2525 | 23,1548 | 0,1987 | 16,46 | 17,80 | 20,20 | 23,15 | 26,42 | 28,30 | 29,64 | 31,70 |
| 13 | 47 | 25,51 | 4,96 | 0,2652 | 24,1529 | 0,2029 | 17,03 | 18,45 | 21,01 | 24,15 | 27,63 | 29,64 | 31,06 | 33,26 |
| 14 | 44 | 25,75 | 4,73 | 0,2762 | 24,9738 | 0,2064 | 17,48 | 18,97 | 21,67 | 24,97 | 28,63 | 30,74 | 32,24 | 34,55 |
| 15 | 35 | 26,56 | 5,78 | 0,2878 | 25,6252 | 0,2093 | 17,83 | 19,38 | 22,19 | 25,63 | 29,43 | 31,63 | 33,18 | 35,58 |
| 16 | 37 | 26,40 | 5,92 | 0,3008 | 26,1495 | 0,2118 | 18,10 | 19,70 | 22,60 | 26,15 | 30,07 | 32,34 | 33,94 | 36,42 |
| 17 | 23 | 25,70 | 5,73 | 0,3136 | 26,6092 | 0,2137 | 18,33 | 19,98 | 22,96 | 26,61 | 30,64 | 32,96 | 34,61 | 37,14 |
| 18 | 20 | 25,94 | 5,11 | 0,3252 | 27,0592 | 0,2154 | 18,57 | 20,26 | 23,32 | 27,06 | 31,19 | 33,57 | 35,25 | 37,84 |
Este estudo apresenta a primeira referência brasileira de IMC‐para‐idade desenvolvida para crianças e adolescentes com SD de ambos os sexos entre 2 e 18 anos. O estudo também encontrou diferenças nos valores de IMC entre as crianças e adolescentes com SD e os valores normativos estabelecidos pelo CDC. Os resultados têm implicações clínicas e práticas em relação ao monitoramento do estado nutricional de crianças e adolescentes com SD no Brasil.
Aos 2 anos, os valores médios de IMC de meninos e meninas com SD apresentaram‐se abaixo dos padrões estabelecidos pelo CDC. Estudos mostram que crianças com SD nos primeiros dois anos de vida são caracterizadas por valores reduzidos de peso corporal.10,16 O baixo peso pode estar relacionado às taxas decrescentes de crescimento e a desordens que envolvem a ingestão de alimentos.17,18 A restrição do crescimento relaciona‐se à fatores genéticos.19 Desordens na sucção/deglutição relacionam‐se à hipotonia e a disfunções no sistema oromotor.18 Após os 2 anos, os escores Z médios de IMC/idade de crianças e adolescentes com SD resultaram em aproximadamente um desvio‐padrão acima dos valores normativos do CDC. Zemel et al. (2015)10 também reportaram valores superiores de IMC/idade em crianças americanas com SD, após os 2 anos, em relação às normas do CDC. Após os 2 anos, crianças com SD tendem a apresentar elevada prevalência de sobrepeso e obesidade quando comparadas com as crianças da população em geral.20,21 Fatores de risco para obesidade na SD incluem alterações do hormônio leptina, taxa metabólica basal reduzida, dieta desequilibrada e baixos níveis de atividade física.22–25
Os percentis de IMC/idade das crianças com SD aumentaram gradativamente entre 2 e 18 anos. Percentis de IMC/idade de crianças americanas com SD entre 2 e 20 anos apresentaram padrões similares.10 Esses aumentos ininterruptos de IMC observados em jovens com SD não condizem com os padrões de IMC da população infantil em geral. Referências internacionais mostram uma rápida aceleração nos percentis medianos de IMC/idade no primeiro ano de vida, seguido de declínio até os 5 anos e reaceleração em idades posteriores.15,26,27
No que se refere à aplicação clínica e prática, as curvas de IMC/idade representam padrões descritivos de crescimento de crianças e adolescentes com SD. Enfatiza‐se que as curvas não indicam um padrão ideal de peso, no qual todas as crianças com SD devem crescer ou o qual devem almejar. O uso dessas curvas, no entanto, permite comparar e monitorar as condições de peso corporal de populações com SD em território brasileiro. Para monitorar o estado nutricional da população jovem brasileira com SD, o Ministério da Saúde recomenda o uso das curvas de peso‐para‐idade de Cronk et al. (1988).11 Essas curvas, no entanto, foram contestadas pela Academia Americana de Pediatria para aplicação clínica e prática.8 A distribuição dos percentis de IMC/idade entre a população do presente estudo e CDC tem se mostrado diferente do ponto de vista prático. Por exemplo, uma criança com SD do sexo masculino com 14 anos (IMC: 23,85kg/m2, percentil 50, ver tabela 1) seria classificada na categoria de sobrepeso quando avaliada pelo CDC (IMC: 22,66kg/m2, percentil 85). Os resultados sugerem que novos estudos devem examinar a associação entre os pontos de cortes de IMC e o estado geral de saúde de crianças e adolescentes com SD.
Esse estudo apresenta algumas limitações. Primeiro, os dados foram obtidos de registros clínicos e podem apresentar erros de medidas. No entanto, na tentativa de minimizar tal viés, foi feito um rigoroso tratamento dos dados. Segundo, a mostra foi restrita ao Estado de São Paulo e não representa a população total de crianças com SD do Brasil. Por outro lado, o Estado de São Paulo, cuja população estimada é de 44.035.304 pessoas (27% do Brasil), pode representar a diversidade econômica e étnica do país. Finalmente, as curvas não representam o estado ótimo de crescimento de crianças com SD, tendo em vista que alguns fatores de influência do crescimento não foram controlados, tais como amamentação, apoio à lactação, comorbidades, saúde materna e situação socioeconômica. Novos estudos devem investigar a relação entre esses fatores e o crescimento de crianças e adolescentes com SD.
Em conclusão, a população brasileira com SD apresentou diferentes padrões de IMC quando comparada com as referências do CDC. As curvas desenvolvidas neste estudo representam a primeira referência nacional de IMC‐para‐idade para jovens com SD. Espera‐se, portanto, que essas curvas possam guiar pais e profissionais na avaliação do estado nutricional de crianças e adolescentes com SD no território brasileiro.
FinanciamentoCoordenação de Aperfeiçoamento de Pessoal de Nível Superior (Capes, BEX 3546/15‐2), Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq, Programa Institucional de Bolsas de Iniciação Científica [PIBIC]).
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
A Roberto A. Soares, João F. Cosmo, Alessandra C.P.D. Costa, Eliane T. Nogueira, Fabio Crozara, Célia de Oliveira e Maria A.C. Pacheco pela excelente assistência técnica. Às Associações de Pais e Amigos dos Excepcionais do Estado de São Paulo (Apaes/SP), ao Ambulatório de Integração das Especialidades Pediátricas da Faculdade de Ciências Médicas (AIEP/FCM/Unicamp), ao Departamento de Genética Médica (DGM/FCM/Unicamp) e ao Centro de Investigação em Pediatria (Ciped/FCM/Unicamp) da Universidade Estadual de Campinas, à Federação das Apaes do Estado de São Paulo (Feapaes/SP), ao Centro de Educação Especial Síndrome de Down (Ceesd) e à Fundação Síndrome de Down (FSD) pela fundamental colaboração no presente estudo.
Como citar este artigo: Bertapelli F, Machado MR, Roso RV, Guerra‐Júnior G. Body mass index reference charts for the individuals with Down syndrome aged 2‐18 years. J Pediatr (Rio J). 2017;93:94–9.
Estudo vinculado à Universidade Estadual de Campinas (Unicamp), Campinas, SP, Brasil.