Urinary tract infection (UTI) caused by resistant strains of bacteria is increasingly prevalent in children. The aim of this study was to investigate the clinical characteristics and risk factors for UTI caused by community‐acquired extended‐spectrum β‐lactamase (CA‐ESBL)‐producing bacteria in infants.
MethodsThis was a retrospective study performed over 5 years in a single Korean center. Hospitalized infants with febrile UTI were enrolled and divided into two groups (CA‐ESBL vs. CA non‐ESBL UTI). The yearly prevalence was calculated. Baseline characteristics and clinical course such as fever duration, laboratory and radiological findings were compared between the two groups. Risk factors associated with the CA‐ESBL UTI were investigated.
ResultsAmong the enrolled infants (n=185), 31 (17%) had CA‐ESBL UTI. The yearly prevalence of ESBL of CA‐ESBL UTI increased during the study (0% in 2010, 22.2% in 2015). Infants with CA‐ESBL UTI had a longer duration of fever after initiating antibiotics (2.0±1.1 vs. 1.5±0.6 days, p=0.020). Cortical defects on renal scan and early treatment failure were more frequent in CA‐ESBL (64.5 vs. 42.2%, p=0.023; 22.6 vs. 4.5%, p=0.001). A logistic regression analysis revealed that urinary tract abnormalities and previous UTI were independent risk factors for CA‐EBSL UTI (odds ratio, 2.7; p=0.025; 10.3; p=0.022).
ConclusionThe incidence of UTI caused by ESBL‐producing bacteria has increased in Korean infants. Recognition of the clinical course and risk factors for ESLB‐producing UTI may help to determine appropriate guidelines for its management.
A infecção do trato urinário (ITU) causada por cepas de bactérias resistentes está cada vez mais prevalente em crianças. O objetivo deste estudo foi investigar as características clínicas e os fatores de risco de ITU causada por bactérias produtoras de β‐lactamases de espectro ampliado adquiridas na comunidade (ESBL CA) em neonatos.
MétodosEstudo retrospectivo feito por mais de cinco anos em um único centro sul‐coreano. Neonatos internados com ITU febril foram inscritos e divididos em dois grupos (ITU por ESBL CA em comparação com não ESBL CA). A prevalência anual foi calculada. As características básicas e o curso clínico, como duração da febre e achados laboratoriais e radiológicos, foram comparados entre os dois grupos. Os fatores de risco associados à ITU por ESBL CA foram investigados.
ResultadosEntre os neonatos inscritos (n=185), 31 (17%) apresentaram ITU por ESBL CA. A prevalência anual de ESBL em ITU por ESBL CA aumentou durante o estudo (0% em 2010, 22,2% em 2015). Os neonatos com ITU por ESBL CA apresentaram maior duração de febre após o início dos antibióticos (2±1,1 em comparação com 1,5±0,6 dias, p=0,020). Os defeitos corticais no exame renal e a falha precoce no tratamento foram mais frequentes em ESBL CA (64,5 em comparação com 42,2%, p=0,023; 22,6 em comparação com 4,5%, p=0,001). Uma análise de regressão logística revelou que as anomalias do trato urinário e a ITU anterior eram fatores de risco independentes de ITU por ESBL CA (razão de chance: 2,7; p=0,025; 10,3; p=0,022).
ConclusãoA incidência de ITU causada por bactérias produtoras de ESBL aumentou em neonatos sul‐coreanos. O reconhecimento do curso clínico e dos fatores de risco de ITU por ESBL poderá ajudar a determinar as diretrizes adequadas de manejo.
A infecção do trato urinário (ITU) é uma causa comum de infecções bacterianas entre neonatos e crianças novas com febre sem uma origem. Em geral, a terapia antibiótica inicial da ITU é empiricamente apoiada até que os resultados de cultura e sensibilidade fiquem disponíveis. Contudo, devido ao uso frequente de antibióticos, têm surgido cepas resistentes. A resistência das bactérias gram‐negativas normalmente se deve a enzimas mediadas por plasmídeos chamadas β‐lactamases de espectro ampliado (ESBLs).1 Elas são frequentemente produzidas pelas espécies Escherichia coli e Klebsiella, patógenos causadores da ITU mais comuns.2 As bactérias produtoras de ESBL foram relatadas pela primeira vez em 19833 e, atualmente, estão espalhadas em todo o mundo.4 As ESBLs conferem não apenas resistência aos antibióticos β‐lactâmicos, como também, às vezes, resistência cruzada a outros antibióticos, como aminoglicosídeos, trimetoprima‐sulfametoxazol (TMP‐SMX) e quinolonas.5
Acredita‐se que as infecções causadas por essas bactérias ocorrem principalmente em hospitais e enfermarias.6 Mais recentemente, as bactérias produtoras de ESBL começaram a se disseminar pela comunidade em geral; de fato, em muitos países, a incidência de infecções adquiridas na comunidade aumentou.7–10. Embora diversos estudos tenham analisado os fatores de risco da ITU causada por bactérias produtoras de ESBL em adultos7,10 e crianças,8,9 estão disponíveis apenas dados limitados sobre ITUs adquiridas na comunidade (CA) causadas por bactérias produtoras de ESBL em neonatos. Portanto, o objetivo deste estudo foi investigar as características clínicas e os fatores de risco das ITUs CA causadas por bactérias produtoras de ESBL em neonatos.
MétodosModelo do estudo e seleção de pacientesEste estudo retrospectivo foi feito em um único centro na Coreia do Sul entre janeiro de 2010 e junho de 2015. Os critérios de inscrição foram: (1) ITU febril causada por E. coli e Klebsiella spp.; (2) pacientes com internação; (3) pacientes menores de 12 meses. Pacientes internados na semana anterior e com uroculturas coletadas mais de 48 horas após a internação foram excluídos. A ITU foi definida como resultados anormais de urinálise e urocultura positiva (≥ 5×104 unidades formadoras de colônias/mL), de acordo com as diretrizes da Academia Americana de Pediatria.11 A falha precoce no tratamento foi definida como febre persistente por mais de três dias, apesar do tratamento antibiótico. A ITU bacteriana foi definida como sintomas clínicos de ITU com as mesmas bactérias isoladas das uroculturas e hemoculturas ao mesmo tempo. Os prontuários médicos dos pacientes foram analisados com relação a dados como idade, sexo, registros de episódios de ITU e resultados de uroculturas, histórico de saúde, internação anterior e achados laboratoriais e radiológicos. Os possíveis fatores de risco para a produção de ESBL foram idade, sexo, micro‐organismo na urina, ITU anterior, uso de antibióticos, internação anterior nos últimos três meses e doença de base, como doenças neurológicas, cardíacas, respiratórias e renais. Os grupos com ESBL CA e não ESBL CA foram comparados a respeito dos possíveis fatores de risco. O estudo foi aprovado pelos Conselhos de Revisão Institucional de nosso hospital e seguiu a Declaração de Helsinque relevante.
Estudos de diagnóstico por imagemForam investigadas anomalias renais, que incluíram refluxo vésico‐ureteral, hidronefrose e rim displásico. Foram feitos ultrassom (US) renal e exame com ácido dimercaptosuccínico (DMSA) marcado com tecnécio‐99m para determinar quaisquer anomalias anatômicas e a presença de pielonefrite aguda, respectivamente. Os resultados do US foram considerados patológicos em caso de morfologia anormal dos rins e ecogenicidade parenquimatosa, qualquer grau de dilatação do sistema coletor (pelve renal, cálices ou ureter distal) ou espessamento da mucosa da bexiga. Um resultado de DMSA anormal foi definido pela presença de áreas focais ou difusas de absorção reduzida de radionuclídeos, sem evidência de perda cortical, ou pela presença de absorção difusamente reduzida em um rim aumentado.12 O DMSA foi repetido após seis meses para detectar qualquer cicatriz cortical renal. Foi feita cistouretrografia miccional em pacientes com resultados anormais do diagnóstico por imagem. O refluxo vesico‐ureteral (RVU) foi classificado de acordo com a classificação do Comitê Internacional de Estudo do Refluxo.13
Identificação de ESBLsO teste da susceptibilidade antimicrobiana foi feito pelo método de difusão em disco conforme recomendado pelas diretrizes do Instituto de Normas Laboratoriais e Clínicas.14 A produção de ESBL foi determinada pelo teste de sinergia de disco duplo, também de acordo com as diretrizes do Instituto de Normas Laboratoriais e Clínicas.14 Um aumento mínimo de 5mm na área testada em combinação com o ácido clavulânico em comparação com a área testada individualmente foi aceito como uma indicação de produção de ESBL.15
Análise estatísticaAs estatísticas descritivas foram relatadas como média com desvio padrão ou percentuais, quando adequado. As variáveis contínuas foram analisadas com testes t de amostras independentes e as variáveis categóricas foram analisadas com o teste exato de Fisher ou o teste qui‐quadrado. A regressão linear foi usada para avaliar as tendências da prevalência anual de ITU por ESBL CA. A regressão logística foi usada para determinar os fatores de risco de bactérias produtoras de ESBL. Os resultados foram avaliados com intervalos de confiança de 95%. O valor de p<0,05 foi considerado significativo. Todas as análises estatísticas foram feitas com o software SPSS, versão 21.0 (SPSS Inc., IL, EUA).
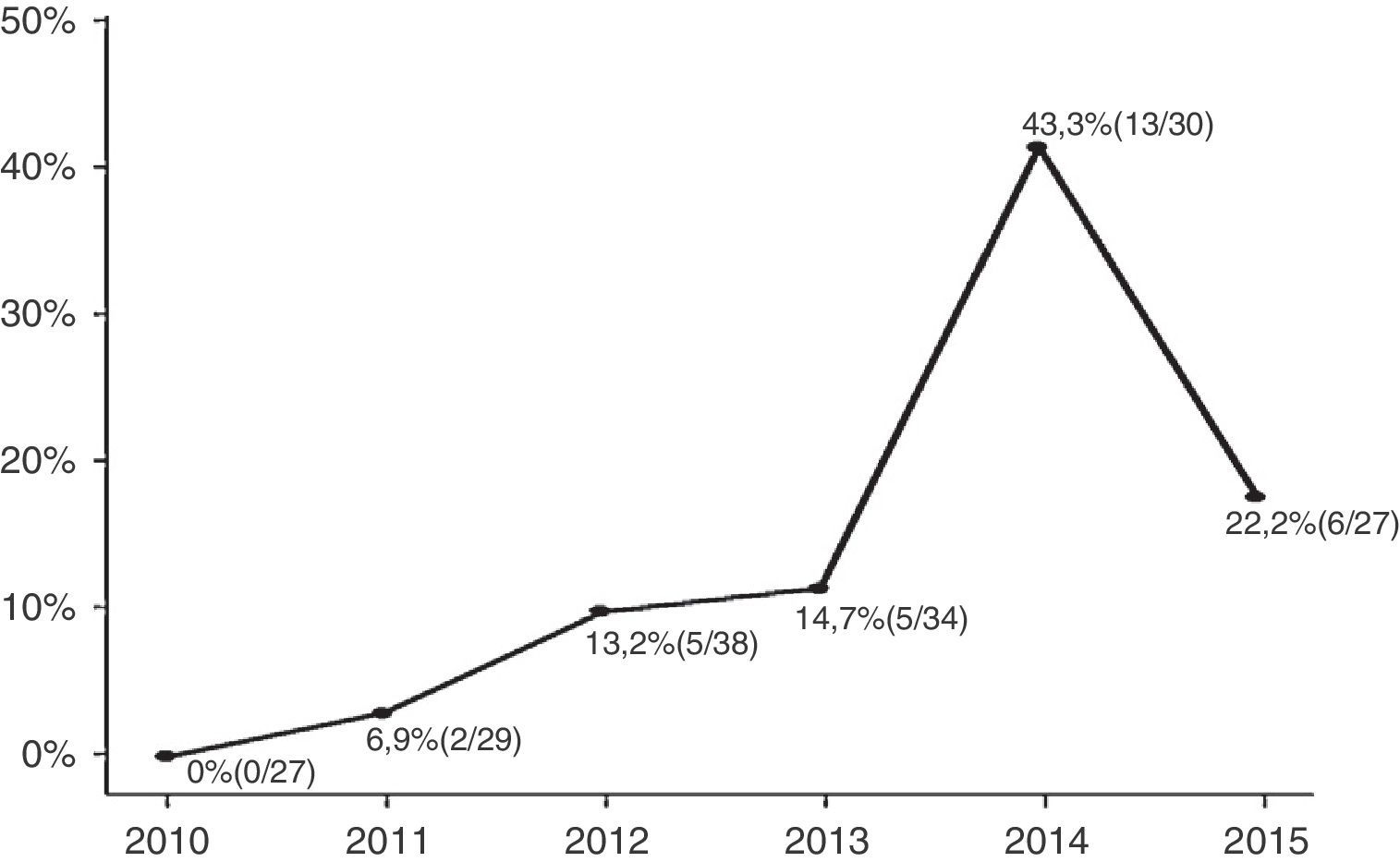
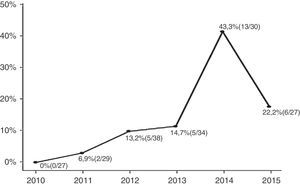
ResultadosForam inscritos 185 neonatos e divididos em dois grupos (ITU por ESBL CA em comparação com não ESBL CA); 31 (16,7%) dos pacientes apresentaram ITU causada por bactérias produtoras de ESBL, ao passo que os 154 pacientes restantes apresentaram bactérias não produtoras de ESBL em suas uroculturas. As proporções de bactérias produtoras de ESBL que causam ITUs foram 0% em 2010, 6,9% em 2011, 13,2% em 2012, 14,7% em 2013, 43,3% em 2014 e 22,2% em 2015. As taxas de incidência anuais de ITU por ESBL CA aumentaram durante o período do estudo e o p da tendência foi significativo (p<0,001) (fig. 1).
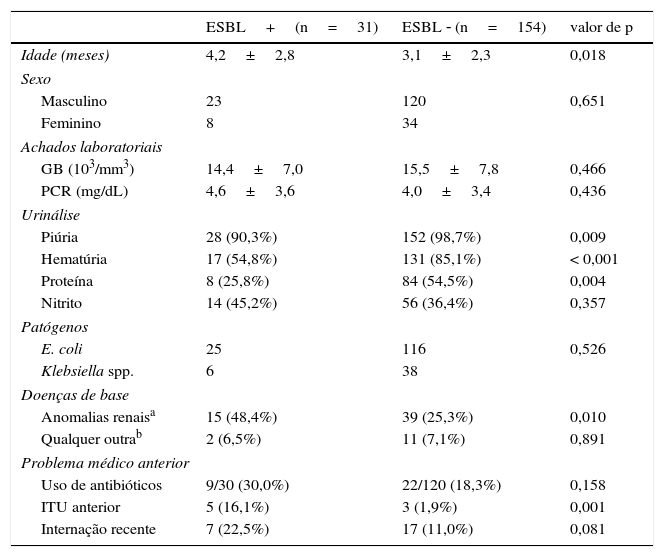
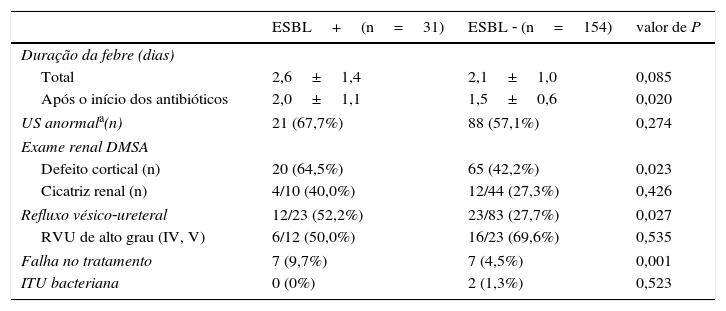
Os grupos com ITU por ESBL CA e não ESBL CA consistiram em 31 (17%) e 154 (83%) pacientes, respectivamente. A idade média era maior no grupo com ITU por ESBL CA do que no grupo com ITU não ESBL CA (4,2±2,8 em comparação com 3,1±2,3 meses, p=0,018). A E. coli foi o patógeno dominante em ambos os grupos: a proporção de produção de ESBL entre a E. coli e a Klebsiella spp. não diferiu (tabela 1). Não foram observadas diferenças no sexo ou nos achados laboratoriais entre os dois grupos. A ITU por ESBL CA levou um tempo mais longo até a defervescência após o início do tratamento que a ITU não ESBL CA (2,0±1,1 em comparação com 1,5±0,6 dias p=0,020) (tabela 1). As anomalias do US não foram diferentes entre os grupos. Os defeitos corticais no exame de DMSA foram mais frequentes na ESBL CA do que no grupo com ITU não ESBL CA (64,5 em comparação com 43,5%, p=0,023); contudo, a presença de cicatrizes renais não diferiu de forma significativa (40 em comparação com 27,3%, p=0,426) (tabela 2). Dos 23 pacientes com ITU por ESBL CA, 12 (52,2%) foram diagnosticados com RVU, cuja taxa foi significativamente maior do que no grupo com ITU não ESBL CA (p=0,027). A ITU bacteriana foi observada em dois pacientes (1,3%) com ITU não ESBL CA. A falha precoce no tratamento foi mais frequente no grupo com ITU por ESBL CA do que no grupo com ITU não ESBL CA (22,6% em comparação com 4,5%, p=0,001).
Características básicas dos pacientes
| ESBL+(n=31) | ESBL ‐ (n=154) | valor de p | |
|---|---|---|---|
| Idade (meses) | 4,2±2,8 | 3,1±2,3 | 0,018 |
| Sexo | |||
| Masculino | 23 | 120 | 0,651 |
| Feminino | 8 | 34 | |
| Achados laboratoriais | |||
| GB (103/mm3) | 14,4±7,0 | 15,5±7,8 | 0,466 |
| PCR (mg/dL) | 4,6±3,6 | 4,0±3,4 | 0,436 |
| Urinálise | |||
| Piúria | 28 (90,3%) | 152 (98,7%) | 0,009 |
| Hematúria | 17 (54,8%) | 131 (85,1%) | < 0,001 |
| Proteína | 8 (25,8%) | 84 (54,5%) | 0,004 |
| Nitrito | 14 (45,2%) | 56 (36,4%) | 0,357 |
| Patógenos | |||
| E. coli | 25 | 116 | 0,526 |
| Klebsiella spp. | 6 | 38 | |
| Doenças de base | |||
| Anomalias renaisa | 15 (48,4%) | 39 (25,3%) | 0,010 |
| Qualquer outrab | 2 (6,5%) | 11 (7,1%) | 0,891 |
| Problema médico anterior | |||
| Uso de antibióticos | 9/30 (30,0%) | 22/120 (18,3%) | 0,158 |
| ITU anterior | 5 (16,1%) | 3 (1,9%) | 0,001 |
| Internação recente | 7 (22,5%) | 17 (11,0%) | 0,081 |
ESBL, β‐lactamase de espectro ampliado; GB, contagem de glóbulos brancos; ITU, infecção do trato urinário; PCR, proteína C reativa.
Curso clínico de ITU por ESBL CA e ITU não ESBL CA
| ESBL+(n=31) | ESBL ‐ (n=154) | valor de P | |
|---|---|---|---|
| Duração da febre (dias) | |||
| Total | 2,6±1,4 | 2,1±1,0 | 0,085 |
| Após o início dos antibióticos | 2,0±1,1 | 1,5±0,6 | 0,020 |
| US anormala(n) | 21 (67,7%) | 88 (57,1%) | 0,274 |
| Exame renal DMSA | |||
| Defeito cortical (n) | 20 (64,5%) | 65 (42,2%) | 0,023 |
| Cicatriz renal (n) | 4/10 (40,0%) | 12/44 (27,3%) | 0,426 |
| Refluxo vésico‐ureteral | 12/23 (52,2%) | 23/83 (27,7%) | 0,027 |
| RVU de alto grau (IV, V) | 6/12 (50,0%) | 16/23 (69,6%) | 0,535 |
| Falha no tratamento | 7 (9,7%) | 7 (4,5%) | 0,001 |
| ITU bacteriana | 0 (0%) | 2 (1,3%) | 0,523 |
DMSA, ácido dimercaptosuccínico; ESBL, β‐lactamase de espectro ampliado; ITU, infecção do trato urinário; RVU, refluxo vesico‐ureteral; US, ultrassonografia.
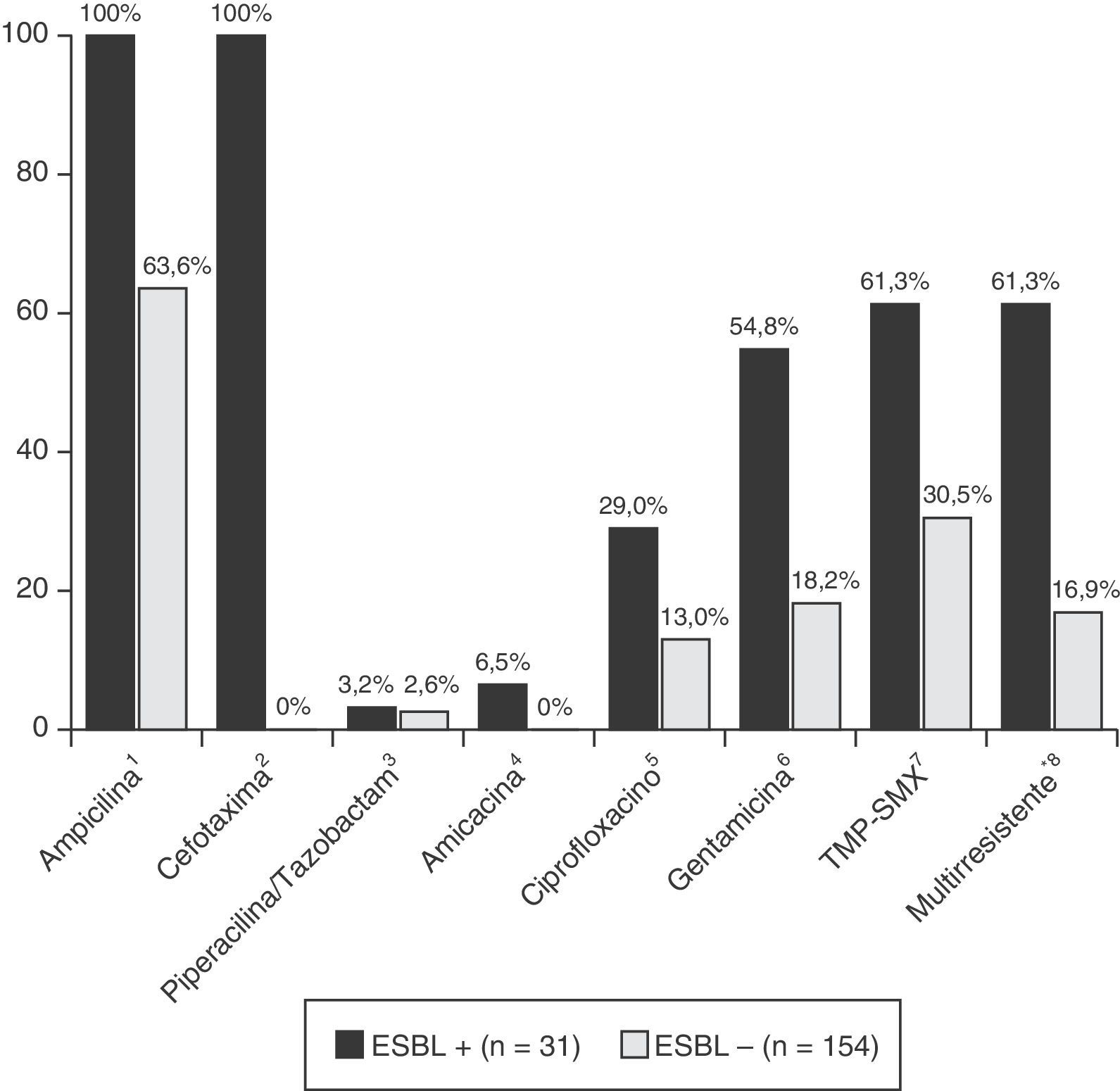
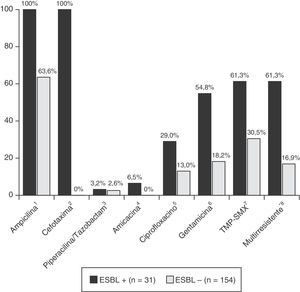
Os pacientes com ITU não ESBL CA apresentaram taxa de resistência antimicrobiana à ampicilina de 63,6%. As taxas de resistência no grupo com ITU por ESBL CA foram 61,3% à TMP‐SMX, 29% ao ciprofloxacino e 54,8% à gentamicina; ao passo que, no grupo com ITU não ESBL CA, elas foram de 30,5% à TMP‐SMX, 13% ao ciprofloxacino e 18,2% à gentamicina (fig. 2). Os pacientes com ITU por ESBL CA apresentaram taxa de resistência significativamente maior a agentes antimicrobianos não β‐lactâmicos: 19 dos 31 isolados de ESBL (61,3%) eram resistentes a pelo menos dois grupos de agentes antibióticos não β‐lactâmicos.
Resistência antibiótica de isolados de bactérias que causam ITU. ITU, infecção do trato urinário; TMP‐SMX, trimetoprima‐sulfametoxazol. *Multirresistente: resistente a mais de dois antibióticos não β‐lactâmicos. Significância calculada pelo teste exato de Fisher: 1p<0,001; 2p<0,001; 3p=1,000; 4p=0,002; 5p=0,005; 6p<0,001; 7p<0,001; 8p<0,001
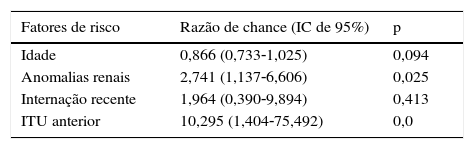
Idade, anomalias renais, ITU anterior e internação recente foram associados a ITU por ESBL CA (tabela 1). A análise de regressão logística identificou anomalia no trato urinário e histórico de ITU anterior como fatores de risco independentes, que se descobriu aumentar o risco 2,7 e 10,3 vezes, respectivamente (tabela 3).
Regressão logística de fatores de risco associados à ITU por ESBL CA em neonatos
| Fatores de risco | Razão de chance (IC de 95%) | p |
|---|---|---|
| Idade | 0,866 (0,733‐1,025) | 0,094 |
| Anomalias renais | 2,741 (1,137‐6,606) | 0,025 |
| Internação recente | 1,964 (0,390‐9,894) | 0,413 |
| ITU anterior | 10,295 (1,404‐75,492) | 0,0 |
ESBL, β‐lactamase de espectro ampliado; ITU, infecção do trato urinário.
O objetivo deste estudo foi destacar o surgimento de ITUs por ESBL CA em neonatos sul‐coreanos e avaliar as características clínicas e possíveis fatores de risco de ITU por ESBL CA em neonatos. Uma incidência cada vez maior de bactérias multirresistentes foi relatada não apenas em infecções hospitalares, como também em infecções CA, principalmente ITUs.8 Assim, a escolha dos antibióticos adequados tornou‐se mais complicada e poderá atrasar a terapia adequada.16,17 Este estudo analisou 185 casos de ITU CA infantil e apresentou uma tendência de aumento na ocorrência de ITU por ESBL CA. Encontramos diferenças significativas no tempo de efervescência e no defeito cortical nos exames de DMSA na ITU por ESBL CA. Nos casos de ITU por ESBL CA, as anomalias do trato urinário, incluindo RVU, foram mais frequentes e as taxas de resistência a outros antibióticos não β‐lactâmicos foram relativamente altas. As anomalias do trato urinário e o histórico de ITU foram considerados fatores de risco independentes.
Nas últimas duas décadas, houve um amplo uso de antibióticos de amplo espectro para conter as taxas crescentes de bactérias produtoras de ESBL em pacientes com ITU em todo o mundo.7,18 A E. coli e a Klebsiella spp., os patógenos mais comuns da ITU, têm mecanismos de resistência antibiótica, inclusive um sistema de efluxo aprimorado, alterações do alvo do medicamento e produção de β‐lactamases mediadas por plasmídeos.19 A resistência normalmente se deve a enzimas β‐lactamase chamadas ESBLs. Os padrões de resistência antibiótica diferem temporal e regionalmente.18,20,21 As taxas de E. coli produtoras de ESBL variam de 2,2% em um estudo18 suíço de 2011 a 55% em um estudo20 chinês de 2009. Diversos fatores estão envolvidos na rápida expansão das bactérias produtoras de ESBL em países com baixo uso de antibióticos, inclusive aquisição a partir de alimentos,22 transmissão entre pessoas a partir de portadores fecais,23 disseminação de bactérias produtoras de ESBL no ambiente24 e existência de reservatórios, como centros de cuidados de longo prazo.25
A maioria dos estudos determinou que os fatores de risco de infecções por bactérias produtoras de ESBL CA normalmente são internação recente, episódios anteriores de ITU, anomalias do trato urinário, doença de base, ITU com Klebsiella spp. e recebimento de profilaxia antimicrobiana para a ITU de cefalosporina.7–9 O uso da profilaxia antimicrobiana é um fator de risco importante para aumentar a resistência antibiótica e a TMP‐SMX reduziu minimamente as susceptibilidades antimicrobianas em comparação à cefalosporina.26 Como apenas dois pacientes receberam a profilaxia antimicrobiana, não conseguimos avaliar o risco da profilaxia antimicrobiana. Em nosso estudo, as anomalias do trato urinário e o histórico de ITU foram considerados fatores de risco independentes de ITU por ESBL CA futura em neonatos. Contudo, um número alto de infecções por bactérias produtoras de ESBL CA ocorre em pacientes sem os fatores de risco óbvios.27 De fato, neste estudo, cerca de 60% dos pacientes com ITU por ESBL CA não apresentaram fatores de risco. Esse resultado pode estar relacionado ao aumento constante no número de portadores saudáveis colonizados por bactérias produtoras de ESBL.23
Uma grande preocupação com relação às bactérias produtoras de ESBL é a alta taxa de resistência cruzada a antibióticos não β‐lactâmicos, como ciprofloxacino, aminoglicosídeos, nitrofurantoína e TMP‐SMX. Neste estudo, 61% dos pacientes apresentaram resistência antibiótica a pelo menos dois antibióticos não β‐lactâmicos úteis usados no tratamento da ITU. Resultados semelhantes foram relatados por outros investigadores.28 A incidência cada vez maior de multirresistência por bactérias produtoras de ESBL pode se tornar um problema no tratamento da ITU.
Muitos estudos relataram que a infecção por essas bactérias pode levar a um atraso na terapia adequada e um aumento simultâneo das taxas de falha no tratamento e comorbidade.21,29 Propor um tratamento antibiótico empírico adequado para a ITU por ESBL CA é difícil e a terapia antibiótica empírica inicial normalmente não tem sucesso. Além disso, quando as bactérias produtoras de ESBL são isoladas, não há quase opção de terapia oral para melhorar os sintomas dos pacientes. Em nosso estudo, a falha do tratamento foi mais frequente no grupo com ITU por ESBL CA; contudo, não houve diferença significativa entre os grupos nas manifestações clínicas como ITU bacteriana ou cicatriz renal. As cepas resistentes não foram associadas à pioria do resultado renal em nosso estudo e estudos anteriores revelaram que a infecção por bactérias produtoras de ESBL aumenta as taxas de falha no tratamento e óbito.21,27,29
Estudos mostraram o reconhecimento crescente de bactérias produtoras de ESBL como causa da infecção CA. A maioria dos dados de infecções por ESBL CA tem como base populações adultas e estão disponíveis relativamente poucos estudos pediátricos.8,9,30 Entre eles, os dados infantis das características clínicas de ITU por ESBL CA e os possíveis fatores de risco são escassos. Porém, como a incidência de bactérias produtoras de ESBL em neonatos com ITUs tem aumentado, é importante entender as alterações epidemiológicas relevantes nos neonatos.
Este estudo tem as seguintes limitações. Primeiro, é retrospectivo. Assim, faltam alguns dados dos prontuários médicos. Segundo, envolveu uma análise em um único centro com um número restrito de pacientes. O tamanho da amostra do grupo com ITU por ESBL CA é pequeno, o que impôs limitações ao poder estatístico. Terceiro, foi feita cistouretrografia miccional (CUGM) apenas quando os achados do estudo de imagem foram anormais. Para obter melhor entendimento das características clínicas e determinar os fatores de risco de ITUs causadas por bactérias produtoras de ESBL em neonatos, são necessários estudos prospectivos de coorte adicionais com base em uma população maior.
Em conclusão, a incidência de ITU causada por bactérias produtoras de ESBL aumentou gradualmente em neonatos sul‐coreanos. As anomalias do trato urinário e ITU anterior foram consideradas fatores de risco independentes significativos associados à ITU por ESBL CA. Nesses pacientes, o reconhecimento dos fatores de risco de ITU por ESBL poderá ajudar a determinar as diretrizes adequadas de manejo e é necessária maior atenção à escolha de terapia antibiótica empírica.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Este estudo foi financiado pela bolsa (HCRI 16916‐1) Chonnam National University Hwasun Hospital Institute for Biomedical Science I.
Como citar este artigo: Kim YH, Yang EM, Kim CJ. Urinary tract infection caused by community‐acquired extended‐spectrum β‐lactamase‐producing bacteria in infants. J Pediatr (Rio J). 2017;93:260–6.