To evaluate the possible association between hyperuricemia and cardiorespiratory fitness levels/nutritional profile, grouped into a single variable, in schoolchildren.
MethodCross‐sectional study of 2335 students from Elementary schools, aged 7–17 years of both genders, stratified by conglomerates of a municipality in Southern Brazil. Body mass index (BMI) was calculated and cardiorespiratory fitness (CRF) was assessed by the 6‐minute run/walk test. The BMI and CRF were grouped into a single variable, considering: (1) low and normal weight/fit; (2) low and normal weight/unfit; (3) overweight‐obesity/fit; (4) overweight‐obesity/unfit. The Poisson regression (prevalence ratio, PR) was used for the association between hyperuricemia and BMI/CRF ratio with 95% confidence intervals and differences were considered significant when p<0.05.
ResultsThere is an association, although subtle, between the presence of hyperuricemia with low levels of CRF and the presence of excess weight, when grouped into a single variable. Boys and girls with this condition have higher prevalence of hyperuricemia (PR: 1.07; p=0.007 for boys; PR: 1.10; p<0.001 for girls).
ConclusionTogether, excess weight and low levels of cardiorespiratory fitness are associated with the presence of hyperuricemia in schoolchildren.
Avaliar a possível relação entre hiperuricemia com aptidão cardiorrespiratória e o estado nutricional, agrupados, em escolares.
MétodoEstudo transversal com 2.335 escolares da educação básica de 7 a 17 anos, de ambos os sexos, estratificados por conglomerados de um munícipio do sul do Brasil. Foi calculado o índice de massa corporal (IMC) e a aptidão cardiorrespiratória (APCR) foi avaliada pelo teste de corrida/caminhada de 6 minutos. O IMC e a APCR foram agrupados em uma única variável, considerando: 1) baixo peso‐normal/apto; 2) baixo peso‐normal/inapto; 3) sobrepeso‐obesidade/apto; 4) sobrepeso‐obesidade/inapto. A regressão de Poisson (razão de prevalência; RP) foi usada para associação entre hiperuricemia e a relação APCR/IMC com intervalos de confiança de 95% e diferenças significativas consideradas para p<0,05.
ResultadosObserva‐se associação, embora sutil, entre a presença de hiperuricemia com baixos níveis de APCR e a presença de excesso de peso, de forma agrupada. Meninos e meninas, com essa condição, têm maior prevalência de hiperuricemia (RP: 1,07; p=0,007; RP: 1,10; p<0,001, respectivamente), em comparação com seus pares com bons níveis de APCR e estado nutricional adequado.
ConclusãoDe forma conjunta, o excesso de peso e os baixos níveis de aptidão cardiorrespiratória estão associados com a presença de hiperuricemia em escolares.
A aptidão cardiorrespiratória (APCR) é um forte preditor de mortalidade em adultos. Seus níveis, na adolescência, têm relação com APCR na fase adulta.1 Além disso, a incidência de baixos níveis de APCR em crianças e adolescentes tem aumentado.2
Atualmente, a APCR tem sido associada com a presença de síndrome metabólica em escolares.3 Sabe‐se que baixos níveis de APCR na infância são preditores de risco metabólico. Portanto, manter os níveis adequados de APCR, desde cedo, é fundamental para a redução da presença de síndrome metabólica na fase adulta.4
Os baixos níveis de APCR têm sido associados com os parâmetros clássicos de síndrome metabólica em escolares.5 Outros marcadores de risco metabólico, não tradicionais, têm sido associados com baixos níveis de APCR, como o ácido úrico, isso demonstra que crianças e adolescentes que têm baixos níveis de APCR apresentam níveis mais elevados desse marcador.6
Porém, a literatura é escassa quanto à relação entre hiperuricemia, níveis de APCR e a presença de sobrepeso/obesidade em crianças e adolescentes, em especial no Brasil. A identificação de um marcador não tradicional, como o ácido úrico, associado aos baixos níveis de APCR e excesso de peso, na infância e adolescência, poderá auxiliar pediatras no diagnóstico precoce, bem como demais profissionais da área da saúde, em especial os profissionais de educação física e nutrição, na elaboração de intervenções, com o intuito de prevenir a ocorrência de risco metabólico na fase adulta. Além disso, o presente estudo traz uma nova abordagem, uma vez que avalia, de forma conjunta, os níveis de APCR e o IMC dos escolares. Diante dessa lacuna e da importância do tema, justifica‐se este estudo, o qual objetivou avaliar possível relação entre hiperuricemia com os níveis de aptidão cardiorrespiratória e o estado nutricional, combinados, em escolares.
MétodoParticiparam do estudo transversal analítico 2.335 escolares, de ambos os sexos, estratificados por conglomerados, 80,3% da zona urbana do município. As idades variaram entre 7 e 17 anos (média = 11,5 anos; desvio‐padrão = 2,8 anos). Todos eram escolares da educação básica do município de Santa Cruz do Sul‐RS, o qual tem 52 escolas de ensino fundamental e médio, 19 estaduais, 29 municipais e quatro particulares, com uma população de 20.380 escolares. Esses dados foram obtidos junto aos órgãos oficiais do governo do município.
Este estudo faz parte de uma pesquisa mais ampla denominada “Saúde dos Escolares – Fase III”, aprovada pelo Comitê de Ética e Pesquisa (CEP) da Universidade de Santa Cruz do Sul (Unisc) sob CAAE n°: 31576714.6.0000.5343, em respeito à Resolução 466/12 do Conselho Nacional de Saúde. Todas as avaliações foram feitas nas dependências da universidade, por profissionais capacitados para cada função. Participaram do estudo apenas escolares com termo de consentimento livre e esclarecido (TCLE) assinado pelos pais ou responsáveis e termo de assentimento assinado pelos escolares com 12 anos ou mais, bem como aqueles que não tivessem restrições para coleta de sangue.
Para o cálculo do tamanho amostral, usou‐se o programa G*Power 3.1 (Heinrich‐Heine‐Universität Düsseldorf, Alemanha), considerou‐se a regressão de Poisson como teste estatístico (presença versus ausência de hiperuricemia como variável dependente). Considerou‐se um poder de teste (1–β)=0,95, nível de significância de α = 0,05 e um tamanho de efeito de 0,30, conforme indicado por Faul et al.7 Dessa forma, estimou‐se uma amostra mínima de 655 escolares.
Participaram do estudo 25 escolas da rede pública e privada, tanto da zona rural quanto urbana. As escolas avaliadas foram selecionadas por sorteio, respeitou‐se a proporcionalidade de densidade populacional de escolares, de acordo com a região do município (centro, norte, sul, leste e oeste) e zona (urbana e rural). Após, foram obtidas as listas de alunos das escolas selecionadas, foram sorteados os alunos para envio do termo de consentimento livre e esclarecido.
Foram incluídos no estudo escolares devidamente matriculados nas escolas sorteadas, de ambos os sexos, entre 7 e 17 anos e que retornaram com o termo de consentimento e assentimento devidamente assinados (2.502 escolares). Desses, foram excluídos 167, devido à incapacidade de coleta sanguínea e feitura do teste de APCR, ou por remoção de dados discrepantes (outliers) do banco de dados, após verificação na análise exploratória.
O IMC foi calculado pela fórmula IMC = peso/altura2 (kg/m2). Para avaliação do peso e da estatura, os escolares foram avaliados descalços e com roupas leves. O IMC foi classificado conforme as curvas de percentis por idade e sexo.8 Os valores obtidos foram reclassificados em duas categorias: baixo peso‐normal e sobrepeso‐obesidade. A APCR foi avaliada pelo teste de corrida/caminhada de seis minutos. Os escolares foram orientados, previamente, a usar calçado adequado e roupa leve para o teste. Os resultados foram obtidos em metros percorridos pelo escolar e classificados de acordo com as tabelas do Projeto Esporte Brasil (PROESP‐BR), para sexo e idade, em zona saudável (bons níveis de APCR; apto) e zona de risco (baixos níveis de APCR; inapto).9
A variável estado nutricional/APCR foi categorizada por meio dos dados de IMC e APCR, obtidos separadamente. Os resultados foram classificados em quatro categorias: 1) baixo peso‐normal/apto; 2) baixo peso‐normal/inapto; 3) sobrepeso‐obesidade/apto e 4) sobrepeso‐obesidade/inapto.
O estágio maturacional foi classificado a partir dos pelos púbicos, em cinco categorias, de acordo com Tanner: estágio I (pré‐puberal), estágio II (inicial de desenvolvimento), estágio III (maturação contínua 1), estágio IV (maturação contínua 2) e estágio V (maturado).10 Foi aplicada uma ficha inquérito com figuras em que os sujeitos assinalavam a que mais se assemelhava com o seu corpo.
A coleta de sangue para a dosagem do ácido úrico foi feita após 12 horas de jejum na veia braquial, no Laboratório de Bioquímica do Exercício da Unisc, por profissionais capacitados (farmacêuticos e técnicos em enfermagem da universidade), com respeito às normas de biossegurança. A concentração de ácido úrico no soro de cada paciente foi determinada por método enzimático fotométrico, com reagente convencional Kovalent e o sistema automatizado Miura 200 (I.S.E., Roma, Itália). Foram considerados como normais valores para ácido úrico inferiores a 5,5mg/dL; valores acima foram considerados hiperuricemia.
Os dados foram analisados no programa estatístico SPSS (IBM Corp. Released 2013. IBM SPSS Statistics para Windows, versão 23.0. NY, EUA) v. 23.0 (IBM–Armonk, NY, United States). Primeiramente, foi usado o teste de Shapiro‐Wilk para testar a normalidade dos dados contínuos. As análises descritivas foram expressas em frequência e percentual. Foi aplicado o teste de qui‐quadrado para comparação das características descritivas dos escolares, por sexo. A associação entre a variável desfecho (hiperuricemia), com a variável categorizada estado nutricional/APCR, foi testada por meio da regressão de Poisson, por meio dos valores de razão de prevalência (RP) e intervalos de confiança (IC) de 95%. As análises foram estratificadas por sexo e ajustadas para faixa etária e estágio maturacional. Foram consideradas significativas as diferenças para p<0,05.
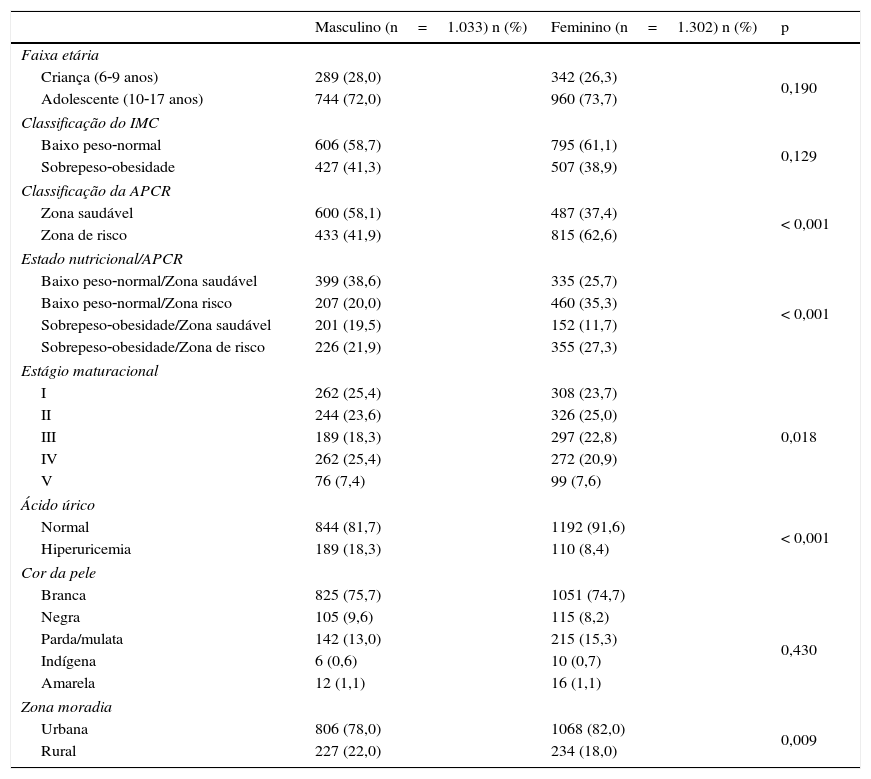
ResultadosForam avaliados 2.335 escolares. Quanto à relação entre o estado nutricional e APCR, 21,9% meninos e 27,3% das meninas se encontravam com sobrepeso‐obesidade/inaptos (tabela 1).
Descrição da amostra. Santa Cruz do Sul, 2014‐2015
| Masculino (n=1.033) n (%) | Feminino (n=1.302) n (%) | p | |
|---|---|---|---|
| Faixa etária | |||
| Criança (6‐9 anos) | 289 (28,0) | 342 (26,3) | 0,190 |
| Adolescente (10‐17 anos) | 744 (72,0) | 960 (73,7) | |
| Classificação do IMC | |||
| Baixo peso‐normal | 606 (58,7) | 795 (61,1) | 0,129 |
| Sobrepeso‐obesidade | 427 (41,3) | 507 (38,9) | |
| Classificação da APCR | |||
| Zona saudável | 600 (58,1) | 487 (37,4) | < 0,001 |
| Zona de risco | 433 (41,9) | 815 (62,6) | |
| Estado nutricional/APCR | |||
| Baixo peso‐normal/Zona saudável | 399 (38,6) | 335 (25,7) | < 0,001 |
| Baixo peso‐normal/Zona risco | 207 (20,0) | 460 (35,3) | |
| Sobrepeso‐obesidade/Zona saudável | 201 (19,5) | 152 (11,7) | |
| Sobrepeso‐obesidade/Zona de risco | 226 (21,9) | 355 (27,3) | |
| Estágio maturacional | |||
| I | 262 (25,4) | 308 (23,7) | 0,018 |
| II | 244 (23,6) | 326 (25,0) | |
| III | 189 (18,3) | 297 (22,8) | |
| IV | 262 (25,4) | 272 (20,9) | |
| V | 76 (7,4) | 99 (7,6) | |
| Ácido úrico | |||
| Normal | 844 (81,7) | 1192 (91,6) | < 0,001 |
| Hiperuricemia | 189 (18,3) | 110 (8,4) | |
| Cor da pele | |||
| Branca | 825 (75,7) | 1051 (74,7) | |
| Negra | 105 (9,6) | 115 (8,2) | 0,430 |
| Parda/mulata | 142 (13,0) | 215 (15,3) | |
| Indígena | 6 (0,6) | 10 (0,7) | |
| Amarela | 12 (1,1) | 16 (1,1) | |
| Zona moradia | |||
| Urbana | 806 (78,0) | 1068 (82,0) | 0,009 |
| Rural | 227 (22,0) | 234 (18,0) | |
APCR, aptidão cardiorrespiratória; IMC, índice de massa corporal; teste de qui‐quadrado, considerando a comparação entre os sexos.
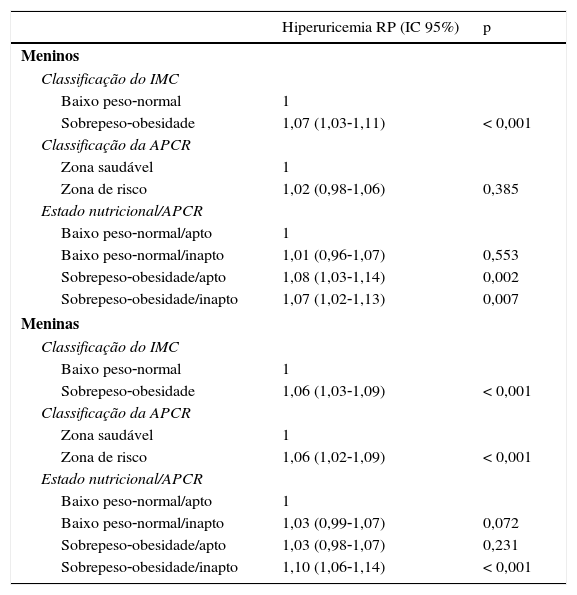
Quando relacionada a hiperuricemia com o estado nutricional, separadamente, verificou‐se que escolares do sexo masculino com sobrepeso ou obesidade têm maior prevalência de hiperuricemia, quando comparados com escolares com baixo peso ou peso normal (RP: 1,07; p<0,001). Entre as meninas, também pode ser verificada essa relação (RP: 1,06; p<0,001). Já quando relacionado com APCR, meninas inaptas apresentaram maior prevalência para hiperuricemia do que meninas aptas (RP: 1,06; p<0,001) (tabela 2).
Relação entre hiperuricemia com APCR e IMC
| Hiperuricemia RP (IC 95%) | p | |
|---|---|---|
| Meninos | ||
| Classificação do IMC | ||
| Baixo peso‐normal | 1 | |
| Sobrepeso‐obesidade | 1,07 (1,03‐1,11) | < 0,001 |
| Classificação da APCR | ||
| Zona saudável | 1 | |
| Zona de risco | 1,02 (0,98‐1,06) | 0,385 |
| Estado nutricional/APCR | ||
| Baixo peso‐normal/apto | 1 | |
| Baixo peso‐normal/inapto | 1,01 (0,96‐1,07) | 0,553 |
| Sobrepeso‐obesidade/apto | 1,08 (1,03‐1,14) | 0,002 |
| Sobrepeso‐obesidade/inapto | 1,07 (1,02‐1,13) | 0,007 |
| Meninas | ||
| Classificação do IMC | ||
| Baixo peso‐normal | 1 | |
| Sobrepeso‐obesidade | 1,06 (1,03‐1,09) | < 0,001 |
| Classificação da APCR | ||
| Zona saudável | 1 | |
| Zona de risco | 1,06 (1,02‐1,09) | < 0,001 |
| Estado nutricional/APCR | ||
| Baixo peso‐normal/apto | 1 | |
| Baixo peso‐normal/inapto | 1,03 (0,99‐1,07) | 0,072 |
| Sobrepeso‐obesidade/apto | 1,03 (0,98‐1,07) | 0,231 |
| Sobrepeso‐obesidade/inapto | 1,10 (1,06‐1,14) | < 0,001 |
Análise ajustada para idade e estágio maturacional; APCR, aptidão cardiorrespiratória; IC, intervalo de confiança; IMC, índice de massa corporal; Regressão de Poisson; RP, razão de prevalência.
Observou‐se associação, embora pequena, entre hiperuricemia com o estado nutricional/APCR, de forma agrupada, com ajuste para idade e estágio maturacional (tabela 2). Escolares do sexo masculino com excesso de peso e inaptos para APCR apresentam maior prevalência de hiperuricemia, quando comparados com indivíduos com peso normal e aptos (RP: 1,07; p=0,007). Valores semelhantes foram encontrados para meninos com excesso de peso, mas que apresentaram boa APCR (RP: 1,08; p=0,002). Entre as meninas avaliadas, foram encontradas diferenças significativas apenas quando comparados excesso de peso e inaptidão cardiorrespiratória com peso normal e bons níveis de APCR (RP: 1,10; p<0,001).
DiscussãoO presente estudo demonstrou, embora de forma sutil, que a presença de hiperuricemia é mais prevalente nos escolares com sobrepeso e obesidade, em meninos e meninas, bem como entre as meninas que apresentam baixos níveis de APCR. Além disso, em ambos os sexos, foi constatada maior prevalência de hiperuricemia nos escolares que apresentam, de forma conjunta, sobrepeso/obesidade e baixos níveis de APCR.
Porém, ressalta‐se que, embora essa relação seja pequena, é relevante, uma vez que a amostra é composta por crianças e adolescentes e as alterações nos níveis de ácido úrico são evidenciadas, de forma mais frequente, na população adulta. Sabe‐se que, nesses indivíduos, os níveis séricos de ácido úrico estão associados com diversos fatores de risco cardiometabólicos, além de hiperuricemia ser preditiva no desenvolvimento de obesidade.11 Embora o ácido úrico tenha função antioxidante no ambiente extracelular, ele tem efeitos prejudiciais, quando entra nas células. Seu impacto prejudicial inclui inibição da função endotelial, indução da agregação de plaquetas, inflamação crônica sistêmica, entre outros.12,13
A partir dos resultados encontrados, é possível perceber que escolares com excesso de peso têm maior prevalência de hiperuricemia, em ambos os sexos, corrobora o que é encontrado na literatura atual. Lee et al.,14 ao avaliar 2.284 crianças entre 6 e 12 anos em 104 escolas de 13 cidades de Taiwan, verificaram que a hiperuricemia está associada com a síndrome metabólica, principalmente com obesidade e gordura abdominal. Em pesquisa com 2.614 crianças em idade escolar (4‐18 anos), na cidade de Bogalusa‐EUA, Sun et al.13 examinaram a associação entre ácido úrico e componentes individuais da síndrome metabólica, níveis elevados de ácido úrico mostraram associação mais forte com IMC.
Uma explicação para a associação entre gordura corporal e hiperuricemia seria o aumento da produção de cetoácidos, durante a noite, naqueles com mais gordura corporal, que causaria uma concorrência entre os ácidos para a excreção renal, além de poder haver predisposição genética para menor excreção de ácido úrico em alguns grupos étnicos.14 Nishida et al. explicam a associação do excesso de peso com a hiperuricemia, devido ao aumento da produção de ácido úrico acoplado com a síntese de triglicerídeos e diminuição da excreção de ácido úrico, como resultado da hiperinsulinemia, que acompanha a obesidade.12
No presente estudo, foi possível verificar que apenas meninas que se encontram em zona de risco para APCR têm maior prevalência de hiperuricemia. Não foram encontradas associações significativas no sexo masculino, o que corrobora estudo feito com indivíduos de todas as idades atendidos no Programa de Atenção à Saúde Cardiovascular da Universidade Federal de Viçosa, que verificaram existir diferenças entre os sexos, quando se associam alterações no ácido úrico com biomarcadores de risco cardiometabólico, como excesso de peso e sedentarismo.15 Essas alterações podem estar associadas ao fato de que meninos e meninas diferem para diversos parâmetros, como os de resistência à insulina, marcadores inflamatórios e produtos do catabolismo de aminoácidos.16 Além disso, meninas apresentam maior percentual de gordura corporal, menores níveis de APCR e são menos ativas,17 o que pode influenciar nos resultados obtidos.
Quando relacionado APCR e o estado nutricional, a prevalência de hiperuricemia é maior quando há excesso de peso, combinado com baixos níveis de APCR. Esse fato ocorreu tanto para meninos quanto para meninas. No sexo masculino, foi possível verificar que escolares com excesso de peso e com bons níveis de APCR também têm maior prevalência de hiperuricemia. Assim, excesso de peso parece ter maior comportamento de risco à saúde do que níveis adequados de APCR. Apesar disso, Barnett et al., em estudo com 1.045 crianças (7‐12 anos) em Nova York‐EUA, associaram níveis inadequados de APCR com a obesidade, consideraram ambos fatores de risco para doenças cardiovasculares, além de APCR classificada na zona de risco na adolescência ter relação com percentuais elevados de gordura corporal na fase adulta.18 Na Espanha, estudo demonstrou que crianças com baixos níveis de APCR apresentam níveis mais elevados de ácido úrico.6 Apesar disso, pouco se sabe sobre a influência da aptidão física, pois são escassas as pesquisas que relacionam exercício físico e níveis de ácido úrico no soro em crianças e adolescentes.
Nishida et al.,12 em Nabeshima‐Japão, verificaram a influência da intensidade da atividade física e do condicionamento aeróbico na concentração de ácido úrico em 71 homens adultos com obesidade. A intensidade moderada de atividade física está associada com níveis mais baixos de ácido úrico. Villegas et al.19 verificaram a prevalência e fatores de risco de hiperuricemia em 3.978 homens adultos (40‐74 anos) em Xangai‐China. A atividade física foi inversamente relacionada com a prevalência da hiperuricemia, enquanto IMC e ganho de peso foram associados positivamente. Williams,20 nos Estados Unidos, analisou distância percorrida por semana e fatores de risco coronarianos em 8.282 corredores homens (15‐80 anos). Os dados foram obtidos por meio de questionário, enquanto as concentrações de dados bioquímicos, entre eles o ácido úrico, foram obtidas a partir de dados cedidos pelos médicos dos corredores. Entre as conclusões, pode ser percebido que corredores de maiores distâncias têm níveis mais baixos de ácido úrico, o que pode estar associado com melhor nível de aptidão cardiorrespiratória.
Estudos com crianças e adolescentes que relacionaram aptidão cardiorrespiratória e níveis de ácido úrico são praticamente inexistentes. O estudo traz contribuições importantes para o entendimento do comportamento no ácido úrico relacionado com variáveis clínicas e metabólicas. Ressalta‐se o número representativo de sujeitos, crianças e adolescentes, cujos dados são pouco disponíveis até o momento. Acredita‐se ser importante adicionar a verificação dos níveis de ácido úrico no soro nos protocolos de avaliação de crianças e adolescentes, pois, a partir dele, pode ser possível a verificação de eventuais complicações cardiovasculares no início do seu desenvolvimento. Barnett et al. também ressaltam a importância das aulas de educação física escolar como uma maneira de aumentar os níveis de APCR das crianças e adolescentes. Isso pode ser alcançado por meio da promoção não só da participação da atividade física, mas da feitura de atividades que acarretem melhoria da APCR, o que traz benefícios tanto na infância e na adolescência quanto para a vida adulta.18
O presente estudo contribui para o conhecimento na área, visto que a relação entre níveis de ácido úrico com APCR e excesso de peso, em crianças e adolescentes, ainda é pouco estabelecida, em especial no Brasil. A relação entre níveis elevados de ácido úrico com APCR e o estado nutricional pode auxiliar profissionais da área da saúde no diagnóstico, tratamento e na prevenção de condições de risco metabólico na infância. Além disso, o estudo traz uma nova abordagem, ao agrupar as variáveis APCR e IMC. Outro ponto forte do estudo é o fato de conter uma amostra representativa de uma população que carece de pesquisas.
Entretanto, o estudo apresenta limitações. Por ser do tipo transversal, não torna possível o estabelecimento de relações de causa e efeito, é possível apenas estabelecer relações entre as variáveis, as quais podem ser influenciadas por fatores intervenientes, como o consumo alimentar dos escolares e a presença de hipertensão arterial, não avaliados no presente estudo, o que pode influenciar indiretamente nos níveis de ácido úrico no soro. Sabe‐se, também, que a obesidade é uma condição multifatorial, a qual também pode ser influenciada por outros marcadores inflamatórios. O uso do IMC também deve ser considerado, uma vez que não é o melhor parâmetro para avaliação de obesidade. Apesar de ser útil em estudos com uma amostra representativa, como no presente, não distingue massa corporal magra e gorda. Sugerem‐se novos estudos que relacionem a intensidade dos exercícios físicos com alterações nos níveis de ácido úrico no soro, para que possa ser possível explorar os efeitos benéficos de um estilo de vida ativo na hiperuricemia.
Concluímos que a hiperuricemia apresentou relação, de forma sutil, com a presença de excesso de peso e baixos níveis de APCR, avaliados de forma conjunta. Sugere‐se que a mensuração do ácido úrico na infância pode ser uma medida de saúde pública útil para intervenção precoce e prevenção de complicações cardiovasculares futuras.
FinanciamentoUniversidade de Santa Cruz do Sul (Unisc).
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Como citar este artigo: Reis LN, Renner JD, Reuter CP, Horta JA, Paiva DN, Valim AR, et al. Hyperuricemia is associated with low cardiorespiratory fitness levels and excess weight in schoolchildren. J Pediatr (Rio J). 2017;93:538–43.
Estudo vinculado à Universidade de Santa Cruz do Sul (Unisc), Santa Cruz do Sul, RS, Brasil.