The aim of this study was to verify the association of echocardiogram, ferritin, C‐reactive protein, and leukocyte count with unfavorable outcomes in pediatric sepsis.
MethodsA prospective cohort study was carried out from March to December 2014, with pediatric critical care patients aged between 28 days and 18 years. Inclusion criteria were diagnosis of sepsis, need for mechanical ventilation for more than 48h, and vasoactive drugs. Serum levels of C‐reactive protein, ferritin, and leukocyte count were collected on the first day (D0), 24h (D1), and 72h (D3) after recruitment. Patients underwent transthoracic echocardiography to determine the ejection fraction of the left ventricle on D1 and D3. The outcomes measured were length of hospital stay and in the pediatric intensive care unit, mechanical ventilation duration, free hours of VM, duration of use of inotropic agents, maximum inotropic score, and mortality.
ResultsTwenty patients completed the study. Patients with elevated ferritin levels on D0 had also fewer ventilator‐free hours (p=0.046) and higher maximum inotropic score (p=0.009). Patients with cardiac dysfunction by echocardiogram on D1 had longer hospital stay (p=0.047), pediatric intensive care unit stay (p=0.020), duration of mechanical ventilation (p=0.011), maximum inotropic score (p=0.001), and fewer ventilator‐free hours (p=0.020).
ConclusionCardiac dysfunction by echocardiography and serum ferritin value was significantly associated with unfavorable outcomes in pediatric patients with sepsis.
Verificar a associação do ecocardiograma, da ferritina, da proteína C reativa (PCR) e da contagem de leucócitos com desfechos desfavoráveis na sepse pediátrica.
MétodosEstudo de coorte prospectivo, de março a dezembro de 2014, com pacientes críticos pediátricos entre 28 dias e 18 anos. Critérios de inclusão foram diagnóstico de sepse, necessidade de ventilação mecânica (VM) por mais de 48 horas e uso de drogas vasoativas. Avaliaram‐se os níveis séricos PCR, ferritina, contagem de leucócitos, no recrutamento (D0), 24 horas (D1) e 72 horas (D3) após o recrutamento. No D1 e no D3 todos os pacientes foram submetidos a ecocardiograma transtorácico para determinação da Fração de Ejeção (FE) do ventrículo esquerdo. Os desfechos avaliados foram tempo de internação hospitalar e na Unidade de Terapia Intensiva Pediátrica (UTIP); duração da VM; horas livres de VM; duração do uso de inotrópicos; escore de inotrópicos máximo e mortalidade.
ResultadosVinte pacientes completaram o estudo. Ferritina elevada no D0 associou‐se com menor tempo livre de ventilação (p=0,046) e maior escore de inotrópicos máximo (p=0,009). A disfunção cardíaca pelo ecocardiograma no D1 relacionou‐se com maior tempo de internação hospitalar (p=0,047), de UTIP (p=0,020), VM total (p=0,011), escore de inotrópicos máximo (p=0,001) e menor tempo livre de VM (p=0,020).
ConclusãoA disfunção cardíaca pelo ecocardiograma e o valor de ferritina sérica associaram‐se significativamente com desfechos desfavoráveis nos pacientes pediátricos com sepse.
A sepse continua a ser uma causa importante de morbidade e mortalidade no ambiente da unidade de terapia intensiva pediátrica (UTIP). Achar ferramentas que possibilitem antecipar ou acompanhar uma evolução desfavorável na sepse pode contribuir para a melhoria do atendimento desses pacientes criticamente enfermos.1,2
Por conta disso, diversos marcadores biológicos têm sido recentemente estudados como avaliadores de evolução de doença nas infecções bacterianas, na sepse e no choque séptico.1–8 Dentre os biomarcadores, os mais usados no nosso meio são a contagem dos leucócitos, a proteína C reativa (PCR) e a ferritina. As duas últimas com escassos estudos em pediatria que relacionem os níveis séricos com desfechos desfavoráveis.1,4,6–8
Na sepse pediátrica, a disfunção miocárdica é uma das principais causas de deterioração clínica do paciente.9 A disfunção miocárdica pode estar presente em até 50% dos casos de sepse grave ou de choque séptico, ocasiona disfunção ventricular sistólica ou diastólica e contribui para o choque e para a mortalidade.10 O ecocardiograma já é usado no manejo de pacientes com choque séptico durante a ressuscitação volumétrica e para escolha da melhor droga vasoativa.11,12 Especula‐se que avaliações obtidas pelo exame ecocardiográfico possam servir como marcadores de evolução na sepse. Além disso, poucos estudos associaram essas medidas com desfechos desfavoráveis na sepse pediátrica.13
Neste estudo observacional, avaliamos a evolução da fração de ejeção do ventrículo esquerdo (FE) medida através do ecocardiograma, da ferritina e da PCR séricas e da contagem de leucócitos em pacientes criticamente enfermos com sepse. Além disso, associamos as medidas desses marcadores com desfechos desfavoráveis.
MétodosEste estudo de coorte prospectivo foi desenvolvido na UTIP do Hospital São Lucas da Pontifícia Universidade Católica do Rio Grande do Sul (PUC‐RS), em Porto Alegre, no Sul do Brasil, de março a dezembro de 2014. Essa unidade atende pacientes de 28 dias a 18 anos com doenças clínicas e cirúrgicas e tem 12 leitos para internação.
Foram incluídos todos os pacientes internados no período descrito que necessitavam de ventilação mecânica (VM) por mais de 48 horas,com apoio cardiovascular (com exceção de dopamina na dose menor do que 5 mcg/kg/min) e que tinham diagnóstico ou suspeita clínica de sepse. Foram critérios de exclusão: cardiopatia congênita, presença de doença endócrina confirmada ou suspeita que envolva eixos somatotróficos e corticotrópicos; necessidade de hemofiltração ou qualquer outra terapia de susbtituição renal; diagnóstico de imunossupressão congênita ou adquirida; alterações metabólicas congênitas confirmadas ou suspeitas do metabolismo da glicose; insuficiência hepática grave; prematuridade e peso inferior a 4kg.
Sepse foi definida como a presença de dois ou mais dos seguintes quatro critérios: taquicardia, taquipneia, alteração de temperatura, leucocitose ou leucopenia para idade na vigência de infecção confirmada ou suspeita. As disfunções orgânicas foram classifcadas de acordo com Goldstein et al.14 Foi considerada síndrome de disfunção de múltiplos órgãos a presença de duas ou mais disfunções orgânicas.
Todos os pacientes do estudo tiveram determinados seus níveis séricos de PCR, ferritina e contagem de leucócitos no momento de entrada no estudo (D0), 24 horas (D1) e 72 horas (D3) depois do recrutamento. A amostra foi estratificada conforme valores de PCR (superiores a 7,6mg/dL e a 16,2mg/dL),2 de ferritina (iguais ou superiores a 300ng/mL)15 e de contagem de leucócitos (inferiores a 5000/uL e superiores a 15.000/uL) para associação com os desfechos.
No D1 e D3 todos os pacientes foram submetidos ao exame de ecocardiograma transtorácico para determinação da fração de ejeção do ventrículo esquerdo (FE). A FE representa o volume ejetado, em porcentagem, do volume diastólico final do ventrículo esquerdo, ou seja, o quanto é ejetado de sangue para a aorta na sístole. A fórmula usada foi a de Teichholz, foi considerada como disfunção cardíaca uma FE<55%.16 Medimos também a fração de encurtamento do ventrículo esquerdo, pela mesma fórmula, em todos os pacientes. Os resultados obtidos foram sobreponíveis, por isso optamos por usar apenas a FE nas análises estatísticas. O aparelho usado foi o modelo Acuson Cypress da marca Siemens (Siemens®, Munique, Alemanha), com transdutor de 3 mHz. Todos os exames usaram o mesmo aparelho e foram feitos pelo mesmo cardiologista pediátrico com experiência do Serviço de Cardiologia Pediátrica do Hospital São Lucas da PUC‐RS. Cada exame teve três medidas consecutivas para minimizar o efeito da variação respiratória, ocasionado principalmente pela ventilação mecânica. Para avaliar a concordância intraobservador foi calculado o Kappa, cujo valor encontrado e considerado aceitável foi de 0,80.
Foram avaliados os seguintes desfechos: tempo de internação hospitalar (dias), tempo de internação na UTIP (dias), tempo de ventilação mecânica total (horas), horas livres de ventilação mecânica (horas), tempo de uso de inotrópicos total (horas), escore de inotrópicos máximo e mortalidade.
Para o cálculo das horas livres de VM considerou‐se um valor máximo de 28 dias de ventilação mecânica (672 horas), ou seja, o valor correpondente ao número de horas livres de ventilação mecânica foi calculado subtraindo‐se o tempo de ventilação mecânica total (horas) de 672 horas. Caso o paciente tenha permanecido mais de 672 horas em VM, foi considerado o valor zero.17 Para o escore de inotrópicos máximo foi levado em consideração o maior valor, obtido em qualquer dia do estudo, calculado por um somatório obtido a partir da fórmula: dose da dopamina+dobutamina+(adrenalina×100)+(noradrenalina×100)+(milrinone×10). Todos expressos em mcg/kg/min.18 O Pediatric Index of Mortality 2 (PIM2) foi calculado no primeiro dia de internação na UTIP como rotina do nosso serviço.19 Foi escolhido como ponto de corte para gravidade o valor de PIM2 igual a 6%, pois é o limite superior de mortalidade histórica da nossa unidade.
Em relação à análise estatística, os dados numéricos foram expressos em valor absoluto e em percentual. Dados demográficos como idade, peso, sexo, tipo de disfunção orgânica, presença de infecção e origem do paciente foram obtidos por meio de registro no prontuário eletrônico. Para verificação de normalidade das amostras, foi usado o teste de Kolmogorov‐Smirnov, foi considerada uma amostra normal quando o valor fosse>0,05. Variáveis qualitativas (categóricas) foram expressas em valores reais e percentagem e quando estratificada a amostra, os grupos foram comparados com o teste qui‐quadrado de Pearson ou teste exato de Fischer. Variáveis quantitativas foram expressas por média e desvio padrão e aquelas com distribuição assimétrica, em mediana e intervalo interquartil (IIQ). No caso de a amostra ser estratificada, os grupos foram comparados com teste t de Student ou Anova para variáveis com distribuição normal e teste de Mann‐Whitney‐Wilcoxon ou Kruskal‐Wallis para variáveis com distribuição não normal. Foram considerados significativos os valores de p<0,05. A análise dos dados foi feita com o programa IBM Statistical Package for the Social Sciences (IBM SPSS Statistics 20).
Este estudo foi aprovado pelo Comitê de Ética em Pesquisa do Hospital São Lucas da PUC‐RS, sob o parecer número 474.050, expedido em 27/11/2013. Para participação no estudo, foi solicitada a autorização através de termo de consentimento informado para os pais ou responsáveis de todos os pacientes recrutados.
ResultadosDurante o período de recrutamento houve 337 internações. Dessas, 41 pacientes foram elegíveis para o estudo. O consentimento dos pais não foi concedido em quatro deles e uma criança morreu antes do início da coleta dos exames. Dos 36 que coletaram as amostras, foram excluídas oito crianças a posteriori por não completarem o estudo ecocardiográfico e oito por erro, perda ou por coleta insuficiente de algum material do estudo. As 20 crianças restantes completaram o protocolo. Não se observou diferença nas características basais, na gravidade medida pelo PIM2 e na mortalidade entre os pacientes excluídos e os que permaneceram no estudo. As características gerais da população em estudo estão descritas na tabela 1.
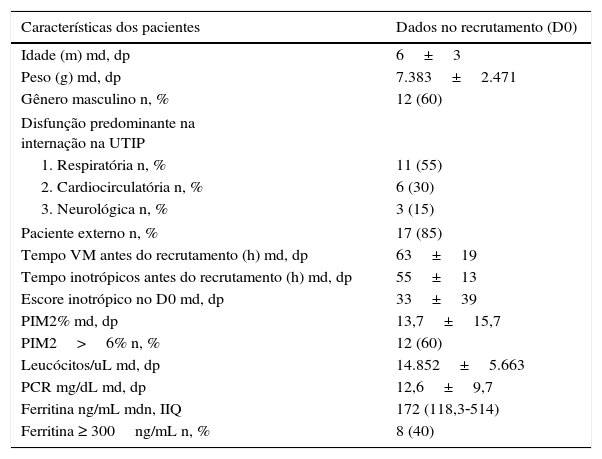
Características gerais da amostra no recrutamento
| Características dos pacientes | Dados no recrutamento (D0) |
|---|---|
| Idade (m) md, dp | 6±3 |
| Peso (g) md, dp | 7.383±2.471 |
| Gênero masculino n, % | 12 (60) |
| Disfunção predominante na internação na UTIP | |
| 1. Respiratória n, % | 11 (55) |
| 2. Cardiocirculatória n, % | 6 (30) |
| 3. Neurológica n, % | 3 (15) |
| Paciente externo n, % | 17 (85) |
| Tempo VM antes do recrutamento (h) md, dp | 63±19 |
| Tempo inotrópicos antes do recrutamento (h) md, dp | 55±13 |
| Escore inotrópico no D0 md, dp | 33±39 |
| PIM2% md, dp | 13,7±15,7 |
| PIM2>6% n, % | 12 (60) |
| Leucócitos/uL md, dp | 14.852±5.663 |
| PCR mg/dL md, dp | 12,6±9,7 |
| Ferritina ng/mL mdn, IIQ | 172 (118,3‐514) |
| Ferritina ≥ 300ng/mL n, % | 8 (40) |
Normalidade verificada pelo teste de Kolmogorov‐Smirnov.
D0, dia zero; dp, desvio padrão; g, gramas; h, horas; IIQ, intervalo interquartil; m, meses; md, média; mdn, mediana; n, número; PCR, proteína C reativa; PIM2, Pediatric Index of Mortality 2; VM, ventilação mecânica; %, percentagem.
No recrutamento, quando estratificados pela gravidade (PIM2<6% ou ≥ 6%), não encontramos diferenças nas características demográficas, nos diagnósticos na internação, no tempo de VM, no tempo de uso e no escore de inotrópicos. Entre os marcadores laboratoriais de resposta inflamatória, a contagem de leucócitos e a PCR também não foram diferentes entre os grupos. Apenas os valores de ferritina foram mais elevados entre os mais graves (média e desvio padrão de 454,4±309,7 versus 91,9±6ng/mL; p=0,005).
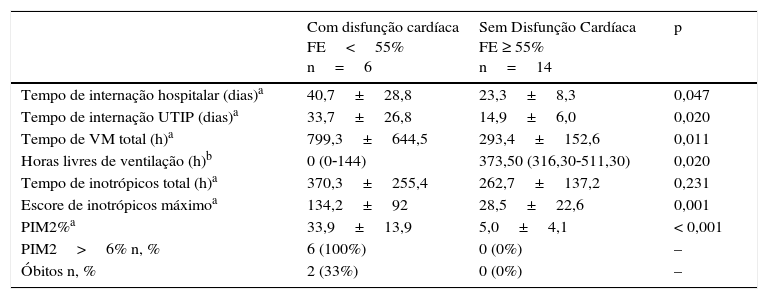
Desempenho cardíaco (FE)Todos os pacientes foram submetidos a ecocardiograma no primeiro e terceiro dia do estudo depois do recrutamento. De forma geral, os valores de FE aumentaram de forma discreta e não significativa no intervalo de estudo. Seis pacientes (30%) apresentaram FE<55%, o que caracterizou disfunção cardíaca. Desses, dois (10%) recuperaram a função cardíaca no D3. Pacientes com disfunção cardíaca no primeiro dia tinham PIM2 mais elevado no momento de admissão na UTIP e apresentaram significativa associação com desfechos desfavoráveis. Dois pacientes desse grupo foram a óbito (tabela 2).
Disfunção cardíaca pelo ecocardiograma no primeiro dia (D1) pós‐recrutamento e desfechos
| Com disfunção cardíaca FE<55% n=6 | Sem Disfunção Cardíaca FE ≥ 55% n=14 | p | |
|---|---|---|---|
| Tempo de internação hospitalar (dias)a | 40,7±28,8 | 23,3±8,3 | 0,047 |
| Tempo de internação UTIP (dias)a | 33,7±26,8 | 14,9±6,0 | 0,020 |
| Tempo de VM total (h)a | 799,3±644,5 | 293,4±152,6 | 0,011 |
| Horas livres de ventilação (h)b | 0 (0‐144) | 373,50 (316,30‐511,30) | 0,020 |
| Tempo de inotrópicos total (h)a | 370,3±255,4 | 262,7±137,2 | 0,231 |
| Escore de inotrópicos máximoa | 134,2±92 | 28,5±22,6 | 0,001 |
| PIM2%a | 33,9±13,9 | 5,0±4,1 | < 0,001 |
| PIM2>6% n, % | 6 (100%) | 0 (0%) | – |
| Óbitos n, % | 2 (33%) | 0 (0%) | – |
Normalidade verificada pelo teste de Kolmogorov‐Smirnov.
h, horas; n, número; PIM2, Pediatric Index of Mortality 2; VM, ventilação mecânica; %, percentagem.
Os mediadores inflamatórios apresentaram‐se elevados no recrutamento e com diferentes padrões no decorrer do estudo. A ferritina apresentou‐se dentro dos limites da normalidade na maioria dos pacientes, sem queda significativa no D3. Os níveis da PCR apresentaram‐se extremamente elevados no recrutamento e diminuíram significativamente, mas ainda com níveis anormais no D3. Os leucócitos totais permaneceram elevados durante todo o período de estudo (tabela 3).
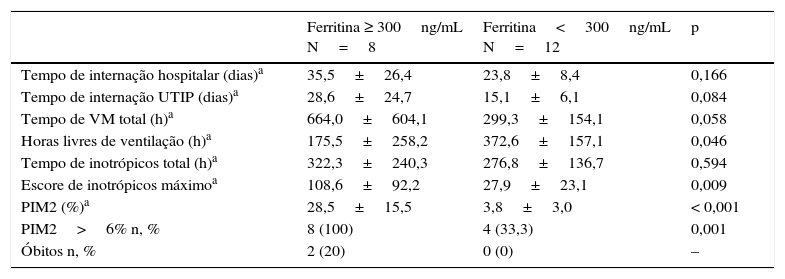
Pacientes com hiperferritinemia (≥ 300ng/mL) no recrutamento (D0) eram mais graves no primeiro dia de internação na UTIP (PIM2 mais elevado) e apresentaram os piores desfechos. Os dois pacientes que evoluíram ao óbito pertenciam a esse grupo (tabela 4).
Hiperferritinemia no recrutamento (D0) e desfechos
| Ferritina ≥ 300ng/mL N=8 | Ferritina<300ng/mL N=12 | p | |
|---|---|---|---|
| Tempo de internação hospitalar (dias)a | 35,5±26,4 | 23,8±8,4 | 0,166 |
| Tempo de internação UTIP (dias)a | 28,6±24,7 | 15,1±6,1 | 0,084 |
| Tempo de VM total (h)a | 664,0±604,1 | 299,3±154,1 | 0,058 |
| Horas livres de ventilação (h)a | 175,5±258,2 | 372,6±157,1 | 0,046 |
| Tempo de inotrópicos total (h)a | 322,3±240,3 | 276,8±136,7 | 0,594 |
| Escore de inotrópicos máximoa | 108,6±92,2 | 27,9±23,1 | 0,009 |
| PIM2 (%)a | 28,5±15,5 | 3,8±3,0 | < 0,001 |
| PIM2>6% n, % | 8 (100) | 4 (33,3) | 0,001 |
| Óbitos n, % | 2 (20) | 0 (0) | – |
h, horas; n, número; PIM2, Pediatric Index of Mortality 2; VM, ventilação mecânica; %, percentagem.
Normalidade verificada pelo teste de Kolmogorov‐Smirnov.
Este foi um dos poucos estudos de coorte que analisaram em conjunto biomarcadores de sepse, medidas de ecocardiograma, evolução e desfechos em pacientes pediátricos criticamente enfermos. Nossos critérios de inclusão foram rígidos, todos os pacientes estavam em ventilação mecânica havia pelo menos 48 horas e necessitavam de suporte de drogas vasoativas. O PIM2 foi maior do que 6% em 12 pacientes (60%), o que indica a alta gravidade dos indivíduos recrutados. A mortalidade encontrada foi de 10%, que é compatível com a literatura.18,20 Nosso estudo demonstrou uma associação significativa entre baixa função sistólica cardíaca, representada pela FE, e hiperferritinemia com desfechos desfavoráveis.
A disfunção cardíaca na sepse pediátrica é uma condição já amplamente conhecida, mas ainda não totalmente compreendida.9 O achado de disfunção cardíaca de ventrículo esquerdo no choque séptico (baixa FE) de 30% é compatível com estudos publicados recentemente por Raj et al., 37%; Pulido et al., 27%; e Furian et al., 33%.9,21,22 Os dois últimos autores não encontraram relação entre a baixa FE e desfechos desfavoráveis ou mortalidade em pacientes adultos. Entretanto, Carmona et al. encontraram aumento da mortalidade em pacientes pediátricos com choque séptico que apresentavam FE menor do que 45% no primeiro dia de internação na UTIP, resultado semelhante ao do nosso estudo.13 Nenhum desses trabalhos associou a disfunção cardíaca medida pela FE com outros desfechos clínicos. Uma possível explicação para os nossos achados é que a disfunção cardíaca, na sepse grave ou no choque séptico, exerce maior influência sobre o quadro clínico do paciente pediátrico quando comparado com o do paciente adulto, que tem predominantemente choque vasoplégico.9,10 Assim, um paciente que já está com a terapia inotrópica aprimorada e ainda tem disfunção cardíaca, terá uma tendência a apresentar piores desfechos.
A ferritina foi o marcador inflamatório que mais se destacou no nosso estudo. Ela é uma proteína armazenadora de ferro responsável por liberá‐lo de forma controlada. Em processos inflamatórios há grande produção dessa proteína, que induz uma diminuição de ferro sérico, acredita‐se que para minimizar a disponibilidade de ferro para microrganismos. Por esse motivo, a ferritina em pacientes críticos pediátricos pode estar elevada e estar associada à gravidade em algumas doenças.6–8 A chance de óbito em um paciente com ferritina acima de 3.000ng/mL é três vezes maior.8 No nosso estudo, 40% dos pacientes encontravam níveis elevados desse biomarcador no D0. Quando estratificamos a amostra em dois grupos, com o ponto de corte de 300ng/mL, notamos uma relação significativa entre hiperferritinemia e desfechos desfavoráveis, como menos horas livres de ventilação mecânica e maior escore de inotrópicos máximo. Além disso, os dois pacientes que foram a óbito pertenciam a esse grupo. Garcia et al. já haviam relacionado níveis de ferritina acima de 500ng/mL com mortalidade.6 A hiperferritinemia sustentada ou valores muito elevados desse marcador representam um cenário de intensa resposta inflamatória que deveria ser benéfica, mas que parece ser indicador de desfechos desfavoráveis.7 Usamos um ponto de corte de 300ng/mL, pois em estudo prévio de Laks e Garcia15 esse foi o valor próximo da mediana dos pacientes com choque séptico. A diminuição do ponto de corte para 300ng/mL valoriza os resultados do nosso estudo.
Rey et al. publicaram no seu estudo em 2007 uma estratificação de valores da PCR em pacientes pediátricos com SIRS, sepse, sepse grave e choque séptico.2 Assim como Rey, no nosso estudo, a PCR no recrutamento estava elevada como no choque séptico (12,6±9,7mg/dL) e demonstrou uma queda significativa nos dias subsequentes. No D3, os pacientes ainda apresentavam valores anormais desse biomarcador (3,5±1,8mg/dL). Entretanto, não houve relação dos valores mais elevados da PCR, encontrados na nossa amostra, com desfechos desfavoráveis. Estudos que estratificam valores da PCR no choque séptico em pacientes pediátricos são escassos. A contagem de leucócitos também não foi útil como marcador de gravidade. Seu valor permaneceu constante. Inicialmente, para análise dos leucócitos, usamos valores de normalidade como referência, pois não encontramos na literatura valores limites que definissem prognóstico para esse marcador. Alguns estudos já haviam demonstrado a baixa validade da contagem de leucócitos como marcador diagnóstico e prognóstico na sepse pediátrica.2,23
Limitações do estudoAlgumas limitações do nosso estudo podem ser apontadas. A primeira em relação à medida da FE através do ecocardiograma, que é um exame profissional dependente. Esse método foi escolhido, apesar da sua limitação, por ser disponível na maioria dos serviços de UTIP do Brasil. A segunda é o uso do PIM2 como desfecho, é um índice prognóstico que indica mortalidade. Pacientes com disfunção cardíaca e hiperferritinemia tinham PIM2 mais elevado. Levando em consideração que se usa o PIM2 em populações de pacientes para estimar mortalidade, o achado da relação dessa medida de gravidade com biomarcadores permite uma interessante aplicação desse índice, que é amplamente usado nas UTIP do nosso meio. A terceira é a falta de outros biomarcadores que já são estudados na sepse pediátrica. Optamos por estudar aqueles que são de fácil obtenção e mais comumente usados no nosso meio. Por fim, apontamos o número de pacientes como uma limitação. Estudamos um grupo expressivo de pacientes muito graves, nos quais os critérios de inclusão e exclusão foram rígidos. A nossa amostra, embora aponte diferenças significativas nos resultados, tem um baixo poder estatístico.
Em resumo, a disfunção cardíaca pelo ecocardiograma (FE<55%) no D1 e o valor de ferritina sérica (≥ 300ng/ml) no D0, obtidos em pacientes pediátricos com sepse internados na UTIP, associaram‐se significativamente a desfechos desfavoráveis.
FinanciamentoConselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq), processo 485488/2011‐6 de Apoio a Projetos de Pesquisa ‐ Universal 14/2011.
Conflitos de interesseDr. Pedro Celiny R. Garcia recebe uma bolsa de pesquisa da Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (Capes). Os outros autores declaram não haver conflitos de interesse.
À Capes, pelo fornecimento das bolsas de estudos, e ao Programa de Pós‐Graduação em Pediatria e Saúde da Criança da PUC‐RS pela possibilidade de feitura deste trabalho.
Como citar este artigo: Tonial CT, Garcia PC, Schweitzer LC, Costa CA, Bruno F, Fiori HH, et al. Cardiac dysfunction and ferritin as early markers of severity in pediatric sepsis. J Pediatr (Rio J). 2017;93:301–7.
Trabalho vinculado à Pontifícia Universidade Católica do Rio Grande do Sul (PUC‐RS), Programa de Pós‐Graduação em Pediatria e Saúde da Criança, Porto Alegre, RS, Brasil.