HIV‐infected individuals (HIVI) are threatened by meningococcal infection and presented lower response to vaccines. Data are scarce on long‐term persistence of human serum bactericidal antibody (hSBA) after a meningococcal C conjugate (MCC) vaccine in HIVI youth; the authors aimed to describe this persistence in HIVI.
MethodsHIVI and HIV uninfected individuals (HIVU), aged 2–18 years, CD4 >15% were recruited. Seroprotection (hSBA ≥1:4) at baseline and at 12–18 months after immunization was evaluated and the association of the different factors with the long‐term persistence was calculated using logistic regression.
ResultsA total of 145 HIVI, 50 HIVU were recruited and immunized, and their median age was 11 years (median age in HIVI group was 12 years, and 10 years in HIVU group, p‐value=0.02). 85 HIVI (44%) had undetectable viral load (UVL). Seroprotection rate was 27.2%: 24.1% in HIVI and 36% in HIVU 12–18 months after immunization (p=0.14). Baseline immunity (odds ratio [OR]=70.70, 95% CI: 65.2–766.6); UVL at entry (OR: 2.87, 95% CI: 0.96–8.62) and lower family income (OR: 0.09, 95% CI: 0.01–0.69) were associated with seroprotection among HIVI.
ConclusionSeroprotection at 12–18 months after single dose of MCC was low for both groups, and higher among individuals who presented baseline immunity. Among HIVI, vaccine should be administered after UVL is achieved.
As pessoas infectadas pelo HIV (HIVI) estão sujeitas a infecção meningocócica e apresentam menor resposta a vacinas. São escassos os dados a respeito da persistência de longo prazo do anticorpo bactericida no soro humano (hSBA) após vacina conjugada meningocócica C (MCC) em HIVI jovens e visamos a descrever essa persistência em HIVI.
MétodosForam recrutadas pessoas HIVI e pessoas não infectadas por HIV (HIVU), entre 2 e 18 anos, CD4>15%. A seroproteção (hSBA ≥ 1:4) basal aos 12–18 meses após a imunização foi avaliada e a associação dos diferentes fatores com a persistência de longo prazo foi calculada com a regressão logística.
ResultadosForam recrutados 145 HIVI e 50 HIVU e imunizados e sua idade média foi determinada em 11 anos (12 no grupo HIVI e 10 no grupo HIVU, valor de p=0,02); 85 HIVI (44%) apresentaram carga viral indetectável (CVI). A taxa de seroproteção foi 27,2%: 24,1% no grupo HIVI e 36% no grupo HIVU 12‐18 meses após imunização (p=0,14). A imunidade basal [razão de chance (RC)=7070, IC: 65,2–7666]; CVI no momento da participação (RC: 2,87, IC de 95%: 0,96‐8,62) e renda familiar mais baixa (RC: 0,09, IC de 95%: 0,01‐0,69) foram associadas a seroproteção entre as pessoas HIVI.
ConclusãoA seroproteção aos 12‐18 meses após única dose de MCC mostrou‐se baixa em ambos os grupos e mais elevada entre as pessoas que apresentaram imunidade basal. Entre as pessoas HIVI, as vacinas devem ser administradas após a CVI ser atingida.
A doença meningocócica (DM) é uma importante causa de septicemia e meningite e um grande desafio de saúde pública em todo o mundo.1,2 As pessoas que convivem com a infeção por vírus da imunodeficiência humana (HIV) estão mais expostas à DM. Estudos demonstraram um risco 5‐10 vezes maior de DM entre crianças infectadas por HIV (HIVI) e quase 10 vezes maior entre adolescentes e adultos em comparação com pessoas não infectadas por HIV (HIVU).3,4 Além disso, as crianças e os adolescentes HIVI apresentam menores taxas de resposta à vacina apesar de ser submetidos à terapêutica antirretroviral de combinação (TARc).5–7 Os anticorpos induzidos pela vacina também podem diminuir mais rapidamente em pessoas portadoras de HIV do que em indivíduos saudáveis. Isso indica que a reconstituição imune não foi suficiente para garantir proteção de longo prazo e destaca a importância de avaliar a imunogenicidade de longo prazo a vacinas meningocócicas e fatores que podem estar associados a uma melhor resposta.8,9
A persistência dos anticorpos após vacinas conjugadas meningocócicas do sorogrupo C (MCC) foi estudada em muitas populações de alto risco com diferentes graus de imunossupressão, porém há poucos estudos em pessoas infectadas por HIV.10–12 Os objetivos deste estudo foram: 1) avaliar a persistência do anticorpo bactericida no soro em relação ao meningococo sorogrupo C. Para avaliá‐lo, usamos complemento humano (hSBA) em crianças e adolescentes HIVI aos 12‐18 meses após uma única dose de MCC, comparamo‐los com os participantes no grupo HIVU; e 2) avaliamos os fatores associados à persistência de anticorpos.
Material e métodosModelo e população do estudoIsso foi um estudo de coorte prospectivo de crianças e adolescentes infectados e não infectados por HIV acompanhados de fevereiro de 2011 a dezembro de 2012 no Instituto de Puericultura e Pediatria Martagão Gesteira (IPPMG), hospital pediátrico da Universidade Federal do Rio de Janeiro, centro de referência para cuidados de pacientes portadores de HIV no Rio de Janeiro. Eles foram recrutados na sala de espera da clínica.
Os critérios de elegibilidade foram: 2 a 18 anos, não ter recebido vacina meningocócica conjugada, não ter recebido vacina viva 4 semanas antes da participação e não ter planejado receber outras vacinas em 2 semanas. Para o grupo de pessoas infectadas por HIV, os critérios de elegibilidade adicionais foram infecção por HIV (definida como dois testes anti‐HIV reativos em crianças>2 anos), ausência dos estágios clínicos 3 ou 4, pela Organização Mundial de Saúde, da doença clínica de HIV no momento da participação e contagem de linfócitos T (CD4) igual ou superior a 350 células/mm3 e/ou 15% no momento de aceitação de participação no estudo. As pessoas não infectadas por HIV foram recrutadas da clínica e envolveram crianças saudáveis no mesmo hospital, eles deveriam apresentar resultado negativo da sorologia para HIV após 18 meses de idade; o teste foi novamente exigido na participação para aqueles que eram sexualmente ativos, para poderem participar. Os indivíduos em ambos os grupos deveriam morar na mesma área geográfica.
Os critérios de exclusão incluíram gravidez, qualquer outra doença imunossupressora, uso de medicamentos imunossupressores sistêmicos, uso de antibióticos por até 3 semanas ou terapia de imunoglobulina nos últimos 6 meses antes da participação, distúrbios hemorrágicos que excluíssem injeção intramuscular, reações adversas a quaisquer componentes da vacina e transtorno psiquiátrico, inclusive intoxicação por drogas ilícitas ou álcool no momento da entrevista (paciente ou responsável legal). Teste de gravidez negativo foi exigido antes da imunização para pacientes em idade reprodutiva. Todos os participantes receberam uma dose (0,5mL de injeção intramuscular de deltoide) de oligossacarídeo meningocócico C conjugado com proteína CRM197, um toxoide da Corynebacterium diphtheria, (Vacinas Chiron/Novartis, Siena, Itália) entre fevereiro de 2001 e dezembro de 2012. Para os voluntários infectados por HIV, a vacina foi fornecida pelo Ministério da Saúde do Brasil; para pacientes não infectados por HIV, foi concedida uma bolsa de pesquisa.
As amostras de sangue para anticorpos N. meningitidis do sorogrupo C com medições dos hSBA, virológicas e imunológicas, bem como questionários padronizados, foram coletadas. Os dados clínicos, laboratoriais e socioeconômicos foram coletados no momento da participação e 1‐2 e 12‐18 meses nas visitas pós‐imunização. Os dados demográficos, clínicos, virológicos e imunológicos foram obtidos dos prontuários médicos (tabela 1). Foram registrados os resultados da contagem de carga viral (CV) e CD4 antes, no início e após a TARc, bem como os dados de nadir e zênite.
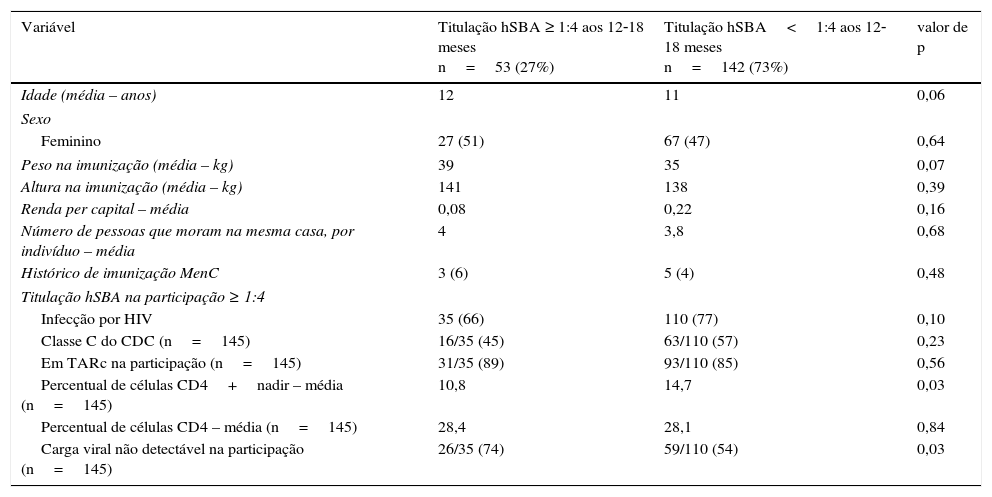
Diferença entre pacientes com titulação hSBA ≥ ou<1:4 aos 12‐18 meses
| Variável | Titulação hSBA ≥ 1:4 aos 12‐18 meses n=53 (27%) | Titulação hSBA<1:4 aos 12‐18 meses n=142 (73%) | valor de p |
|---|---|---|---|
| Idade (média – anos) | 12 | 11 | 0,06 |
| Sexo | |||
| Feminino | 27 (51) | 67 (47) | 0,64 |
| Peso na imunização (média – kg) | 39 | 35 | 0,07 |
| Altura na imunização (média – kg) | 141 | 138 | 0,39 |
| Renda per capital – média | 0,08 | 0,22 | 0,16 |
| Número de pessoas que moram na mesma casa, por indivíduo – média | 4 | 3,8 | 0,68 |
| Histórico de imunização MenC | 3 (6) | 5 (4) | 0,48 |
| Titulação hSBA na participação ≥ 1:4 | |||
| Infecção por HIV | 35 (66) | 110 (77) | 0,10 |
| Classe C do CDC (n=145) | 16/35 (45) | 63/110 (57) | 0,23 |
| Em TARc na participação (n=145) | 31/35 (89) | 93/110 (85) | 0,56 |
| Percentual de células CD4+nadir – média (n=145) | 10,8 | 14,7 | 0,03 |
| Percentual de células CD4 – média (n=145) | 28,4 | 28,1 | 0,84 |
| Carga viral não detectável na participação (n=145) | 26/35 (74) | 59/110 (54) | 0,03 |
CDC, Centros de Controle e Prevenção de Doenças – classificação clínica do HIV; hSBA, ensaio bactericida do soro humano; MenC, vacina meningocócica C não conjugada contra polissacarídeos; TARc, terapia antirretroviral combinada.
Os resultados da imunogenicidade e de segurança de curto prazo após a primeira dose de imunização com MCC foram relatados anteriormente.13 O ensaio com hSBA foi feito conforme descrito anteriormente.13,14 A seroproteção foi definida como titulação hSBA ≥ 1:4 e os indivíduos foram classificados como persistência ao hSBA de acordo com a presença da titulação ≥ 1:412‐18 meses após imunização.
Análise estatísticaAs variáveis contínuas e categóricas foram comparadas entre as pessoas infectadas e não infectadas por HIV, com os testes exatos de Mann‐Whitney e Fisher, respectivamente. Comparamos as variáveis contínuas e categóricas entre as pessoas de acordo com a persistência de anticorpos com a análise de regressão logística. As variáveis com valores de p<0,15 na análise univariada foram incluídas em um modelo de regressão logística. Usamos a mesma estratégia para estudar as variáveis inerentes à infecção por HIV para avaliar um modelo exclusivo de população infectada por HIV. A relevância estatística foi definida como valor de p≤0,05.
Todas as análises foram feitas com o software STATA (versão 13.0; Stata Corporation, TX, EUA).
Seres humanosA aprovação ética foi obtida do Conselho de Revisão Institucional do IPPMG (CRI) e da Comissão Nacional de Ética em Pesquisa, CONEP. Os participantes e/ou seus pais/responsáveis assinaram o consentimento informado antes da participação e foi obtido o consentimento para crianças de sete anos ou mais velhas, conforme exigido pelo CRI local.
ResultadosForam inscritos no estudo 154 participantes infectados por HIV e 50 não infectados por HIV, nove no grupo HIV foram excluídos em 12‐18 meses (seis não fizeram o acompanhamento, um foi transferida para outro estado e um estava em uso prolongado de antibióticos) e tínhamos dados de 195 participantes; 52% dos participantes eram meninas sem diferença entre os grupos (valor de p=0,11). A idade média no momento da participação foi de 11 anos: 12 anos para participantes infectados por HIV e 10 anos para participantes não infectados por HIV (valor de p=0,02) (tabela 1).
Não houve diferenças nos escores z de índice de massa corporal média entre os infectados e não infectados por HIV; 0,39 e 0,14, respectivamente (valor de p=0,17). O grupo de participantes não infectados por HIV tem um número médio maior de pessoas que moram na mesma residência (5 em comparação com 4; valor de<0,01). Apesar de a renda familiar média em ambos os grupos ser inferior a um salário mínimo, ao considerarmos também a distribuição dessa variável, o grupo de participantes não infectados por HIV apresentou renda familiar significativamente menor (valor de p=0,01); 89% dos participantes infectados por HIV receberam TARc, 124 dos quais iniciaram a TARc antes da participação e cinco após. O tempo médio da TARc foi 7,5 anos (intervalo interquartil – 5,9‐9,9 anos); 59 (41%) apresentaram histórico de doenças Classe C pelo CDC e 85 (44%) não apresentaram CV detectável no momento da participação.
De modo geral, 14,9% (29/195) apresentaram hSBA basal>1:4 (antesda imunização), com uma maior proporção entre aqueles não infectados por HIV (30% em comparação com 9,7%; valor de p=0,01). Dentre aqueles com hSBA basal>1:4, a renda familiar média era 17% do salário mínimo.
Aos 12‐18 meses pós‐imunização, 53 (27,2%) mantiveram as titulações SBA seroprotetoras: 24,1% entre os infectados por HIV e 36% entre os não infectados por HIV (valor de p=0,14). Dos 29 indivíduos que apresentaram imunidade basal, 21 (72%) mantiveram a titulação hSBA protetora na visita aos 12‐18 meses. Apesar de a taxa de imunidade basal ter sido maior entre os não infectados por HIV, mais participantes infectados por HIV continuaram com hSBA>1:4, caso tivessem apresentado imunidade anterior no momento da participação (8/15 para participantes não infectados por HIV em comparação com 13/14 para participantes no grupo de infectados por HIV, valor de p=0,04).
Não houve diferença na taxa de seroproteção por idade no momento da participação (p=0,08) ou tempo entre a vacinação e nas visitas aos 12‐18 meses (valor de p=0,57).
A principal variável associada à persistência ao hSBA 12‐18 meses após MCC na população total, bem como para os participantes infectados por HIV, foi hSBA de basal>1:4; contudo, idade mais avançada e participantes mais pesados também foram associados à persistência ao hSBA na população total. A CV não detectável no momento da participação também foi importante no grupo de participantes infectados por HIV (tabela 2). No modelo de regressão logística, o hSBA basal >1:4 foi a variável mais significativa no modelo da população total e o mesmo foi observado no modelo do grupo de participantes infectados por HIV. Nesse último grupo, a carga viral não detectável no momento da participação (na imunização) apresentou também uma tendência de relevância (tabela 2).
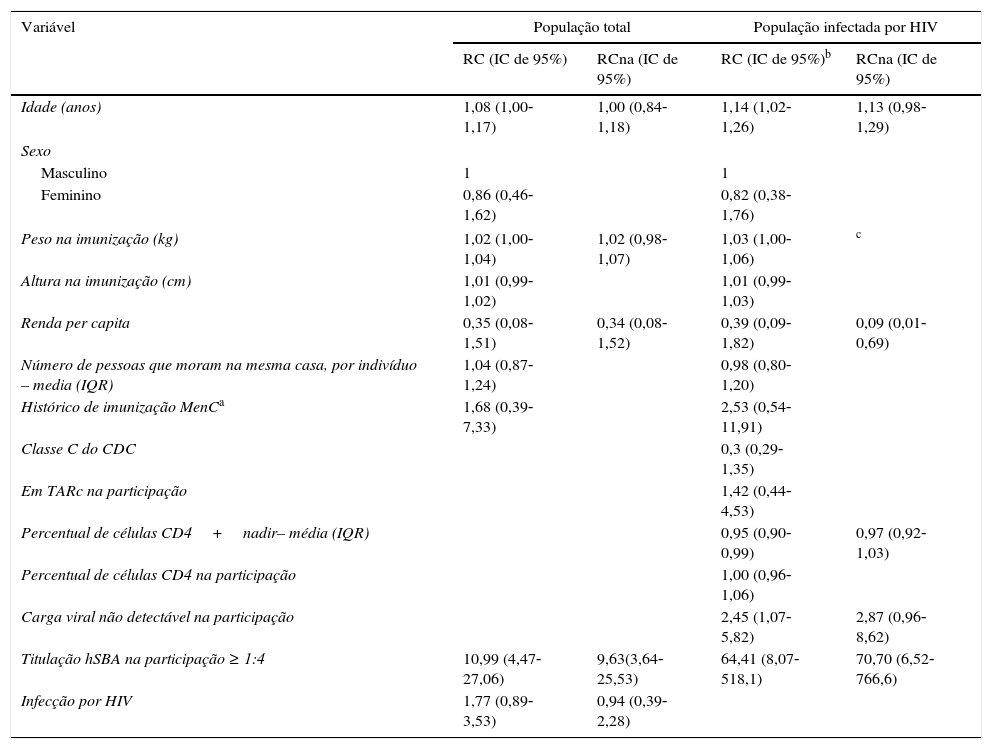
Razão de chance não ajustada e ajustada (RC e RCna) e intervalo de confiança de 95% (IC de 95%) para hSBA ≥ 1:4 após 12‐18 meses de imunização da população total (n=195) e especificamente para pessoas infectadas por HIV (n=145)
| Variável | População total | População infectada por HIV | ||
|---|---|---|---|---|
| RC (IC de 95%) | RCna (IC de 95%) | RC (IC de 95%)b | RCna (IC de 95%) | |
| Idade (anos) | 1,08 (1,00‐1,17) | 1,00 (0,84‐ 1,18) | 1,14 (1,02‐ 1,26) | 1,13 (0,98‐1,29) |
| Sexo | ||||
| Masculino | 1 | 1 | ||
| Feminino | 0,86 (0,46‐1,62) | 0,82 (0,38‐ 1,76) | ||
| Peso na imunização (kg) | 1,02 (1,00‐1,04) | 1,02 (0,98‐1,07) | 1,03 (1,00‐ 1,06) | c |
| Altura na imunização (cm) | 1,01 (0,99‐1,02) | 1,01 (0,99‐ 1,03) | ||
| Renda per capita | 0,35 (0,08‐1,51) | 0,34 (0,08‐1,52) | 0,39 (0,09‐1,82) | 0,09 (0,01‐0,69) |
| Número de pessoas que moram na mesma casa, por indivíduo – media (IQR) | 1,04 (0,87‐1,24) | 0,98 (0,80‐1,20) | ||
| Histórico de imunização MenCa | 1,68 (0,39‐7,33) | 2,53 (0,54‐11,91) | ||
| Classe C do CDC | 0,3 (0,29‐1,35) | |||
| Em TARc na participação | 1,42 (0,44‐4,53) | |||
| Percentual de células CD4+nadir– média (IQR) | 0,95 (0,90‐0,99) | 0,97 (0,92‐1,03) | ||
| Percentual de células CD4 na participação | 1,00 (0,96‐1,06) | |||
| Carga viral não detectável na participação | 2,45 (1,07‐5,82) | 2,87 (0,96‐8,62) | ||
| Titulação hSBA na participação ≥ 1:4 | 10,99 (4,47‐27,06) | 9,63(3,64‐25,53) | 64,41 (8,07‐518,1) | 70,70 (6,52‐766,6) |
| Infecção por HIV | 1,77 (0,89‐3,53) | 0,94 (0,39‐2,28) | ||
IQR, intervalo interquartil.
A persistência dos anticorpos bactericidas MCC 12‐18 meses após a imunização em crianças e adolescentes brasileiros com e sem infecção por HIV foi baixa (27,2%) e menor nas pessoas infectados por HIV, apesar de não ser estatisticamente significativa. A taxa de persistência dos anticorpos foi de acordo com o observado na literatura (19‐57%).12,15–17
A principal variável associada à persistência dos anticorpos bactericidas MCC foi a titulação hSBA ≥1:4. Para as pessoas que apresentaram imunidade basal, a vacina de dose única foi provavelmente o segundo contato com esse agente, a imunização primária foi considerada um reforço.18
Até onde sabemos, este é o primeiro estudo de persistência de anticorpos MCC em crianças e adolescentes infectados pelo HIV. Siberry et al. acompanharam 45 crianças entre 2‐10 anos por até 72 semanas após a segunda dose de vacina meningocócica ACWY.19 Eles observaram persistência de 45% dos anticorpos Neisseria meningitidis C, definido como SBA de coelhos ≥ 1:128, as taxas mais elevadas de imunidade de longo prazo foram em pacientes negros. De fato, em nossa análise multivariada, uma variável socioeconômica (SES), renda, foi associada à persistência imune. Supomos que os pacientes com situação socioeconômica inferior estiveram expostos a ambientes lotados, portanto estavam mais expostos à Neisseria meningitidis do sorogrupo C; contudo, fatores genéticos também devem desempenhar um papel na associação da SES inferior e da persistência imune.
Com base em nossos resultados, o SBA de proteção aumentou gradualmente com o tempo e são necessárias pelo menos duas doses de MCC para manter a proteção contra N. meningitides em participantes entre 2‐18 anos. Além disso, a resposta imune ideal ao MCC entre pessoas infectadas por HIV poderá coincidir com a CV não detectável, o que teria implicações sobre o tempo de imunização nesse grupo.
Em outros estudos pediátricos, a persistência antibiótica foi maior entre os pacientes mais velhos na imunização.12,16,17,20–24 Esse fenômeno não foi observado em nosso estudo, após ajuste em outras variáveis, como imunidade basal. Contudo, a infecção por HIV não foi significativamente associada à falta de resposta imunológica após 12‐18 meses da imunização, conforme esperado. Considerando que o grupo de participantes infectados por HIV apresentou pior resposta imune ao MCC 1‐2 meses após imunização,13 e como o grupo de infectados por HIV inclui participantes mais velhos do que os de não infectados por HIV e apresentou maior situação socioeconômica, talvez essas variáveis tenham desempenhado um papel importante na determinação da falta de diferença entre os grupos de participantes infectados por HIV e não infectados por HIV ou de idade. Provavelmente, o tamanho da amostra do estudo não foi suficiente para diferenciar as covariáveis em alguns grupos.
Mostramos que uma dose de vacina MCC não foi suficiente para manter a proteção imune aos 12‐18 meses entre as pessoas infectadas e não infectadas por HIV, mesmo entre as pessoas infectadas por HIV com imunidade preservada ou restaurada. Devem‐se buscar estudos que avaliam novas abordagens de vacinação. Para manter a resposta imune entre as pessoas infectadas por HIV, provavelmente é importante imunizar essas pessoas com carga viral não detectável.
FinanciamentoBolsas de estudo do Fogarty International Center of the National Institutes of Health, para CBH (n° 5R01 TW008397) e Fundação de Amparo à Pesquisa do Estado do Rio de Janeiro (Faperj) (n° #E‐26/112.645/2012) para LGM. Este trabalho também foi em parte apoiado por uma bolsa de estudos do Programa de Treinamento Global em Pesquisa de Doenças Infecciosas do Fogarty International Center, para a Universidade de Pittsburgh (n° D43TW006592). O conteúdo é exclusivamente responsabilidade dos autores e não necessariamente representa as opiniões oficiais dos institutos nacionais de saúde.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Aos pais, às crianças e aos adolescentes que participaram deste estudo.
Como citar este artigo: Frota AC, Harrison LH, Ferreira B, Menna‐Barreto D, Castro RB, Silva GP, et al. Antibody persistence following meningococcal C conjugate vaccination in children and adolescents infected with human immunodeficiency virus. J Pediatr (Rio J). 2017;93:532–7.